Composición de anticuerpos de HER2.
Una composición que comprende:
a) un especie principal de anticuerpo de HER2 que se une al dominio II de HER2,
y comprende una secuencia de aminoácidos variable ligera proporcionada como SEC ID Nº: 3 y una secuencia de aminoácidos variable pesada proporcionada como SEC ID Nº: 4; y
b) una variante de anticuerpo que comprende la especie principal de anticuerpo de HER2 y una extensión de líder amino-terminal que comprende VHS- en una cadena ligera de la variante de anticuerpo.
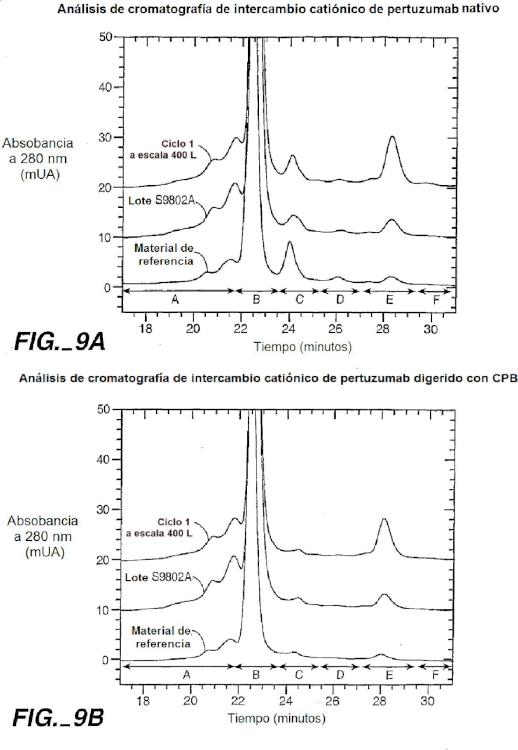
en la que del 5 % a aproximadamente el 15 % de las moléculas de anticuerpo en la composición comprenden la extensión líder amino-terminal, como se cuantifica por análisis de intercambio catiónico.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/025084.
Solicitante: GENENTECH, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1 DNA WAY SOUTH SAN FRANCISCO, CA 94080-4990 ESTADOS UNIDOS DE AMERICA.
Inventor/es: KAO,YUNG-HSIANG, VANDERLAAN,MARTIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/32 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra productos de traducción de oncogenes.
PDF original: ES-2521140_T3.pdf




Fragmento de la descripción:
Composición de anticuerpos de HER2 Campo de la invención
La presente invención se refiere a una composición que comprende un anticuerpo de HER2 de especie principal que se une con el dominio II de HER2, y una variante de secuencia de aminoácidos del mismo que comprende una extensión líder amino-terminal. La invención también se refiere a formulaciones farmacéuticas que comprenden la composición, y usos terapéuticos para la composición. La invención es como se define en las reivindicaciones
Antecedentes de la invención
Anticuerpos de HER2
La familia HER de tirosina quinasas receptoras son importantes mediadores del crecimiento, diferenciación y supervivencia celular. La familia del receptor incluye cuatro miembros diferentes incluyendo el receptor del factor de crecimiento epidérmico (EGFR, ErbB1 o HER1), HER2 (ErbB2 o p185neu), HER3 (ErbB3) y HER4 (ErbB4 o tyro2).
EGFR, codificado por el gen erbBI, se ha implicado de forma causativa en los tumores malignos humanos. En particular, se ha observado expresión aumentada de EGFR en cáncer de mama, vejiga, pulmón, cabeza, cuello y estómago así como glioblastomas. La expresión aumentada del receptor EGFR se ha asociado con frecuencia con la producción aumentada del ligando de EGFR, el factor de crecimiento transformante alfa (TGF-a), por las mismas células tumorales dando como resultado la activación del receptor por una ruta estimuladora autocrina. Baselga y Mendelsohn Pharmac. Ther. 64: 127-154 (1994). Se han evaluado anticuerpos monoclonales dirigidos contra el EGFR o sus ligandos, TGF-a y EGF, como agentes terapéuticos en el tratamiento de dichos tumores malignos. Véase, por ejemplo, Baselga y Mendelsohn., mencionado anteriormente; Masui et al Cáncer Research 44: 12- 17 (1984); y Wu etal. J. Clin. Invest. 95:1897-195 (1995).
El segundo miembro de la familia HER, p185neu, se identificó originalmente como el producto del gen transformante de neuroblastomas de ratas tratadas químicamente. La forma activada del proto-oncogén neu resulta de una mutación puntual (de valina a ácido glutámico) en la región transmembrana de la proteína codificada. Se observa amplificación del homólogo humano de neu en cánceres de mama y ováricos y se correlaciona con un mal pronóstico (Slamon et al., Science, 235: 177-182 (1987); Slamon et al., Science, 244: 77-712 (1989); y Patente de Estados Unidos N2 4.968.63). Hasta la fecha, no se ha presentado ninguna mutación puntual análoga a la del proto-oncogén neu para tumores humanos. También se ha observado sobreexpresión de HER2 (frecuentemente pero no uniformemente debida a la amplificación génica) en otros carcinomas incluyendo carcinomas del estómago, endometrio, glándula salivar, pulmón, riñón, colon, tiroides, páncreas y vejiga. Véase, entre otros, King et al., Science, 229: 974 (1985); Yokota etal., Lancet: 1: 765-767 (1986); Fukushige etal., Mol Cell Biol, 6: 955-958 (1986); Guerin et al., Oncogene Res., 3: 21-31 (1988); Cohén et al., Oncogene, 4: 81-88 (1989); Yonemura et al., Cáncer Res., 51: 134 (1991); Borst etal., Gynecol. Oncol., 38: 364 (199); Weiner et al., Cáncer Res., 5:421-425 (199); Kern etal., Cáncer Res., 5: 5184 (199); Park etal., Cáncer Res., 49: 665 (1989); Zhau etal., Mol. Carcinog. 3: 254-257 (199); Aasland et al. Br. J. Cáncer 57: 358-363 (1988); Williams et al. Pathobiology 59: 46-52 (1991); y McCann et al., Cáncer, 65: 88-92 (199). HER2 puede sobreexpresarse en cáncer de próstata (Gu et al. Cáncer Lett. 99: 185-9 (1996); Ross et al. Hum. Pathol. 28: 821-33 (1997); Ross et al. Cáncer 79: 2162-7 (1997); y Sadasivan etal. J. Urol. 15:126-31 (1993)).
Se han descrito anticuerpos dirigidos contra los productos proteicos p185neu de rata y HER2 humano. Drebin y colaboradores han inducido anticuerpos contra el producto del gen neu de rata, p185neu. Véase, por ejemplo, Drebin et al., Cell 41: 695-76 (1985); Myers et al., Meth. Enzym. 198: 277-29 (1991); y documento W94/22478. Drebin et al Oncogene 2: 273-277 (1988) indica que las mezclas de anticuerpos reactivos con dos regiones distintas de p185neu da como resultado efectos antitumorales sinérgicos en células NIH-3T3 transformadas con neu implantadas en ratones desnudos. Véase también Patente de Estados Unidos 5.824.311 presentada el 2 de octubre de 1998.
Hudziak et al., Mol. Cell. Biol. 9(3): 1165-1172 (1989) describe la generación de un panel de anticuerpos de HER2 que se caracterizaron usando la línea celular de tumor de mama humano SK-BR-3. Se determinó la proliferación celular relativa de las células SK-BR-3 después de exposición a los anticuerpos por tinción con violeta cristal de las monocapas después de 72 horas. Usando este ensayo, se obtuvo inhibición máxima con el anticuerpo llamado 4D5 que inhibía la proliferación celular en un 56 %. Otros anticuerpos en el panel redujeron la proliferación celular en un menor grado en este ensayo. Se descubrió además que el anticuerpo 4D5 sensibilizaba líneas celulares tumorales de mama que sobreexpresaban HER2 a los efectos citotóxicos del TNF-a. Véase también Patente de Estados Unidos N2 5.677.171 presentada el 14 de octubre de 1997. Los anticuerpos de HER2 analizados Hudziak et al. se caracterizan adicionalmente en Fendly et al. Cáncer Research 5: 155-1558 (199); Kotts et al. In Vitro 26(3): 59A (199); Sarup etal. Growth Regulation 1: 72-82 (1991); Shepard et al. J. Clin. Immunol. 11(3): 117-127 (1991); Kumar et al. Mol. Cell. Biol. 11(2): 979-986 (1991); Lewis et al. Cáncer Immunol. Immunother. 37: 255-263 (1993); Pietras etal. Oncogene 9: 1829-1838 (1994); Vitetta etal. Cáncer Research 54: 531-539 (1994); Sliwkowski et al.
J. Biol. Chem. 269(2): 14661-14665 (1994); Scott et al. J. Biol. Chem. 266: 143-5 (1991); Dsouza et al. Proc. Nati. Acad. Sci. 91: 722-726 (1994); Lewis et al. Cáncer Research 56: 1457-1465 (1996); y Schaefer et al. Oncogene 15:1385-1394 (1997).
Una versión humanizada recombinante del anticuerpo murino de HER2 4D5 (huMAb4D5-8, rhuMAb HER2, Trastuzumab o HERCEPTIN®; Patente de Estados Unidos N2 5.821.337) está clínicamente activo en pacientes con cánceres de mama metastásicos que sobreexpresan HER2 que han recibido terapia antineoplásica previa extensiva (Baselga et al., J. Clin. Oncol. 14: 737-744 (1996)). El trastuzumab recibió la aprobación de comercialización de la Administración de Fármacos y Alimentos el 25 de septiembre de 1998 para el tratamiento de pacientes con cáncer de mama metastásico cuyos tumores sobreexpresan la proteína HER2.
Se han descrito otros anticuerpos de HER2 con diversas propiedades en Tagliabue ef al. Int. J. Cáncer 47: 933-937 (1991); McKenzie et al. Oncogene 4: 543-548 (1989); Maier et al. Cáncer Res. 51: 5361-5369 (1991); Bacus et al. Molecular Carcinogenesis 3: 35-362 (199); Stancovski et al. PNAS (USA) 88: 8691-8695 (1991); Bacus et al. Cáncer Research 52: 258-2589 (1992); Xu et al. Int. J. Cáncer 53: 41-48 (1993); W94/136; Kasprzyk et al. Cáncer Research 52: 2771-2776 (1992); Hancock et al. Cáncer Res. 51: 4575-458 (1991); Shawver et al. Cáncer Res. 54: 1367-1373 (1994); Arteaga et al. Cáncer Res. 54: 3758-3765 (1994); Harwerth et al. J. Biol. Chem. 267: 1516-15167 (1992); Patente de Estados Unidos 5.783.186; y Klapper et al. Oncogene 14: 299-219 (1997).
La exploración de homología ha dado como resultado la identificación de otros dos miembros de la familia del receptor HER; HER3 (Patentes de Estados Unidos N2 5.183.884 y 5.48.968 así como Kraus et al. PNAS (USA) 86: 9193-9197 (1989)) y HER4 (Solicitud de Patente EP N2 599.274; Plowman et al., Proc. Nati. Acad. Sci. USA, 9: 1746-175 (1993); y Plowman et al., Nature, 366: 473-475 (1993)). Ambos de estos receptores presentan expresión aumentada en al menos algunas líneas celulares de cáncer de mama.
Los receptores HER se encuentran en general en diversas combinaciones en células y se cree que la heterodimerización aumenta la diversidad de respuestas celulares a diversos ligandos de HER (Earp et al. Breast Cáncer Research and Treatment 35: 115-132 (1995)). EGFR se une con seis ligandos diferentes; el factor de crecimiento epidérmico (EGF), el factor de crecimiento transformante alfa (TGF-a), anfirregulina, el factor de crecimiento epidérmico de unión a heparina (HB-EGF), betacelulina y epirregulina (Groenen et al. Growth Factors 11: 235-257 (1994)). Una familia de proteínas heregulinas resultante del corte y empalme alternativo de un único gen son ligandos para HER3 y HER4. La familia de heregulina incluye heregulinas alfa, beta y gamma (Holmes et al., Science, 256: 125-121 (1992); Patente de Estados Unidos N2 5.641.869; y Schaefer et al. Oncogene 15: 1385- 1394 (1997)); factores de diferenciación de neu (NDF), factores de crecimiento glial (GGF); actividad inductora del receptor de acetilcolina (ARIA);... [Seguir leyendo]
Reivindicaciones:
1. Una composición que comprende:
a) un especie principal de anticuerpo de HER2 que se une al dominio II de HER2, y comprende una secuencia de aminoácidos variable ligera proporcionada como SEC ID N2: 3 y una secuencia de aminoácidos variable pesada proporcionada como SEC ID N2: 4; y
b) una variante de anticuerpo que comprende la especie principal de anticuerpo de HER2 y una extensión de líder amino-terminal que comprende VHS- en una cadena ligera de la variante de anticuerpo.
en la que del 5 % a aproximadamente el 15 % de las moléculas de anticuerpo en la composición comprenden la extensión líder amino-terminal, como se cuantifica por análisis de intercambio catiónico.
2. La composición de la reivindicación 1, en la que la extensión líder amino-terminal es en dos cadenas ligeras de la variante de anticuerpo.
3. La composición de la reivindicación 1 o de la reivindicación 2, en la que la especie principal de anticuerpo de HER2 y la variante de anticuerpo son ambas anticuerpos intactos.
4. La composición de acuerdo con una cualquiera de las reivindicaciones anteriores en la que la especie principal del anticuerpo de HER2 comprende las secuencias de aminoácidos de cadena ligera y de cadena pesada en SEC ID N2: 15 y 16, respectivamente.
5. La composición de acuerdo con una cualquiera de las reivindicaciones anteriores en la que la extensión líder amino-terminal consiste en VHS-.
6. La composición de acuerdo con la reivindicación 4 que comprende además una segunda variante de la especie principal de anticuerpo de HER2, en donde la segunda variante de la especie principal de anticuerpo de HER2 se selecciona del grupo que consiste en:
(i) la especie principal de anticuerpo de HER2 que comprende un resto de Usina C-terminal en dos cadenas
pesadas del mismo,
(ii) la especie principal de anticuerpo de HER2 que comprende Asn-386 y/o Asn-391 desamidadas en una o dos
cadenas pesadas del mismo, y
(iii) la especie principal de anticuerpo de HER2 que comprende un resto de metionina oxidado en Met-254 de SEC ID N2: 16.
7. La composición de una cualquiera de las reivindicaciones anteriores que comprende además una variante de glucosilación del anticuerpo de la especie principal de anticuerpo HER2, en donde la variante de glucosilación se selecciona del grupo que consiste en (i) la especie principal de anticuerpo de HER2 que comprende una estructura de oligosacáridos G1 o G2 unida a una región Fe del mismo;
(ii) la especie principal de anticuerpo de HER2 que comprende un resto de carbohidrato unido a una cadena
ligera del mismo;
(iii) la especie principal de anticuerpo de HER2 que comprende una cadena pesada no glucosilada; y
(iv) la especie principal de anticuerpo de HER2 con una estructura de oligasacárido sialidado unida a una región Fe del mismo.
8. La composición de una cualquiera de las reivindicaciones anteriores en la que la especie principal de anticuerpo de HER2 se une al punto de unión entre los dominios I, II y III de HER2.
9. Un anticuerpo que comprende:
(a) una cadena ligera que comprende una secuencia de aminoácidos proporcionada como SEC ID N2: 23, o una variante desamidada y/u oxidada de la misma; y
(b) una cadena pesada que comprende una secuencia de aminoácidos proporcionada como SEC ID N2:16, SEC ID N2: 24 o una variante desamidada y/u oxidada de la misma.
1. Una formulación farmacéutica que comprende la composición de una cualquiera de las reivindicaciones 1 a 8, o el anticuerpo de la reivindicación 9 en un vehículo farmacéuticamente aceptable.
11. Una formulación farmacéutica de acuerdo con la reivindicación 1, para uso en un método para tratar cáncer que expresa HER2 en un paciente, que comprende administrar la formulación farmacéutica al paciente en una cantidad eficaz para tratar el cáncer.
12. Uso de una composición de acuerdo con una cualquiera de las reivindicaciones 1 a 8, o del anticuerpo de la reivindicación 9, en la preparación de un medicamento para tratar cáncer que expresa HER2.
Patentes similares o relacionadas:
Anticuerpo biespecífico o mezcla de anticuerpos con cadenas ligeras comunes, del 15 de Julio de 2020, de Jiangsu Alphamab Biopharmaceuticals Co., Ltd: Anticuerpo biespecífico o parte de unión a antígeno del mismo, en el que el anticuerpo biespecífico o la parte de unión a antígeno del mismo tiene una cadena […]
Anticuerpos contra HER2 biespecíficos, del 1 de Julio de 2020, de MEDIMMUNE, LLC: Un anticuerpo anti-HER2 biespecifico que comprende un primer dominio de union a antigeno de inmunoglobulina y un segundo dominio de union a antigeno de inmunoglobulina, […]
Anticuerpos anti-CD3 y métodos de uso, del 27 de Mayo de 2020, de GENENTECH, INC.: Un anticuerpo anti-CD3 que es un anticuerpo biespecífico, en donde el anticuerpo biespecífico comprende un brazo anti-CD3 que comprende un primer dominio de unión que […]
Anticuerpos anti-CD3 y métodos de uso, del 27 de Mayo de 2020, de GENENTECH, INC.: Un anticuerpo biespecífico que comprende un brazo anti-CD3 que comprende un primer dominio de unión que comprende (a) un dominio VH que comprende una secuencia de aminoácidos […]
Moléculas de fusión anticuerpos-mutante de interferón modificadas, del 6 de Mayo de 2020, de ImmunGene, Inc: Una molécula de fusión genéticamente modificada que comprende un anticuerpo antígeno asociado a tumor (AAT) (Ab) unido a una molécula mutante de interferón alfa (IFN-α), […]
Proteínas que comprenden regiones efectoras de la subunidad A de la toxina Shiga próximas al extremo amino terminal y regiones de unión de tipo inmunoglobulina de reconocimiento celular capaces de unirse específicamente a HER2/neu/ErbB2, del 6 de Mayo de 2020, de MOLECULAR TEMPLATES, INC: Proteína citotóxica que comprende: a) una región de unión de tipo inmunoglobulina que comprende uno o más polipéptidos y es capaz de unirse específicamente a […]
Inmunotoxinas de unión a CD20 para inducir la internalización celular y procedimientos que usan las mismas, del 6 de Mayo de 2020, de MOLECULAR TEMPLATES, INC: Una proteína de unión a CD20 que comprende: a) una región de unión a CD20 que comprende una región de unión de tipo inmunoglobulina: (i) capaz […]
Células NK-92 que expresan CAR como agentes terapéuticos celulares, del 6 de Mayo de 2020, de CHEMOTHERAPEUTISCHES FORSCHUNGSINSTITUT GEORG-SPEYER-HAUS: Una célula o línea celular NK-92 específica de ErbB2, que contiene un vector lentiviral que codifica un receptor de antígeno quimérico que comprende […]