Células troncales mesenquimatosas que expresan el receptor de TNF.
Procedimiento para la obtención de células troncales mesenquimatosas que expresan el receptor de TNF-α
deTipo I en una cantidad de por lo menos 13 pg/106 células, que comprende:
determinar la cantidad de receptor de TNF-α de Tipo I expresado por las células troncales mesenquimatosas encada una de por lo menos una población celular que incluye las células troncales mesenquimatosas obtenidas depor lo menos un donante; y
seleccionar las células troncales mesenquimatosas que expresan el receptor de TNF-α de Tipo I en una cantidadde por lo menos 13 pg/106 células.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/000274.
Solicitante: OSIRIS THERAPEUTICS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 7015 Albert Einstein Drive Columbia, MD 21046 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DANILKOVITCH,ALLA, CARTER,DIANE, TYRELL,ALICIA, BUBNIC,SIMON, MARCELINO,MICHELLE, MONROY,RODNEY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/0775 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre mesenquimales; Células madre derivadas de tejido adiposo.
PDF original: ES-2415855_T3.pdf
Fragmento de la descripción:
Células troncales mesenquimatosas que expresan el receptor de TNF.
La presente invención se refiere a un procedimiento para la obtención de células troncales (stem) mesenquimatosas que expresan el receptor del factor de necrosis tumoral alfa (TNF-a) de Tipo I (TNFRI) , en una cantidad de por lo menos 13 pg/106 células. Estas células troncales mesenquimatosas inhiben la proliferación de los linfocitos.
Las células troncales mesenquimatosas (MSC) son células troncales histoespecíficas que se pueden diferenciar fácilmente en líneas celulares que incluyen osteoblastos, miocitos, condrocitos y adipocitos (Pittenger, et al., Science, Vol. 284. pg. 143 (1999) ; Haynesworth, et al., Bone, Vol. 13, pg. 69 (1992) ; Prockop, Science, Vol. 276, pg. 71 (1997) ) . Los estudios in vitro han demostrado la capacidad de las MSC para diferenciarse en músculo (Wakitani, et al., Muscle Nerve, Vol. 18, pg. 1417 (1995) ) , precursores neuronales (Woodbur y , et al., J. Neurosci. Res., Vol. 69, pg. 908 (2002) ; Sanchez-Ramos, et al., Exp. Neurol., Vol. 171, pg. 109 (2001) ) cardiomiocitos (Toma, et al., Circulation, Vol. 105, pg. 93 (2002) ; Fakuda, Artif. Organs, Vol. 25, pg. 187 (2001) ) y posiblemente otros tipos de células. Además, se ha demostrado que las MSC proporcionan capas de alimentación eficaces para la expansión de las células troncales hematopoyéticas (Eaves, et al., Ann. N.Y. Acad. Sci., Vol. 938, pg. 63 (2001) ; Wagers, et al., Gene Therapy, Vol. 9, pg. 606 (2002) ) . Estudios recientes con diferentes modelos animales han demostrado que las MSC pueden ser útiles en la reparación o regeneración del hueso, del cartílago, del menisco o de los tejidos miocardicos dañados (Dekok, et al., Clin. Oral Implants Res., Vol. 14, pg. 481 (2003) ) ; Wu et al., Transplantation, Vol. 75, pg. 679 (2003) ; Noel, et al., Curr. Opin. Investig. Drugs, Vol. 3, pg. 1000 (2002) ; Ballas, et al., J. Cell. Biochem. Suppl., Vol. 38, pg. 20 (2002) ; Mackenzie, et al., Blood Cells Mol. Dis., Vol. 27, pgs. 601-604 (2001) ) . Varios investigadores han utilizado las MSC con resultados esperanzadores para el trasplante en modelos animales de enfermedades que incluyen la osteogénesis imperfecta (Pereira, et al., Proc. Nat. Acad. Sci., Vol. 95, pg. 1142 (1998) ) , el Parkinson (Schwartz, et al., Hum. Gene Ther., Vol. 10, pg. 2539 (1999) ) , lesiones en la médula espinal (Chopp, et al., Neuroreport, Vol. 11, pg. 3001 (2000) ; Wu, et al., J. Neurosci. Res., Vol. 72, pg. 393 (2003) ) y trastornos cardíacos (Tomita et al., Circulation, Vol. 100, pg. 247 (1999) ; Shake, et al., Ann. Thorac. Surg., Vol. 73, pg. 1919 (2002) ) . De forma importante, también se han publicado resultados prometedores de ensayos clínicos para la osteogénesis imperfecta (Horowitz, et al., Blood, Vol. 97, pg. 1227 (2001) ; Horowitz, et al., Proc. Nat. Acad. Sci., Vol. 99, pg. 8932 (2002) ) y mejoras en injertos en trasplantes heterólogos de médula ósea (Frassoni, et al., Int. Society for Cell Therapy, SA006 (abstract) (2002) ; Koc, et al.; J. Clin. Oncol., Vol. 18, págs. 307-316 (2000) ) .
Además, los estudios in vitro de distintos laboratorios han demostrado que las MSC pueden inhibir la proliferación de linfocitos T tanto en cultivos de mezclas de linfocitos o mediante otros estímulos como los antígenos y los mitógenos (Di Nicola, et al., Blood, Vol. 99, pgs. 3638-3843 (2002) ; Tse et al., Transplantation, Vol. 75, pgs. 389-397 (2003) ; Aggarwal, et al., Blood, Vol. 105, pgs. 1815-1822 (2005) ) . Los resultados recientes de estudios in vitro demuestran además que las MSC hacen disminuir la secreción de las citocinas proinflamatorias, el factor de necrosis tumoral alfa (TNF-a) y el interferón-y (IFN-y) , y simultáneamente hace aumentar la producción de las citocinas antiinflamatorias Interleucina-10 (IL-10) e Interleucina-4 (IL-4) a través de las células inmunitarias. (Aggarwal, 2005) . Estos resultados indican que debido a las actividades inmunoreguladoras y antiinflamatorias, las MSC pueden ser beneficiosas para el tratamiento de respuestas inmunológicas que tienen lugar en patologías de injerto contra el huésped (EICH) , trasplantes de órganos sólidos y enfermedades autoinmunitarias como la esclerosis múltiple y la artritis reumatoide. Un informe de un caso clínico que demuestra el efecto terapéutico de las MSC en casos de EICH agudos apoya firmemente esta hipótesis. (Le Blanc, et al., The Lancet, Vol. 363, págs. 1439-1441 (2004) ) .
Los receptores del TNF-a se expresan en la superficie de las células troncales mesenquimatosas. Los datos acumulados indican que el TNF-a es un regulador importante de la función de las células troncales mesenquimatosas. La incubación de TNF-a en cultivos de células troncales mesenquimatosas humanas sobrerregula la prostaglandina E2 (PGE2) y la secreción del factor de crecimiento del queratinocito, induce la actividad de la enzima idoleamina 2, 3 desoxigenasa (IDO) y estimula la migración celular. Se ha demostrado que el TNF-a está presente en sitios con heridas e inflamación, especialmente en los órganos que son diana de la enfermedad del injerto contra el huésped. (Koide, et al., Transplantation, Vol. 64, pgs. 518-524 (1997) ; Kuroiwa, et al., J. Clin. Invest., Vol. 107, pgs. 1365-1373 (2001) ; Deans, et al., Exp. Hematol., Vol. 28, págs. 875-884 (2002) ; Ellison, et al., J. Clin. Immunol., Vol. 24, pgs. 197-211 (2004) ) . Por consiguiente, estos datos indican que la expresión de los receptores del TNF-a por parte de las células troncales mesenquimatosas puede ser decisiva para las actividades inmunosupresoras, inmunorreguladoras, antiinflamatorias, de reparación del tejido o de la curación de heridas, así como la migración a los lugares que presentan inflamación.
Existen dos tipos de receptores de TNF-a, o TNFRs: el Tipo I (TNFRI) , también conocido como p55, y el Tipo II (TNFR II) , también conocido como p75. (Tartaglia, et al., Proc. Nat. Acad. Sci., Vol. 88, págs. 9292-9296 (1991) .) Ambos tipos de receptores de TNF-a están presentes en las MSC; sin embargo, el TNFRI es el tipo predominante. (Vancheri, et al., Am. J. Respir. Cell. Mol. Biol., Vol. 22, págs. 628-634 (2000) ; Debets, et al., Cytokine, Vol. 8, págs. 80-88 (1996) ) .
A continuación se describirá la invención haciendo referencia a las figuras en las que: La figura 1 es un gráfico que muestra la correlación entre la expresión del TNFRI y la capacidad de las MSC para inhibir la proliferación de PBMC in vitro;
La Figura 2 es un gráfico que muestra la expresión del TNFRI por células troncales mesenquimatosas almacenadas a una temperatura de -80ºC, -70ºC, -60ºC y -50ºC;
La Figura 3 es un gráfico que muestra la expresión del TNFRI y la capacidad para inhibir la proliferación de PBMC in vitro de las células troncales mesenquimatosas almacenadas a una temperatura de -80ºC y a -50ºC; y
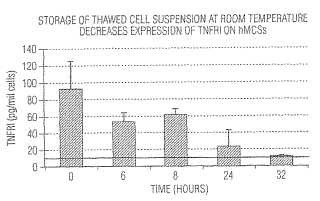
La Figura 4 es un gráfico que muestra la expresión del TNFRI por las células troncales mesenquimatosas almacenadas a una temperatura de -135ºC o inferior, y después descongeladas y mantenidas a temperatura ambiente durante 6, 8, 24 ó 32 horas.
Según un aspecto de la presente invención, se proporciona un procedimiento para la obtención de células troncales mesenquimatosas que expresan el receptor TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células, que comprende:
determinar la cantidad de receptor de TNF-a de Tipo I expresado por las células troncales mesenquimatosas en cada uno de por lo menos una población celular que incluye las células troncales mesenquimatosas obtenidas de por lo menos un donante; y
seleccionar las células troncales mesenquimatosas que expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células.
Según otro aspecto de la presente invención, se proporciona un procedimiento para la determinación de la potencia inmunosupresora de las células troncales mesenquimatosas que comprende la medición del nivel de expresión del receptor del TNF-a de Tipo I por las células troncales mesenquimatosas.
Según otro aspecto de la presente invención, se proporciona un procedimiento para la selección de células troncales mesenquimatosas que presentan una actividad inmunosupresora que comprende la selección de una población de células troncales mesenquimatosas que expresan el receptor del TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células.
Las células troncales mesenquimatosas expresan el receptor del TNF-a de Tipo I (TNFRI) en una cantidad eficaz para inhibir la proliferación de linfocitos. En una forma de realización, las células troncales mesenquimatosas expresan el TNFRI en una cantidad de por lo menos 13 pg/106 células. En otra forma de realización, las células troncales mesenquimatosas expresan... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la obtención de células troncales mesenquimatosas que expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células, que comprende:
determinar la cantidad de receptor de TNF-a de Tipo I expresado por las células troncales mesenquimatosas en cada una de por lo menos una población celular que incluye las células troncales mesenquimatosas obtenidas de por lo menos un donante; y
seleccionar las células troncales mesenquimatosas que expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células.
2. Procedimiento según la reivindicación 1 en el que dichas células troncales mesenquimatosas expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 15 pg/106 células, preferentemente 18 pg/106 células.
3. Procedimiento para la determinación de la potencia inmunosupresora de las células troncales mesenquimatosas que comprende la medición del nivel de expresión del receptor de TNF-a de Tipo I por parte de las células troncales mesenquimatosas.
4. Procedimiento según la reivindicación 3 en el que la expresión del receptor de TNF-a de Tipo I se mide mediante un ensayo de inmunoabsorción ligada a enzima.
5. Procedimiento según cualquiera de las reivindicaciones 1 a 4 en el que dichas células troncales mesenquimatosas son células troncales mesenquimatosas humanas.
6. Procedimiento para la selección de células troncales mesenquimatosas con actividad inmunosupresora que comprende la selección de una población de células troncales mesenquimatosas que expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 13 pg/106 células.
7. Procedimiento según la reivindicación 6 en el que se selecciona una población de células troncales mesenquimatosas que expresan el receptor de TNF-a de Tipo I en una cantidad de por lo menos 18 pg/106 células.
8. Procedimiento según la reivindicación 6 o 7 que comprende además la mezcla de dicha población celular seleccionada con un vehículo farmacéutico.
Patentes similares o relacionadas:
Función promotora del crecimiento del cabello de células madre de tamaño pequeño y uso de las mismas, del 6 de Mayo de 2020, de MEDIPOST, CO., LTD.: Una composición para su uso en la terapia de pérdida de cabello para prevenir la pérdida de cabello y estimular el crecimiento del cabello, que comprende: células […]
Terapia con células madre basada en células madre procedentes de tejido adiposo, del 6 de Mayo de 2020, de RIGSHOSPITALET: Una composición que comprende una suspensión de una población sustancialmente homogénea e inmunosupresora de células madre procedentes de tejido adiposo (ASC) humanas adultas […]
Métodos y composiciones para modular la diferenciación de células pluripotenciales, del 1 de Abril de 2020, de SANBIO, INC: Método para restringir el potencial de una célula estromal adherente de médula para diferenciarse en un linaje condrogénico, comprendiendo […]
Composiciones y métodos de células grasas marrones, del 1 de Abril de 2020, de Biorestorative Therapies, Inc: Un método para generar una célula grasa marrón, el método comprende: aislar una célula madre de un tejido graso marrón obtenido; y cultivar la célula […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en hepatocitos, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en hepatocitos, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un medio […]
Método para diferenciar, células madre pluripotentes inducidas a partir de células madre mesenquimatosas, en neuronas, del 26 de Febrero de 2020, de BBHC Co. Ltd: Un método para diferenciar células madre mesenquimatosas en neuronas, que comprende las etapas de: (a) añadir un extracto de Ecklonia cava a un […]
Método para la producción de célula madre pluripotente inducida a partir de célula madre mesenquimatosa y célula madre pluripotente inducida producida mediante el método, del 12 de Febrero de 2020, de BBHC Co. Ltd: Método para la producción de una célula madre pluripotente inducida, comprendiendo el método: añadir un extracto de Ecklonia cava a un medio […]
Método de proliferación celular y agente farmacéutico para reparación y regeneración de tejido, del 12 de Febrero de 2020, de Sapporo Medical University: Método para hacer crecer células madre mesenquimatosas humanas en una muestra recogida de un sujeto vivo cultivando las células en un medio, comprendiendo […]