Células madre mesenquimatosas y sus utilizaciones.
Células madre mesenquimatosas no manipuladas genéticamente para su utilización en el tratamiento de laencefalomielitis autoinmunitaria,
la esclerosis múltiple o las enfermedades inflamatorias del intestino en un animal.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/008506.
Solicitante: OSIRIS THERAPEUTICS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2001 ALICEANNA STREET BALTIMORE, MD 21231 ESTADOS UNIDOS DE AMERICA.
Inventor/es: PITTENGER, MARK, F., AGGARWAL,SUDEEPTA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00).
PDF original: ES-2385450_T3.pdf
Fragmento de la descripción:
Células madre mesenquimatosas y sus utilizaciones.
La presente invención se refiere a nuevas utilizaciones para las células madre mesenquimatosas.
Las células madre mesenquimatosas (MSC) son células madre pluripotentes que pueden diferenciarse fácilmente en linajes incluyendo los osteoblastos, los miocitos, los condrocitos y los adipocitos (Pittenger, et al., Science, Vol. 284, pág. 143 (1999) ; Haynesworth, et al., Bone, Vol. 13, pág. 69 (1992) ; Prockop, Science, Vol. 276, pág. 71 (1997) ) . Los estudios in vitro han demostrado la capacidad de las MSC para diferenciarse en el músculo (Wakitani, et al., Muscle Nerve, Vol. 18, pág. 1417 (1995) ) , precursores de tipo neuronal (Woodbur y , et al., J. Neurosci. Res., Vol. 69, pág. 908 (2002) ; Sanchez-Ramos, et al., Exp. Neurol., Vol. 171, pág. 109 (2001) ) , cardiomiocitos (Toma, et al., Circulation, Vol. 105, pág. 93 (2002) ; Fakuda, Artif. Organs, Vol. 25, pág. 187 (2001) ) y posiblemente otros tipos de células. Además, se ha demostrado que las MSC proporcionan capas de alimentación eficaces para la expansión de las células madre hematopoyéticas y embrionarias (Eaves, et al., Ann. N.Y. Acad. Sci., Vol. 938, pág. 63 (2001) ; Wagers, et al., Gene Therapy, Vol. 9, pág. 606 (2002) ) . Los estudios recientes con una variedad de modelos de animales han demostrado que las MSC pueden ser útiles en la reparación o regeneración de los tejidos dañados de hueso, cartílago, menisco o miocardio (DeKok, et al., Clin. Oral Implants Res., Vol. 14, pág. 481 (2003) ) ; Wu, et al., Transplantation, Vol. 75, pág. 679 (2003) ; Noel, et al., Curr. Opin. Investig. Drugs, Vol. 3, pág. 1000 (2002) ; Ballas, et al., J. Cell. Biochem. Suppl., Vol. 38, pág. 20 (2002) ; Mackenzie, et al., Blod Cells Mol. Dis., Vol. 27 (2002) ) . Varios investigadores han utilizado las MSC con resultados alentadores para el trasplante en modelos de enfermedades de animales incluyendo la osteogenia imperfecta (Pereira, et al., Proc. Nat. Acad. Sci., Vol. 95, pág. 1142 (1998) ) , el parkinsonismo (Schwartz, et al., Hum. Gene Ther., Vol. 10, pág. 2539 (1999) ) , lesión de la médula espinal (Chopp, et al., Neuroreport, Vol. 11, pág. 3001 (2000) ; Wu, et al., J. Neurosci. Res., Vol. 72, pág. 393 (2003) ) y trastornos cardíacos (Tomita, et al., Circulation, Vol. 100, pág. 247 (1999) ; Shake, et al., Ann. Thorac. Surg., Vol. 73, pág. 1919 (2002) ) . En gran medida, se han publicado también resultados prometedores en pruebas clínicas para la osteogenia imperfecta (Horowitz, et al., Proc. Nat. Acad. Sci., Vol. 99, pág. 8932 (2002) ) y el aumento de trasplante de trasplantes heterólogos de medula ósea (Frassoni, et al., Int. Society for Cell Therapy, SA006 (resumen) (2002) ; Koc, et al., J. Clin. Oncol., Vol. 18, pág. 307 (2000) ) .
Las MSC expresan el antígeno de clase I del complejo con histocompatibilidad mayor (MHC) en su superficie pero limitaban el MHC de clase II (Le Blanc, et al., Exp. Hematol., Vol. 31, pág. 890 (2003) ; Potian, et al., J. Immunol., Vol. 171, pág. 3426 (2003) ) y moléculas coestimulantes ni B7 ni CD40 (Majumdar, et al., J. Biomed. Sci., Vol. 10, pág. 228 (2003) ) , lo que sugiere que estas células tienen un fenotipo poco inmunógeno (Tse, et al., Transplantation, Vol. 75, pág. 389 (2003) ) . Las MSC inhiben también las respuestas proliferantes de los linfocitos T de manera independiente de MHC (Bartholomew, et al., Exp. Hematol., Vol. 30, pág. 42 (2002) ; Devine, et al., Cancer J., Vol. 7, pág. 576 (2001) ; DiNicola, et al., Blood, Vol. 99, pág. 3838 (2002) ) . Estas propiedades inmunológicas de las MSC pueden acentuar su implante del trasplante y limitar la capacidad del sistema inmunitario del receptor para reconocer y rechazar las células del alotrasplante después del trasplante. La producción de factores por las MSC, que modulan la respuesta inmunitaria y ayudan a la hematopoyesis junto con su capacidad para diferenciarse en tipos de células apropiadas bajo estímulos locales las convierten en células madre deseables para los estudios de trasplante celular (Majundar, et al., Hematother. Stem. Cell. Res., Vol. 9, pág. 841 (2000) ; Haynesworth, et al., J. Cell. Physiol., Vol. 166, pág. 585 (1996) ) .
Los documentos US 2003/049843, WO 03/004661 y EP 1 279 738 describen vehículos adenovíricos con un tropismo para las células madre mesenquimatosas destinadas a suministrar ácidos nucleicos de interés a las células madre mesenquimatosas. El documento WO 01/80865 da a conocer la reparación de articulaciones lesionadas o enfermas mediante la administración de células madre mesenquimatosas para sustituir el tejido desaparecido y/o dañado en la articulación. El documento WO 2004/006942 describe un procedimiento para mantener el suministro de las células en un área objetivo en un cuerpo de mamífero, en el que las células, por ejemplo, células madre mesenquimatosas normales o modificadas genéticamente, se introducen a través de una zona de introducción de un área objetivo y un elemento tampón que contiene un agente terapéutico se deposita en el punto de introducción. El documento WO 03/105908 describe el direccionamiento de las células, por ejemplo, células madre mesenquimatosas expandidas en el cultivo, a un tejido objetivo utilizando una molécula que presenta el carbohidrato. El documento WO 03/068248 describe la inducción de la formación del folículo de cabello en una capa dérmica que está situada bajo una superficie externa de la piel suministrando células inductivas de la cubierta dérmica y/o células inductivas de la papila dérmica, por ejemplo, las procedentes de células madre mesenquimatosas, en la capa dérmica utilizando un dispositivo de suministro. El documento WO 03/078609 describe procedimientos de inducir diferenciación de células madre tales como las células madre mesenquimatosas cultivando las células en presencia de una muestra de tejido y/o medio extracelular de una muestra de tejido. El documento US 2002/110544 se refiere a la utilización de células madre mesenquimatosas para regenerar el cartílago hialino en osteoartritis. El documento KR 10-2004-0016785 describe la transdiferenciación de células madre mesenquimatosas en células neuronales transduciendo células madre mesenquimatosas con factores de transcripción hélice-bucle-hélice básicos (bHLH, por sus siglas en inglés) neurógenos. El documento WO 00/49136 describe células madre mesenquimatosas que están genéticamente modificadas con un ácido nucleico que modifica un polipéptido supresor del sistema inmunitario para evitar el rechazo de las células madre mesenquimatosas por un receptor. El documento WO 03/059276 describe células de
desarrollo más potente producidas a partir de células de desarrollo menos potente tales como las células madre mesenquimatosas y las utilizaciones potenciales de las mismas.
Los solicitantes actualmente han examinado las interacciones de las células madre mesenquimatosas con poblaciones de células inmunitarias aisladas, incluyendo los dendrocitos (DC1 y DC2) , los linfocitos T efectores (Th1 y Th2) y las células NK. Basándose en dichas interacciones, los solicitantes descubrieron que las células madre mesenquimatosas pueden regular la producción de varios factores que pueden regular varias etapas en los procesos de respuesta inmunitaria. De este modo, las células madre mesenquimatosas pueden emplearse en el tratamiento de enfermedades y trastornos que implican al sistema inmunitario, o enfermedades, afecciones o trastornos que implican inflamación o respuestas alérgicas. Dichas enfermedades, afecciones y trastornos comprenden de manera no limitativa, enfermedades autoinmunitarias, alergias, artritis, heridas inflamadas, alopecia circunscrita (calvicie) , enfermedades periodontales incluyendo la gingivitis y periodontitis, y otras enfermedades, afecciones o trastornos que implican una respuesta inmunitaria.
Además, se cree que las células madre mesenquimatosas estimulan las células mononucleares de la sangre periférica (PBMC) para producir el factor de crecimiento endotelial vascular, o VEGF, que favorece la angiogenia al estimular la formación de nuevos vasos sanguíneos.
Además, se cree que las células madre mesenquimatosas estimulan los dendrocitos (DC) al producir interferón-beta (IFN-º) , que favorece la supresión tumoral y la inmunidad contra la infección vírica.
La presente invención proporciona células madre mesenquimatosas no manipuladas genéticamente para el tratamiento de la encefalomielitis autoinmunitaria, la esclerosis múltiple o las enfermedades inflamatorias del intestino en un animal.
Aunque el alcance de la presente invención no debe limitarse... [Seguir leyendo]
Reivindicaciones:
1. Células madre mesenquimatosas no manipuladas genéticamente para su utilización en el tratamiento de la encefalomielitis autoinmunitaria, la esclerosis múltiple o las enfermedades inflamatorias del intestino en un animal. 5
2. Células madre mesenquimatosas no manipuladas genéticamente para su utilización en el tratamiento de la encefalomielitis autoinmunitaria, la esclerosis múltiple o las enfermedades inflamatorias del intestino tal como se han caracterizado en la reivindicación 1, que están destinadas a ser administradas en combinación con un fármaco antinflamatorio.
3. Células madre mesenquimatosas no manipuladas genéticamente para su utilización en el tratamiento de la encefalomielitis autoinmunitaria, la esclerosis múltiple o las enfermedades inflamatorias del intestino tal como se han caracterizado en la reivindicación 1 ó 2 en las que el animal es un mamífero.
4. Células madre mesenquimatosas no manipuladas genéticamente para su utilización en el tratamiento de la encefalomielitis autoinmunitaria, la esclerosis múltiple o las enfermedades inflamatorias del intestino tal como se han caracterizado en la reivindicación 3 en las que el animal es un ser humano.
Patentes similares o relacionadas:
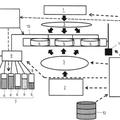 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Composiciones mejoradas para hidrogeles, del 22 de Julio de 2020, de Biogelx Limited: Una composición de hidrogel, que comprende una mezcla de los derivados peptídicos primero y segundo en una proporción de 1:4 a 4:1, en donde los primeros derivados […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Producción de tapsigarginas por cultivo en suspensión de células de Thapsia, del 6 de Mayo de 2020, de PHYTON HOLDINGS, LLC: Método de producción de lactonas sesquiterpénicas de la familia de tapsigargina, comprendiendo el método las etapas de: (a) cultivar células vegetales […]
Composición de medio para preparar toxina botulínica, del 6 de Mayo de 2020, de Daewoong Co., Ltd: Una composición de medio libre de EET para su uso en el cultivo de Clostridium botulinum, la composición de medio comprende: peptonas de origen […]
Células virales resistentes y sus usos, del 22 de Abril de 2020, de Sigma-Aldrich Co. LLC: Una línea celular de ovario de hámster chino (CHO) modificada genéticamente en la que la entrada y/o propagación del virus diminuto del ratón (MVM) […]
Composiciones de cultivo de células con antioxidantes y procedimientos para la producción de polipéptidos, del 15 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento de producción de un anticuerpo o un fragmento del mismo producido recombinantemente que comprende la etapa de cultivar una célula que comprende […]