Catalizador para la reducción de oxígeno.
Un catalizador para la reducción de oxígeno que comprende un sulfuro de rutenio y cobalto químicamente estable en un ambiente clorhídrico en presencia de cloro disuelto y opcionalmente de oxígeno disuelto,
en el que dicho sulfuro es RuxCoyS soportado sobre negro de carbono.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11160589.
Solicitante: INDUSTRIE DE NORA S.P.A.
Nacionalidad solicitante: Italia.
Dirección: VIA BISTOLFI 35 20134 MILANO ITALIA.
Inventor/es: DE CASTRO, EMORY S., ALLEN, ROBERT J., GULLA,Andrea,F.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01J21/18 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 21/00 Catalizadores que contienen los elementos, los óxidos o los hidróxidos de magnesio, de boro, de aluminio, de carbono, de silicio, de titanio, de zirconio o de hafnio. › Carbono.
- B01J23/89 B01J […] › B01J 23/00 Catalizadores que contienen metales, óxidos o hidróxidos metálicos no previstos en el grupo B01J 21/00 (B01J 21/16 tiene prioridad). › combinados con metales nobles.
- B01J27/045 B01J […] › B01J 27/00 Catalizadores que contienen los elementos o compuestos de halógenos, azufre, selenio, teluro, fósforo, o nitrógeno; Catalizadores que comprenden compuestos de carbono. › Metales del grupo del platino.
- C25B1/26 QUIMICA; METALURGIA. › C25 PROCESOS ELECTROLITICOS O ELECTROFORETICOS; SUS APARATOS. › C25B PROCESOS ELECTROLITICOS O ELECTROFORETICOS PARA LA PRODUCCION DE COMPUESTOS ORGANICOS O INORGANICOS, O DE NO METALES; SUS APARATOS (protección anódica o catódica C23F 13/00; crecimiento de monocristales C30B). › C25B 1/00 Producción electrolítica de compuestos inorgánicos o no metales. › Cloro; Sus compuestos (por producción simultánea de hidróxidos de metales alcalinos y de cloro, de sus oxiácidos o de sus sales C25B 1/34).
- C25B11/04 C25B […] › C25B 11/00 Electrodos; Su fabricación no prevista en otro lugar. › caracterizados por el material.
- H01M4/86 ELECTRICIDAD. › H01 ELEMENTOS ELECTRICOS BASICOS. › H01M PROCEDIMIENTOS O MEDIOS, p. ej. BATERÍAS, PARA LA CONVERSION DIRECTA DE LA ENERGIA QUIMICA EN ENERGIA ELECTRICA. › H01M 4/00 Electrodos. › Electrodos inertes que tienen una actividad catalítica, p. ej. para pilas de combustible.
- H01M4/88 H01M 4/00 […] › Procesos de fabricación.
- H01M4/90 H01M 4/00 […] › Empleo de material catalítico específico.
PDF original: ES-2522538_T3.pdf
Fragmento de la descripción:
Catalizador para la reducción de oxígeno ANTECEDENTES DE LA INVENCIÓN
La electrólisis de soluciones acuosas de HCI es un método muy conocido para la recuperación de cloro gaseoso de gran valor. El ácido clorhídrico acuoso es un subproducto químico abundante, especialmente en plantas químicas que hacen uso de cloro como un reaccionante: en este caso, el cloro desprendido en el compartimento anódlco del electrolizador se puede reciclar como un material de alimentación a la planta química. La electrólisis se vuelve extremadamente atractiva cuando el cátodo estándar que desprende hidrógeno se reemplaza por un electrodo de difusión de gas que consume oxígeno debido a la disminución asociada en el consumo de energía. La capacidad del electrodo de difusión de gas para funcionar satisfactoriamente en este contexto depende cruclalmente de la naturaleza y el rendimiento del catalizador, y así de la estructura del electrodo de difusión de gas.
El platino se conoce generalmente como el catalizador más eficaz para la electrorreducclón de oxígeno en una amplia gama de condiciones; la activación de electrodos de difusión de gas con catalizadores basados en platino es muy conocida en la técnica, y encuentra una amplia aplicación en pilas de combustible y electrolizadores de muchos tipos. Sin embargo, el caso de la electrólisis de HCI acuoso plantea Importantes desventajas en el uso de platino como catalizador catódico, ya que es inevitable que el cátodo de difusión de gas entre en contacto al menos parcialmente con el electrolito líquido, que contiene ion cloruro y cloro disuelto. Ante todo, el platino es susceptible de envenenamiento con Iones cloruro que afecta negativamente a su actividad hacia la reducción de oxígeno; una segunda fuente de envenenamiento está constituida por especies contaminantes, especialmente especies orgánicas, que en la mayoría de los casos están disueltas en el ácido clorhídrico obtenido como subproducto que sufre electrólisis. De forma aún más importante, la acción complejante combinada del ácido clorhídrico y el cloro gaseoso disuelto convierte al platino metálico en una sal soluble que se disuelve, haciendo este material Inapropiado para el uso en electrodos de difusión de gas. Por otra parte, se tienen que tomar precauciones extremadamente cuidadosas durante las paradas periódicas de los electrolizadores, de otro modo el cambio repentino en el potencial catódico, combinado con el ambiente químico muy agresivo, provoca la disolución de una cantidad significativa de catalizador, y la desactivación parcial de la porción restante. Aunque se pueden establecer procedimientos adaptados para paradas planeadas de los electrolizadores con costes adicionales, poco o nada se puede hacer en el caso de una parada descontrolada repentina debida a causas impredecibles como cortes de energía en la red eléctrica.
Estos problemas se han mitigado parcialmente con la divulgación de algunos catalizadores basados en rodio, que han resultado ser menos activos que el platino para la reacción de reducción de oxígeno, pero menos afectados por los iones cloruro presentes en el sistema, dando así resultados más que aceptables por lo que se refiere al voltaje de funcionamiento al incorporarlos en electrodos de difusión de gas. En particular, el catalizador de rodio metálico/óxido de rodio divulgado en la Patente de EE. UU. 5.958.197 también resultaba bastante resistente al ambiente clorhídrico en presencia de cloro disuelto y oxígeno, aunque requiere procedimientos de activación engorrosos para desarrollar completamente su forma resistente a la corrosión.
La Patente de EE. UU. 6.149.782 divulgaba un catalizador aún más resistente basado en sulfuro de rodio, que no requiere ninguna etapa de activación y que muestra la ventaja adicional de ser insensible a contaminantes orgánicos del material de alimentación ácido.
Aunque estos catalizadores muestran comportamientos muy buenos tanto en cuanto a la actividad como a la resistencia química en el ambiente duro asociado con la electrólisis despolarizada de ácido clorhídrico acuoso, su precio y su disponibilidad es un gran problema en cuanto a la explotación comercial eficaz. Como es bien conocido por los expertos en la especialidad, el rodio es por ahora el más costoso de los metales nobles, superando su precio incluso el del osmio y siendo un orden de magnitud, por ejemplo, el del rutenio y el iridio; aunque la electrólisis despolarizada de ácido clorhídrico acuoso es una tecnología con una gran demanda de mercado, el precio de los catalizadores del estado de la técnica es por lo tanto demasiado alto para permitir que la comercialización sea satisfactoria.
Entre los metales nobles de precio razonable que podrían ser útiles para la reducción de oxígeno en medio ácido, el rutenio sería aparentemente una elección obvia, siendo su actividad comparable a la del rodio y siendo su precio, de media, aproximadamente veinte veces inferior. RuC>2 preparado mediante precipitación acuosa a partir de RuCh es un catalizador muy conocido; desgraciadamente, su estabilidad química (antes de una estabilización térmica) en medio clorhídrico saturado en cloro es escasa y el catalizador se disuelve en un tiempo relativamente corto. Otros sulfuras parecen seguir la misma suerte a menos que el material se estabilice térmicamente. Hoy por hoy, el sulfuro de rodio preparado a través de preparación acuosa ofrece una buena alternativa (véase la Patente de EE. UU. 6.149.782). El sulfuro de rutenio obtenido de un modo similar resultaba ser poco estable en un ambiente clorhídrico saturado en cloro. El único catalizador similar para la reducción de oxígeno y divulgado en la técnica anterior, el catalizador de tipo fase de Chevrel, a saber MoxRuyS/C, también es inestable a temperatura y concentración de
ácido elevadas (véase J. Chem. Soc., Faraday Trans., 1996, 92, 4311).
OBJETIVOS DE LA INVENCIÓN
Un objetivo de la presente invención es proporcionar un catalizador para la reducción de oxígeno químicamente estable en un ambiente clorhídrico en presencia de cloro disuelto y opcionalmente de oxígeno disuelto que venza las 5 desventajas de la técnica anterior.
Bajo otro aspecto, un objetivo de la presente invención es proporcionar un electrodo de difusión de gas que incorpore un catalizador para la reducción de oxígeno para el uso en pilas de electrólisis de ácido clorhídrico despolarizado.
Bajo un aspecto más, un objetivo de la presente invención es proporcionar un método para producir un catalizador 10 para la reducción de oxígeno químicamente estable en un ambiente clorhídrico en presencia de cloro disuelto y opcionalmente de oxígeno disuelto que venza las desventajas de la técnica anterior, y un método para producir un electrodo de difusión de gas que incorpore el mismo.
Estos y otros objetivos y ventajas de la invención serán obvios a partir de la siguiente descripción detallada. DESCRIPCIÓN DE LA INVENCIÓN
Bajo un primer aspecto, el catalizador de la invención consiste en una forma químicamente estable de sulfuro de rutenio soportado; puesto que el catalizador de la invención se dirige al uso en cátodos de difusión de gas para electrólisis despolarizada de ácido clorhídrico, en la siguiente descripción, por "forma químicamente estable" se entiende una forma químicamente estable en un ambiente de ácido clorhídrico también en presencia de cloro disuelto y opcionalmente de oxígeno disuelto.
Bajo un segundo aspecto, el electrodo de difusión de gas de la invención comprende un tejido conductor, preferiblemente una tela de carbono, revestido con una forma químicamente estable de catalizador de sulfuro de rutenio soportado opcionalmente mezclado con un aglutinante hidrófobo. Bajo un tercer aspecto, el método para producir el catalizador de la invención comprende someter a un soporte conductor a impregnación con humedad incipiente con un precursor de rutenio y opcionalmente de otro metal de transición, secar el soporte Impregnado y 25 tratar el producto resultante bajo una atmósfera que comprende sulfuro de hidrógeno.
Bajo un cuarto aspecto, el método para producir el catalizador de la invención comprende someter a un compuesto de óxido de rutenio soportado, opcionalmente Ru02 soportado en carbono, a una reacción de sulfurización en una atmósfera que comprende sulfuro de hidrógeno.
Bajo un quinto aspecto, el método para producir el electrodo de difusión de gas de la invención comprende revestir 30 un tejido eléctricamente conductor con el catalizador de la invención opcionalmente mezclado con un aglutinante hidrófobo, y opcionalmente sinterizar el tejido revestido.
En una realización preferida, el catalizador de... [Seguir leyendo]
Reivindicaciones:
1. Un catalizador para la reducción de oxigeno que comprende un sulfuro de rutenio y cobalto químicamente estable en un ambiente clorhídrico en presencia de cloro disuelto y opclonalmente de oxígeno disuelto, en el que dicho sulfuro es RuxCoyS soportado sobre negro de carbono.
2. El catalizador según la reivindicación 1, en el que la relación atómica Ru:Co está comprendida entre 0,2 y 5.
3. El catalizador según la reivindicación 2, en el que la relación atómica Ru:Co está comprendida entre 2,8 y 3,2.
4. El catalizador según una cualquiera de las reivindicaciones 1 a 3, en el que dicho negro de carbono tiene una superficie específica que supera 120 m2/g.
5. El catalizador según una cualquiera de las reivindicaciones 1 a 4, obtenido mediante impregnación con humedad incipiente de dicho carbono con sales precursoras de rutenio y de cobalto, evaporando el disolvente y tratando el producto resultante bajo una atmósfera de sulfuro de hidrógeno opcionalmente diluido con un gas portador inerte.
6. El catalizador según la reivindicación 5, en el que dichas sales precursoras comprenden al menos uno de RuCh y Co(N03)2.
7. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicho disolvente comprende 2- propanol.
8. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicha evaporación del disolvente se lleva a cabo bajo vacío a una temperatura por encima de 90°C.
9. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicho tratamiento bajo una atmósfera de sulfuro de hidrógeno se lleva a cabo en un reactor de flujo.
10. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicho tratamiento bajo una atmósfera de sulfuro de hidrógeno se lleva a cabo a una temperatura que supera 100°C, preferiblemente comprendida entre 300 y 500°C.
11. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicho tratamiento bajo una atmósfera de sulfuro de hidrógeno se prolonga durante un tiempo que supera treinta minutos, preferiblemente entre una y cuatro horas.
12. El catalizador según una cualquiera de las reivindicaciones 5 o 6, en el que dicho gas portador inerte es hidrógeno y la relación molar de dicho nitrógeno a dicho sulfuro de hidrógeno está comprendida entre 0,5 y 4.
13. Un electrodo de difusión de gas que comprende un tejido conductor, en el que el catalizador según cualquiera de las reivindicaciones precedentes se aplica sobre al menos una cara de dicho tejido conductor.
14. El electrodo de difusión de gas según la reivindicación 13, en el que dicho tejido conductor es una tela de carbono.
15. El electrodo de difusión de gas según la reivindicación 13, en el que dicho catalizador se mezcla con un aglutinante hidrófobo opcionalmente perfluorado.
Patentes similares o relacionadas:
Celda electrolítica para la producción de soluciones oxidantes, del 17 de Junio de 2020, de INDUSTRIE DE NORA S.P.A: Celda electrolítica para la producción de soluciones oxidantes, que comprende un compartimento anódico que contiene un ánodo […]
Método para producir un electrodo de difusión de gas, del 13 de Mayo de 2020, de INDUSTRIE DE NORA S.P.A: Un método para producir un electrodo de difusión de gas, comprendiendo dicho método las etapas de: revestir un tejido conductor sobre al menos un lado del mismo con un catalizador […]
Aparato de electrocloración, del 6 de Mayo de 2020, de Gaffey Technical Services Limited: Un aparato de electrocloración para generar una solución de hipoclorito de sodio que comprende una celda electrolítica ; un depósito de salmuera situado […]
 Electrodo, del 28 de Agosto de 2019, de Nouryon Chemicals International B.V: Un electrodo que comprende:
- un sustrato de electrodo de titanio ,
- una capa de TiOx con un grosor total en el intervalo de entre 40 - 200 μm […]
Electrodo, del 28 de Agosto de 2019, de Nouryon Chemicals International B.V: Un electrodo que comprende:
- un sustrato de electrodo de titanio ,
- una capa de TiOx con un grosor total en el intervalo de entre 40 - 200 μm […]
 Procedimientos de preparación de carbonato de litio altamente puro y de otros compuestos que contienen litio altamente puro, del 31 de Julio de 2019, de All American Lithium LLC: Un procedimiento de producción de un compuesto que contiene litio, que comprende las etapas de:
poner en contacto una salmuera acuosa que contiene […]
Procedimientos de preparación de carbonato de litio altamente puro y de otros compuestos que contienen litio altamente puro, del 31 de Julio de 2019, de All American Lithium LLC: Un procedimiento de producción de un compuesto que contiene litio, que comprende las etapas de:
poner en contacto una salmuera acuosa que contiene […]
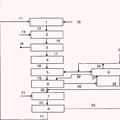 Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Procedimiento para la producción de electrodos de grafito para procesos electrolíticos, del 15 de Mayo de 2019, de Covestro Deutschland AG: Procedimiento para la producción de electrodos de grafito con un revestimiento predominantemente de metal noble para la electrólisis de ácido clorhídrico, en el que el electrodo […]
Revestimiento catalítico y método de fabricación del mismo, del 13 de Mayo de 2019, de INDUSTRIE DE NORA S.P.A: Sustrato de metal de de válvula revestida que tiene un revestimiento que comprende una primera capa catalítica que no contiene titanio y que consiste en una fase amorfa […]