Biotejido de colágeno y métodos de preparación y uso del mismo.
Un método para preparar un laminado de membrana amniótica a partir de una placenta que tiene una membrana amniótica y una membrana coriónica que comprende:
(a) separar la membrana amniótica de la membrana coriónica;
(b) descelularizar la membrana amniótica; y
(c) formar capas de al menos dos de las membranas amnióticas descelularizadas en contacto entre sí de modo que se forma un laminado de membrana amniótica,
en el que la descelularización de la membrana amniótica no forma congelación en ningún punto en la preparación de la membrana amniótica o en la puesta en contacto de la membrana con una proteasa.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/009304.
Solicitante: ANTHROGENESIS CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 7 Powder Horn Drive Warren NJ 07059 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HARIRI,ROBERT J, KAPLUNOVSKY,ALEKSANDR M, MURPHY,PATRICIA A.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/50 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Placenta; Células madre de la placenta; Fluido amniótico; Amnios; Células madre del líquido amniótico.
- A61L27/36 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › que contienen ingredientes de composición indeterminada o sus productos de reacción.
- C12N5/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00).
PDF original: ES-2526088_T3.pdf
Fragmento de la descripción:
Biotejido de colágeno y métodos de preparación y uso del mismo
1. Campo de la invención
La presente invención se refiere a un método para preparar un laminado de membrana amniótica a partir de una placenta que tiene una membrana amniótica y una membrana coriónica. La presente invención también se refiere a un laminado de membrana amniótica, que se puede obtener con el método de la presente invención.
La presente invención comprende membranas de colágeno producidas a partir del amnios, denominado en el presente documento biotejido de colágeno. El biotejido de colágeno comprendido en la invención tiene la integridad estructural de la membrana amniótica sin tratar nativa, es decir, la estructura terciaria y cuaternaria nativa. La presente divulgación proporciona un método para preparar un biotejido de colágeno a partir de membrana de placenta, preferentemente una membrana de placenta humana que tiene una membrana coriónica y amniótica, por descelularización de la membrana amniótica. En una realización precedente, la membrana amniótica está completamente descelularizada. El biotejido de colágeno comprendido en la invención tiene numerosos usos en el campo médico y quirúrgico incluyendo, por ejemplo, reparación de vasos sanguíneos, construcción y sustitución de un vaso sanguíneo, sustitución de tendones y ligamentos, vendaje de heridas, injertos quirúrgicos, usos oftálmico, suturas y otros. Los beneficios del biotejido se deben, en parte, a sus propiedades físicas tales como resistencia biomecánica, flexibilidad, capacidad de sutura, y baja inmunogenicidad, particularmente cuando se deriva de placenta humana.
2. Antecedentes de la invención
2.1 MEMBRANA AMNIÓTICA: ANATOMÍA E HISTOLOGÍA
El saco placentario está formado por dos capas conectadas estrechamente mediante tejido conjuntivo flexible. Se conocen como las capas amniótica y coriónica (Véase la FIGURA 1). La capa amniótica es la más interna de las dos capas y entra en contacto con el fluido amniótico que rodea al feto y en conjunto forman el saco amniótico. La capa amniótica es avascular y está revestida con epitelio columnar sencillo que recubre una membrana basal y tiene un espesor de 3-6 micrómetros. La membrana coriónica es la capa más externa del saco y está muy celularizada. El árbol vascular se origina en la placenta y se extiende a las membranas de la placenta a través de la capa coriónica. La capa coriónica se separa de la capa amniótica mediante tejido colector flexible y combinadas, las dos capas miden 12-18 micrómetros. Las membranas de la placenta tienen una matriz de colágeno que está muy cargada de mucopolisacáridos y se cree que sirven principalmente como un saco protector para el feto en desarrollo. Las membranas también mantienen una barrera para agentes infecciosos e inmunológicos presentes en la circulación materna. Las membranas de la placenta tienen medios de transporte tanto activos como pasivos. La mayoría de las moléculas pequeñas y proteínas pueden viajar libremente a través de ellos, pero las proteínas grandes como IgM no pueden cruzar a través de la capa basal.
La conservación de las membranas de la placenta (que son de fuentes animales o humanas) en alcohol etílico al 95 % o glicerol mezclados en proporciones de un 5-5 % con medios de cultivo tisular se ha usado para la conservación de la membrana amniótica antes de su congelación. Estos conservantes eliminan la vitalidad de los tejidos de placenta haciendo los núcleos piknóticos pero la matriz de colágeno y las membranas básales se conservan. De forma interesante, ambas formas de conservación también eliminan la antigenicidad de las membranas trasplantadas y también cualquier agente potencialmente virulento. La conservación nuevamente se consigue después de que las membranas amnióticas se separen cuidadosamente del corión. El lado de la membrana amniótica con la lámina y epitelio básales es brillante y el lado opuesto frente al corión no tiene brillo.
2.2 APLICACIONES CLÍNICAS PREVIAS DE MEMBRANAS AMNIÓTICAS
Los posibles problemas potenciales con tejidos xenogénicos (tejidos de otras especies) que transportan enfermedades zoonóticas o que causan rechazo entre especies han hecho estos tejidos menos deseables. Los injertos alogénicos, o injertos de diferentes individuos de la misma especie, siguen siendo la fuente preferente de materiales para injerto en seres humanos. La escasez de tejidos de donantes humanos para injerto es un problema creciente que ha estimulado el desarrollo de nuevos materiales para injerto de tejido. Muy a menudo estas fuentes de material biológico de partida son escasas, difíciles de obtener, y con un coste muy elevado. Sin embargo, la lámina de colágeno de amnios humano tiene características biomecánicas deseables útiles en aplicaciones de injerto de tejido. Por lo tanto, las membranas amnióticas son una buena fuente de material de injerto alogénico.
La membrana fetal que incluye la membrana amniótica y coriónica se ha usado en cirugías documentadas ya en 191 y ha sido revisada por Trelford y Trelford-Sauder en 1979 (Véase Trelford y Trelford-Sauder, 1979, Am. J. Obstet. Gynecol. 833). En 191, Davis fue el primero en informar del uso de membranas fetales como un material quirúrgico en transplante de piel, por ejemplo en pieles quemadas y ulceradas (Davis et al., 191, Johns Hopkins Med. J.; 15: 37). Estos estudios se realizaron principalmente en animales y los ensayos en seres humanos fueron decepcionantes. Desde entonces, se ha desarrollado el uso de membranas amnióticas en cirugía (Véase, por ejemplo, Stem etai, 1913, JAMA, 13: 973-4; Sabella et al., 1913 Med. Records NY, 83: 478-8; de Rotth et al., 194
Arch. Opthalmol, 23: 522-5; Sorsby et al., 1946, Br. J. Opthamlol. 3: 337-45). En la actualidad se usa como un apósito biológico para piel quemada, heridas en la piel, y úlceras crónicas en las piernas, como un tejido adyuvante en la reconstrucción quirúrgica de vagina artificial, y para la reparación de onfaloceles (Véase por ejemplo, Trelford y Trelford-Sauder, 1979, 134 Am. J. Obstet. Gynecol. 833; Colocho et al., 1974 Arch. Surg. 19: 37-3; Faulk et al. 198 Lancef, 1156; Prasad et al., 1986, J. Trauma, 26: 945-6; Subrahmanyan et al., 1995, J. Plástic Surg. 48: 477-8; Gruss et al., 1978, J. Can. Med. Assoc. 118: 1237-46; Ward et al., 1984, Br. J. Plástic Surg. 37: 191-3; Dhall, 1984, J. Obstet. Gynaecol. 91: 279-82). También sea usado para prevenir la adherencia de tejido en procedimientos quirúrgicos del abdomen, cabeza y pelvis (Gharib etal., 1996, Pediatr. Surg. Int. 11: 96-9; Rennekampff et al., 1994, Invest. Surg. 7: 187-93). En la década de 194, varios autores informaron del papel beneficioso de la membrana amniótica en el tratamiento de una diversidad de trastornos de la superficie ocular (Véase por ejemplo, de Rotth et al., 194 Arch. Opthalmol, 23: 522-5; Sorsby et al., 1946, Br. J. Opthalmol. 3: 337-45; Lavery et al., 1946, Trans. Opthalmol. Soc. UK, 66: 668).
Anteriormente se han descrito numerosos intentos en el campo para optimizar la preparación y conservación de las membranas amnióticas para uso en trasplante (véase por ejemplo, Dua et al., 1999, Br. J. Opthalmol 83: 748-52 ("Dua") para una revisión). Diversas preparaciones de membranas amnióticas han incluido conservación con mezclas de solución salina y antibiótico, deshidratación con alcohol con o sin separación de la capa amniótica de la capa coriónica. Sin embargo, todos los métodos que se describen en Dua, y en las referencias que se han descrito anteriormente aún presentan deficiencias que es necesario abordar mediante mejoras en la preparación y conservación de las membranas amnióticas.
Más recientemente, se han desvelado métodos que dependen de la congelación para la conservación de la membrana amniótica para su aplicación en procedimientos quirúrgicos de injerto de tejido para corregir defectos epiteliales de la córnea. Véanse por ejemplo, las Patentes de Estados Unidos N° 6.152.142 y N° 6.326.19B1 ("Tseng"). Tseng desvela una membrana amniótica que está montada sobre un sustrato y se conserva en una mezcla de Medio de Eagle modificado con Dulbecco y glicerol y se congela a -8 °C. El proceso de congelación del tejido en cualquier momento durante su preparación hace que la membrana amniótica de Tseng sea frágil, e incluso más frágil después de las etapas de descongelación y activación. Además, las etapas de descongelación y activación añaden tiempo necesario para la manipulación de la membrana amniótica. Además, debido a la fragilidad de la membrana amniótica de Tseng causada por la etapa de congelación en el proceso de conservación y preparación, se requiere un soporte o apoyo estructural para garantizar la... [Seguir leyendo]
Reivindicaciones:
1. Un método para preparar un laminado de membrana amniótica a partir de una placenta que tiene una membrana amniótica y una membrana coriónica que comprende:
(a) separar la membrana amniótica de la membrana coriónica;
(b) descelularizar la membrana amniótica; y
(c) formar capas de al menos dos de las membranas amnióticas descelularizadas en contacto entre sí de modo que se forma un laminado de membrana amniótica,
en el que la descelularlzaclón de la membrana amniótica no forma congelación en ningún punto en la preparación de la membrana amniótica o en la puesta en contacto de la membrana con una proteasa.
2. El método de la reivindicación 1, que comprende adiclonalmente lavar la membrana amniótica descelularlzada al menos una vez después de la etapa (b) y antes de la etapa (c).
3. El método de la reivindicación 1, que comprende adicionalmente secar el laminado de membrana amniótica descelularizada.
4. El método de la reivindicación 1, que comprende adicionalmente ensamblar al menos dos de dichos laminados de membrana amniótica en un armazón tridimensional complejo.
5. Un laminado de membrana amniótica que comprende al menos dos capas de una membrana amniótica deshidratada, descelularizada y libre de sustrato, en el que dicha membrana amniótica tiene una estructura terciaria y cuaternaria nativa.
6. El laminado de membrana amniótica de la reivindicación 5, en el que la membrana amniótica comprende colágeno, elastina, y fibronectina.
7. El laminado de membrana amniótica de la reivindicación 5, que comprende adiclonalmente una o más composiciones de hidrogel.
8. El laminado de membrana amniótica de la reivindicación 7, en el que la composición de hidrogel comprende un polímero seleccionado entre el grupo que consiste en alcohol de polivinilo, polietilenglicol, ácido hialurónico, dextrano, y derivados o análogos de los mismos.
9. El laminado de membrana amniótica de cualquiera de las reivindicaciones 5-8, en el que se da forma al laminado en una lámina, tubo o microesfera.
Patentes similares o relacionadas:
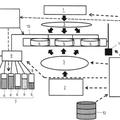 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Composiciones mejoradas para hidrogeles, del 22 de Julio de 2020, de Biogelx Limited: Una composición de hidrogel, que comprende una mezcla de los derivados peptídicos primero y segundo en una proporción de 1:4 a 4:1, en donde los primeros derivados […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Producción de tapsigarginas por cultivo en suspensión de células de Thapsia, del 6 de Mayo de 2020, de PHYTON HOLDINGS, LLC: Método de producción de lactonas sesquiterpénicas de la familia de tapsigargina, comprendiendo el método las etapas de: (a) cultivar células vegetales […]
Composición de medio para preparar toxina botulínica, del 6 de Mayo de 2020, de Daewoong Co., Ltd: Una composición de medio libre de EET para su uso en el cultivo de Clostridium botulinum, la composición de medio comprende: peptonas de origen […]
Células virales resistentes y sus usos, del 22 de Abril de 2020, de Sigma-Aldrich Co. LLC: Una línea celular de ovario de hámster chino (CHO) modificada genéticamente en la que la entrada y/o propagación del virus diminuto del ratón (MVM) […]
Composiciones de cultivo de células con antioxidantes y procedimientos para la producción de polipéptidos, del 15 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento de producción de un anticuerpo o un fragmento del mismo producido recombinantemente que comprende la etapa de cultivar una célula que comprende […]