AVES TRANSGÉNICAS Y PRODUCCIÓN DE PROTEÍNA.
Un ave transgénica que porta un vector retroviral en el material genético de su tejido de línea germinar,
en el que el vector comprende un gen exógeno y un promotor constitutivo, en relación operacional y posicional para expresar el gen exógeno, y el gen exógeno se expresa en el oviducto aviar del ave transgénica para producir una proteína exógena en la que la proteína exógena contiene una secuencia señal y se secreta en el lumen del oviducto de modo que la proteína se deposite en la clara de un huevo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1998/021975.
Solicitante: UNIVERSITY OF GEORGIA RESEARCH FOUNDATION, INC.
SYNAGEVA BIOPHARMA CORP.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 623 BOYD GRADUATE STUDIES RESEARCH CENTER ATHENS, GA 30602-7411 ESTADOS UNIDOS DE AMERICA.
Inventor/es: RAPP, JEFFREY, C., IVARIE,Robert,D, HARVEY,Alex,J, MORRIS,Julie,A, LIU,Guodong.
Fecha de Publicación: .
Fecha Solicitud PCT: 15 de Octubre de 1998.
Clasificación Internacional de Patentes:
- C12N15/85A1
- C12N15/85A1B
- C12N15/90B
Clasificación PCT:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- C12N15/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N15/90 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Introducción estable de ADN extraño en el cromosoma.
Clasificación antigua:
- A01K67/027 A01K 67/00 […] › Nuevas razas de vertebrados.
- C12N15/00 C12N […] › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N15/90 C12N 15/00 […] › Introducción estable de ADN extraño en el cromosoma.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2357495_T3.pdf
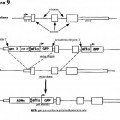

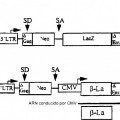

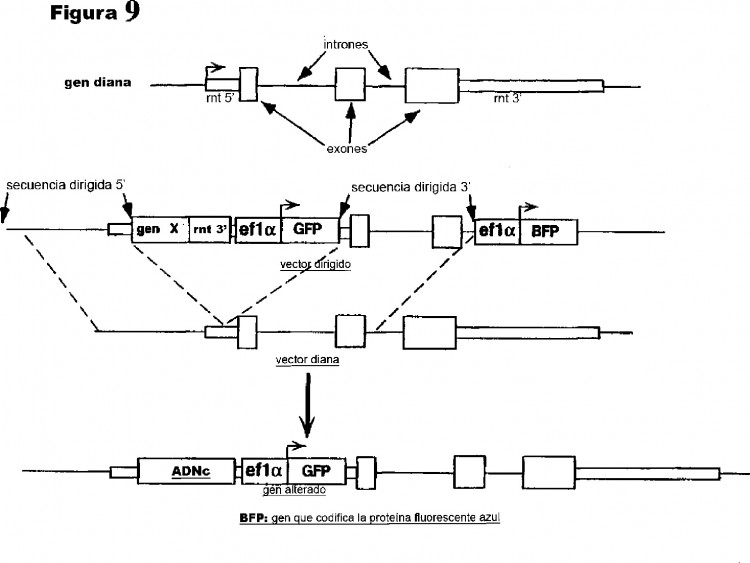
Fragmento de la descripción:
Aves transgénicas y producción de proteína.
Antecedentes de la invención
La presente invención se refiere a procedimientos para la introducción de material genético exógeno en células aviares y la expresión del material genético exógeno en las células. La invención también se refiere a especies aviares transgénicas, que incluyen pollos, que producen huevos aviares que contienen proteína exógena.
Se usan numerosas proteínas naturales y sintéticas en aplicaciones diagnósticas y terapéuticas; muchas otras están en desarrollo o en ensayos clínicos. Los procedimientos actuales de producción de proteínas incluyen el aislamiento a partir de fuentes naturales y la producción recombinante en células bacterianas y de mamíferos. Sin embargo, debido a la complejidad y al alto coste de estos procedimientos de producción de proteínas, se están realizando esfuerzos para desarrollar alternativas. Por ejemplo, se han notificado procedimientos para producir proteínas exógenas en la leche de cerdos, ovejas, cabras y vacas. Estas aproximaciones se ven afectadas por varias limitaciones, incluyendo tiempos de generación largos entre rebaños fundadores y de producción transgénica, ganadería extensiva y costes veterinarios, y niveles variables de expresión debido a los efectos de posición en el sitio de la inserción transgén en el genoma. Las proteínas también se producen usando procedimientos de molienda y malteado a partir de cebada y centeno. Sin embargo, las modificaciones postraduccionales de las plantas se diferencian de las modificaciones postraduccionales de los vertebrados, lo que a menudo tiene un efecto crítico en la función de las proteínas exógenas.
Al igual que un biorreactor de cultivo de tejido y de glándula mamaria, el oviducto aviar también puede servir potencialmente como un biorreactor. Los procedimientos exitosos de modificación del material genético aviar son tales que se secretan altos niveles de proteínas exógenas en y se empaquetan dentro de huevos permitirían la producción económica de grandes cantidades de proteína. Diversas ventajas de una aproximación de este tipo serían: a) tiempos de generación cortos (24 semanas) y establecimiento rápido de bandadas transgénicas por medio de inseminación artificial; b) producción fácilmente a escala incrementando los tamaños de bandadas para cumplir con las necesidades de producción; c) modificación postraduccional de proteínas expresadas; 4) alimentación automatizada y recogida de huevos; d) claras de huevo estériles de manera natural y e) costes de procesamiento reducidos debido a la concentración alta de proteína en la clara de huevo.
El sistema reproductivo aviar, que incluye el del pollo, se ha descrito bien. El huevo de la gallina consta de diversas capas que se secretan sobre la yema durante su paso a través del oviducto. La producción de un huevo comienza con la formación de la yema grande en el ovario de la gallina. Entonces, el ovocito no fertilizado se posiciona sobre el saco vitelino. Tras la ovulación o la liberación de la yema desde el ovario, el ovocito pasa a través del infundíbulo del oviducto, en el que se fertiliza si está presente el esperma. Entonces, se mueve dentro del magno del oviducto que está recubierto con células de glándulas tubulares. Estas células secretan las proteínas de la clara de huevo, que incluyen ovoalbúmina, lisozima, ovomucoide, conalbúmina y ovomucina, dentro del lumen del magno donde se depositan sobre el embrión aviar y la yema.
El gen de ovoalbúmina codifica una proteína de 45 kD se expresa de manera específica en las células de glándulas tubulares del magno del oviducto (Beato, Cell 56:335-344 (1989)). La ovoalbúmina es la proteína de la clara de huevo más abundante, que comprende más del 50 por ciento de la proteína total producida por las células de glándulas tubulares, o aproximadamente 4 gramos de proteína por huevo de categoría A grande (Gilbert, "Egg albumen and its formation" en Physiology and Biochemistry of the Domestic Fowl, Bell y Freeman, eds., Academic Press, Londres, Nueva York, pág. 1291-1329). Se han clonado el gen de ovoalbúmina y más de 20 kb de cada región flanqueante y se han analizado (Lai et al., Proc. Natl. Acad. Sci. EE.UU. 75:2205-2209 (1978); Gannon et al., Nature 278:428-424 (1979); Roop et al., Cell 19:63-68 (1980); y Royal et al., Nature 279:125-132 (1975)).
Se ha prestado mucha atención a la regulación del gen de ovoalbúmina. El gen responde a hormonas esteroideas tales como estrógeno, glucocorticoides y progesterona, que inducen la acumulación de aproximadamente 70.000 tránscritos de ARNm de ovoalbúmina por célula de glándulas tubulares en polluelos inmaduros y 100.000 tránscritos de ARNm de ovoalbúmina por célula de glándulas tubulares en la gallina ponedora madura (Palmiter; J. Biol. Chem. 248:8260-8270 (1973); Palmiter, Cell 4:189-197 (1975)). El análisis de hipersensibilidad de ADNsa y los ensayos de gen promotor-indicador en células de glándulas tubulares transfectadas definieron una región de 7,4 kb que contenía secuencias requeridas para la expresión del gen de la ovoalbúmina. Esta región 5' flanqueante contiene cuatro sitios de hipersensibilidad 1 de ADNsa centrados en -0,25, -0,8, -3,2 y -6,0 kb desde el sitio de comienzo de transcripción. Estos sitios se denominan HS-I, -II, -III y -IV, respectivamente. Estas regiones reflejan alteraciones en la estructura de la cromatina y están correlacionadas de manera específica con la expresión del gen de la ovoalbúmina en células del oviducto (Kaye et al., EMBO 3:1137-1144 (1984)). La hipersensibilidad de HS-II y de -III está inducida por estrógeno, apoyando la función de estas regiones en la inducción de hormonas de la expresión del gen de la ovoalbúmina.
Se requieren tanto HS-I como HS-II para la inducción esteroidea de la transcripción del gen de la ovoalbúmina, y es suficiente una porción de 1,4 kb de la región 5' que incluya estos elementos para conducir la expresión de la ovoalbúmina dependiente de esteroides en células de glándulas tubulares explantadas (Sanders y McKnight, Biochemistry 27: 6550-6557 (1988)). HS-I se denomina como el elemento de respuesta negativa ("ERN") ya que contiene diversos elementos reguladores negativos que reprimen la expresión de la ovoalbúmina en ausencia de hormona (Haekers et al., Mol. Endo. 9:1113-1126 (1995)). Los factores de la proteína unen estos elementos, que incluyen algunos factores que sólo se encuentran en el núcleo del oviducto lo que sugiere un papel en la expresión específica de tejido. HS-II se denomina como el elemento de respuesta dependiente de esteroides ("ERDE") ya que se requiere para promover la inducción esteroidea de la transcripción. Se une a una proteína o complejo de proteínas conocido como Chirp-I. Chirp-I se induce mediante estrógenos y rota rápidamente en presencia de ciclohexamida (Dean et al., Mol. Cell. Biol. 16:2015-2024 (1996)). Los experimentos que usan un sistema de cultivo de células de glándulas tubulares definieron un juego de factores adicionales que unen ERDE de manera dependiente de esteroides, incluyendo un factor similar a NFκB (Nordstrom et al., J. Biol. Chem. 268:13193-13202 (1993); Schweers y Sanders, J. Biol. Chem. 266: 10490-10497 (1991)).
Se conoce menos sobre la función de HS-III y de -IV. HS-III contiene un elemento funcional de respuesta a estrógenos y confiere inducibilidad por estrógenos al promotor proximal a ovoalbúmina o bien al promotor heterólogo al co-transfectarse en células HeLa con un ADNc receptor de estrógeno. Estos datos implican que HS-III puede jugar un papel funcional en la regulación general del gen de la ovoalbúmina. Se conoce poco sobre la función de HS-IV, excepto que no contiene un elemento funcional de respuesta a estrógenos (Kato et al., Cell 68: 731-742 (1992)).
Se ha mostrado mucho interés por la modificación de genomas eucariotas introduciendo material genético extraño y/o alterando genes específicos. Se puede probar que ciertas células eucariotas son huéspedes superiores para la producción de proteínas eucariotas exógenas. La introducción de genes que codifican ciertas proteínas también permite la creación de nuevos fenotipos que pueden incrementar el valor económico. Además, se pueden curar algunos estados de enfermedad... [Seguir leyendo]
Reivindicaciones:
1. Un ave transgénica que porta un vector retroviral en el material genético de su tejido de línea germinar, en el que el vector comprende un gen exógeno y un promotor constitutivo, en relación operacional y posicional para expresar el gen exógeno, y el gen exógeno se expresa en el oviducto aviar del ave transgénica para producir una proteína exógena en la que la proteína exógena contiene una secuencia señal y se secreta en el lumen del oviducto de modo que la proteína se deposite en la clara de un huevo.
2. Un procedimiento para producir una proteína exógena en un oviducto aviar, que comprende:
proporcionar un vector retroviral que comprende una secuencia de codificación y un promotor constitutivo unido de manera operable a la secuencia de codificación, en el que el promotor puede efectuar la expresión de la secuencia de codificación en las células de glándulas tubulares de un oviducto aviar;
crear células transgénicas introduciendo el vector en células blastodérmicas embrionarias, en el que la secuencia del vector se inserta en el genoma aviar y en el que la introducción del vector en las células blastodérmicas embrionarias está mediada por retrovirus; y
derivar un ave transgénica madura a partir de células transgénicas, en el que las células de glándulas tubulares del ave transgénica expresan la proteína, y la proteína resultante se secreta en el lumen del oviducto, de modo que la proteína se deposita en la clara de huevo de un huevo.
3. Un procedimiento para producir un huevo aviar que contenga proteína exógena, que comprende:
proporcionar un vector retroviral que comprende una secuencia de codificación y un promotor constitutivo unido de manera operable a la secuencia de codificación, en el que el promotor puede efectuar la expresión de la secuencia de codificación en las células de glándulas tubulares de un oviducto aviar;
crear células transgénicas introduciendo el vector en células blastodérmicas embrionarias, en el que la secuencia del vector se inserta en el ave y en el que la introducción del vector en las células blastodérmicas embrionarias está mediada por retrovirus; y
derivar un ave transgénica madura a partir de células transgénicas, en el que las células de glándulas tubulares del ave transgénica expresan la secuencia de codificación, y la proteína resultante se secreta en el lumen del oviducto, de modo que la proteína se deposita en la clara de huevo de un huevo.
4. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 3, que comprende además la cría a partir de esta ave transgénica madura para producir crías, en el que las células de glándulas tubulares del ave transgénica de cría expresan la secuencia de codificación, y la proteína resultante se secreta en el lumen del oviducto, de modo que la proteína se deposita en la clara de huevo de un huevo.
5. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 4, que comprende además la etapa de aislar la proteína del huevo.
6. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 5, en el que la etapa de introducir el vector en las células blastodérmicas embrionarias incluye administrar células auxiliares a un blastodermo embrionario, en el que las células auxiliares producen el retrovirus.
7. El ave transgénica de la reivindicación 1 o el procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 6, en el que el promotor se selecciona del grupo que consta del promotor del CMV, el promotor del SV40 y el promotor del virus del sarcoma de Rous (RSV).
8. El ave transgénica de la reivindicación 1 o el procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 7, en el que la proteína exógena en una proteína farmacéutica.
9. El procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 8, en el que el procedimiento comprende además formular la proteína como un medicamento.
10. El ave transgénica de la reivindicación 1 o el procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 9, en el que la proteína exógena se selecciona del grupo que consta de interferón, α-1 antitripsina, antitrombina III, colágeno, factores VIII, IX, X, fibrinógeno, insulina, lactoferrina, proteína C, activador de plasminógeno de tipo de tejido, somatotropina, anticuerpo, hormona de crecimiento humano, inmunotoxina, quimotripsina, factor de estimulación de colonias de granulocitos macrófagos , factor de estimulación de colonias de granulocitos y eritropoyetina.
11. El ave transgénica de la reivindicación 1 o el procedimiento de acuerdo con una cualquiera de las reivindicaciones 2 a 10, en el que el ave transgénica se selecciona del grupo que consta de un pollo o un pavo.
Patentes similares o relacionadas:
MUTANTES FÚNGICOS FILAMENTOSOS CON EFICIENCIA MEJORADA DE RECOMBINACIÓN HOMÓLOGA, del 17 de Enero de 2011, de DSM IP ASSETS B.V.: Método para aumentar la eficiencia de integración direccionada de un polinucleótido en un sitio predeterminado del genoma de una célula fúngica […]
NUEVO METODO DE CLONACION DE DNA BASADO EN EL SISTEMA DE RECOMBINACION RECE-RECT DE E. COLI, del 20 de Abril de 2010, de EUROPIISCHES LABORATORIUM FIR MOLEKULARBIOLOGIE (EMBL): Un método para la clonación de moléculas de DNA en células, que comprende los pasos de (a) proporcionar una célula huésped aislada capaz de realizar la recombinación homóloga […]
RECOMBINACION DE ADN ESPECIFICO DE SECUENCIA EN CELULAS EUCARIOTAS, del 12 de Marzo de 2010, de DROGE, PETER: Procedimiento para la recombinación específica de secuencia de ADN en una célula eucariota in vitro que comprende a) la introducción en una célula […]
ANIMALES TRANSGENICOS NO HUMANOS CAPACES DE PRODUCIR ANTICUERPOS HETEROLOGOS, del 27 de Septiembre de 2010, de GENPHARM INTERNATIONAL, INC.: LA INVENCION TRATA DE ANIMALES NO HUMANOS TRANSGENICOS CAPACES DE PRODUCIR ANTICUERPOS HETEROLOGOS Y PROCEDIMIENTOS PARA PRODUCIR ANTICUERPOS DE SECUENCIA HUMANA QUE SE […]
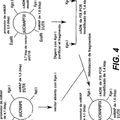 EXPRESION DEL FACTOR IX HUMANO ACTIVO EN TEJIDO MAMARIO DE ANIMALES TRANSGENICOS, del 27 de Mayo de 2010, de AMERICAN RED CROSS: Un mamífero transgénico no humano que contiene una molécula de ADN exógena establemente integrada en su genoma, en el que dicha molécula de ADN exógena comprende: (a) […]
EXPRESION DEL FACTOR IX HUMANO ACTIVO EN TEJIDO MAMARIO DE ANIMALES TRANSGENICOS, del 27 de Mayo de 2010, de AMERICAN RED CROSS: Un mamífero transgénico no humano que contiene una molécula de ADN exógena establemente integrada en su genoma, en el que dicha molécula de ADN exógena comprende: (a) […]
SECUENCIAS DE DNA USADAS EN LA PRODUCCION DE BSSL/CEL HUMANAS RECOMBINATES EN MAMIFEROS TRANSGENICOS NO HUMANOS Y EL USO DE LA BSSL/CEL PRODUCIDA EN FORMULAS INFANTILES, del 30 de Marzo de 2010, de ASTRA AKTIEBOLAG: LA PRESENTE INVENCION ES RELATIVA A UNA MOLECULA DE DNA QUE CONTIENE SECUENCIAS INTRON Y QUE CODIFICA UNA PROTEINA HUMANA QUE ES, DEPENDIENDO DEL PUNTO DE ACCION, DENOMINADA […]
MAMIFERO NO HUMANO TRANSGENICO PARA LA REGION CONSTANTE DE LA CADENA PESADA DE LAS INMUNOGLOBULINAS HUMANAS DE CLASE A Y SUS APLICACIONES, del 18 de Marzo de 2010, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS) UNIVERSITE DE LIMOGES: Mamífero no humano transgénico, caracterizado por que comprende un locus IgH modificado mediante sustitución de la secuencia de conmutación Sµ por […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]