APARATO DE DIALISIS PARA DETERMINAR LA CONCENTRACION DE IONES EN LA SANGRE.
Aparato de diálisis con un hemodializador y/o un hemofiltro, así como con un circuito sanguíneo extracorporal,
al cual están conectados los medios para la adición de citrato a la sangre, corriente arriba del hemodializador y/o hemofiltro, caracterizado por un conducto de producto dializado que presenta medios para la detección de una concentración de iones en el producto dializado, corriente abajo del hemodializador y/o hemofiltro respecto de la dirección de flujo del producto dializado, así como medios para la adición de una solución sustituta a la sangre que contiene iones, que pueden ser puestos en contacto, corriente abajo del hemodializador y/o hemofiltro, con el circuito sanguíneo extracorporal
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E01129707.
Solicitante: FRESENIUS MEDICAL CARE DEUTSCHLAND GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ELSE-KRINER-STRASSE 1,61352 BAD HOMBURG V.D.H.
Inventor/es: KRAMER, MATTHIAS, DR., NIER,VOLKER,DR.
Fecha de Publicación: .
Fecha Solicitud PCT: 13 de Diciembre de 2001.
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación Internacional de Patentes:
- A61M1/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61M DISPOSITIVOS PARA INTRODUCIR AGENTES EN EL CUERPO O PARA DEPOSITARLOS SOBRE EL MISMO (introducción de remedios en o sobre el cuerpo de animales A61D 7/00; medios para la inserción de tampones A61F 13/26; dispositivos para la administración vía oral de alimentos o medicinas A61J; recipientes para la recogida, almacenamiento o administración de sangre o de fluidos médicos A61J 1/05 ); DISPOSITIVOS PARA HACER CIRCULAR LOS AGENTES POR EL CUERPO O PARA SU EXTRACCION (cirugía A61B; aspectos químicos de los artículos quirúrgicos A61L; magnetoterapia utilizando elementos magnéticos colocados dentro del cuerpo A61N 2/10 ); DISPOSITIVOS PARA INDUCIR UN ESTADO DE SUEÑO O LETARGIA O PARA PONERLE FIN. › A61M 1/00 Dispositivos de succión o de bombeo de uso médico; Dispositivos para extraer, tratar o transportar los líquidos del cuerpo; Sistemas de drenaje (catéteres A61M 25/00; conectores o acoplamientos para tubos, válvulas o conjuntos de derivación, especialmente concebidos para uso médico A61M 39/00; dispositivos para tomar muestras sanguíneas A61B 5/15; instrumentos para retirar la saliva para dentistas A61C 17/06; filtros para implantar en los vasos sanguíneos A61F 2/01). › con membranas.
- G01N33/84 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen compuestos inorgánicos o el pH.
Clasificación PCT:
- A61M1/14 A61M 1/00 […] › Sistemas de diálisis; Riñones artificiales; Oxigenadores de la sangre (membranas semipermeables caracterizadas por sus materiales, sus procedimientos de fabricación B01D 71/00).
- A61M1/16 A61M 1/00 […] › con membranas.
- G01N33/84 G01N 33/00 […] › en los que intervienen compuestos inorgánicos o el pH.
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Aparato de diálisis para determinar la concentración de iones en la sangre.
La presente invención comprende un aparato de diálisis con un hemodializador y/o un hemofiltro, así como con un circuito sanguíneo extracorporal al cual están conectados los medios para la adición de citrato a la sangre, corriente arriba del hemodializador y/o un hemofiltro.
Numerosos iones, átomos y moléculas no se encuentran aislados, sino en forma de los más diversos complejos. Esto comprende tanto los iones, átomos y moléculas en el circuito sanguíneo de un paciente como así también en la sangre extraída al paciente, a los fines de determinado tratamiento de la sangre o del paciente, y que se mezcla fuera del cuerpo con los complejizantes adecuados.
Un ejemplo de la complejización de iones es la denominada hemodiálisis/hemofiltración anticoagulada con citrato. En este caso se lleva a cabo una complejización de iones de Ca++ de la sangre en el circuito sanguíneo extracorporal mediante citrato para inhibir la coagulación de la sangre durante el tratamiento, sobre todo, durante el contacto de la sangre con la membrana en el dializador.
En la mayoría de los pacientes de hemodiálisis es necesaria la inhibición de la coagulación de la sangre. El método estándar es la utilización de heparina infraccionada, infundida mediante una bomba de inyección en la rama arterial del sistema de mangueras extracorporal. La utilización tanto de heparina infraccionada como así también de anticoagulantes alternativos, como heparina de bajo peso molecular o hirudina es problemática, por una parte, para los pacientes, y por otra, también para otras terapias extracorporales, por los siguientes motivos:
La anticoagulación actúa sistémicamente (es decir, no sólo en el contacto con la membrana en el circuito extracorporal, sino en todo el cuerpo), lo cual provoca un peligro de hemorragia crítica para algunos pacientes. Sobre todo en el sector de la medicina intensiva un 30-40% de los pacientes corren peligro de hemorragia.
Algunos pacientes presentan reacciones de incompatibilidad, por ejemplo, la trombocitopenia inducida por heparina, que impide la utilización de de estos anticoagulantes.
Las terapias de adsorción (por ejemplo, las terapias de reemplazo hepático) pueden ser incompatibles con la utilización de, por ejemplo, heparina, si ésta satura los puntos de unión (previstos para la adsorción de toxinas) del adsorbente.
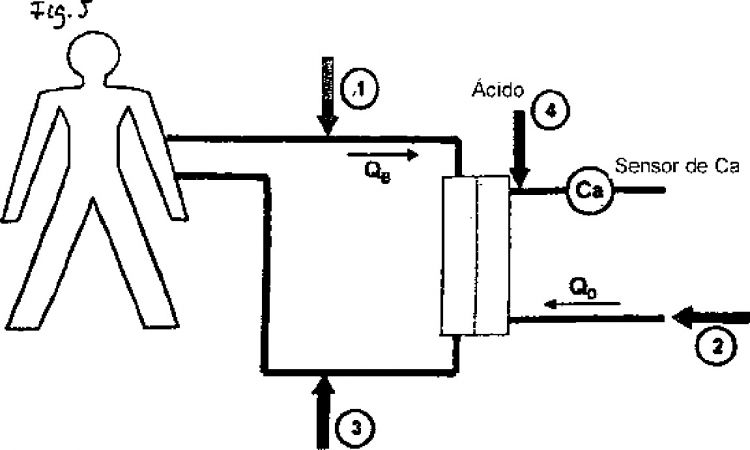
Una alternativa que evita los problemas enumerados es la inhibición de la coagulación a nivel regional (sólo en el circuito extracorporal, sobre todo, durante el contacto de la sangre con la membrana) mediante citrato. En este procedimiento, representado en la figura 1, la concentración de calcio libre (Ca) es reducida por la adición de citrato trisódico en el punto correspondiente a la posición 1 en la figura 1, hasta interrumpir la cascada de coagulación. En ese caso, dos moléculas de citrato conforman un complejo con, respectivamente, tres iones de Ca. También la utilización de producto dializado libre de Ca, correspondiente a la posición 2 en la figura 1, y la consecuente eliminación de Ca, contribuyen con la reducción de la concentración. Para evitar una depleción del cuerpo de Ca y Mg (que también se liga con citrato) se debe infundir otra solución (véase posición 3 en la figura 1), que contiene iones de Ca y de Mg en una concentración adaptada, en la rama venosa del circuito extracorporal o en un acceso venoso independiente.
Estudios clínicos [Morita Y, Johnson RW, Dorn RE, Hall DS, "Regional anticoagulation during hemodialysis using citrate" (Anticoagulación regional durante la hemodiálisis utilizando citrato). The American Journal of the Medical Sciences (1961); Janssen MJMF et al., "Citrate compared to low molecular weight heparin anticoagulation in chronic hemodialysis patients" (Citratos comparados con anticoagulación con heparina de bajo peso molecular en pacientes crónicos de hemodiálisis), Kindney Int (1996) 49:806-813; Mehta RL, McDonald BR, Aguilar MM, Ward DM, "Regional citrate anticoagulation for continuous arteriovenous hemodialysis in critically ill patients" (Anticoagulación regional con citrato para hemodiálisis arteriovenosa continua en pacientes con enfermedades críticas). Kidney Int (1990) 38:976-981] demuestran que la anticoagulación regional con citrato inhibe de manera muy efectiva la coagulación de la sangre en el circuito extracorporal. Al mismo tiempo, se reduce el riesgo de hemorragia para los pacientes. Por ello, la diálisis con citrato es considerada una alternativa interesante y efectiva a la anticoagulación convencional con heparina para aquel sector de la población de pacientes para los cuales es perjudicial o está claramente contraindicada la utilización de heparina, como ha sido descrito anteriormente.
A pesar de esta clara ventaja terapéutica, la anticoagulación con citrato sólo se utiliza hasta ahora de manera limitada, y no como procedimiento automatizado estandarizado. Los motivos de ello son:
El mayor costo del procedimiento puede ser limitado mediante una realización técnica adecuada; ciertos costos mayores están legitimados en el caso de pacientes con intolerancias a la heparina. El suministro de citrato o de complejos de citrato se puede reducir notablemente mediante la extracción eficiente a través de la membrana (utilización de un filtro Highflux de gran superficie, eventualmente, en combinación con HDF en postdilución). Un suministro restante reducido probablemente es tolerado, si no es así, también puede ser estimado y compensado mediante un modelado adecuado del proceso de diálisis y la metabolización de los complejos.
Por la memoria WO 91/06326 se conoce un procedimiento de diálisis de anticoagulación con citrato. Como anticoagulante, se agrega al conducto arterial de alimentación del circuito sanguíneo extracorporal citrato trisódico, asimismo, la cantidad de citrato trisódico por unidad de tiempo sólo es adaptada a la tasa de flujo sanguíneo en el circuito extrapolar. Al incrementarse o reducirse la tasa de flujo sanguíneo, también se incrementa o se reduce la tasa de suministros de citrato trisódico. La concentración de iones de calcio de la sangre del paciente no se vigila de manera continua, sino a distancias temporales mayores, mediante pruebas de sangre. Dado que falta una supervisión constante o continua de la concentración de calcio en la sangre de los pacientes y la cantidad de citrato agregado sólo se orienta según la tasa de flujo de sangre y no según el nivel de calcio del paciente, en este procedimiento conocido no se puede excluir de manera segura que presenten valores de calcio en la sangre del paciente que sean ni fisiológicos y puedan acarrear consecuencias que pongan en riesgo la vida del paciente.
Por la memoria US 5 714 060 A se conoce un dializador con un hemodializador, así como con un circuito sanguíneo extracorporal, al cual está conectada una bolsa para la adición de la solución de sal común a la sangre, corriente arriba del hemodializador, así como un sensor de sangre corriente abajo del hemodializador.
Aunque también se conocen sensores sensibles a iones, mediante los cuales también se pueden obtener la concentración de iones de calcio o magnesio en la sangre del paciente a intervalos temporales reducidos. Sin embargo, la utilización de un sensor en contacto con la sangre es desventajosa, y por ello, indeseable, debido a la posible toxicidad, los requerimientos de esterilización así como...
Reivindicaciones:
1. Aparato de diálisis con un hemodializador y/o un hemofiltro, así como con un circuito sanguíneo extracorporal, al cual están conectados los medios para la adición de citrato a la sangre, corriente arriba del hemodializador y/o hemofiltro, caracterizado por un conducto de producto dializado que presenta medios para la detección de una concentración de iones en el producto dializado, corriente abajo del hemodializador y/o hemofiltro respecto de la dirección de flujo del producto dializado, así como medios para la adición de una solución sustituta a la sangre que contiene iones, que pueden ser puestos en contacto, corriente abajo del hemodializador y/o hemofiltro, con el circuito sanguíneo extracorporal.
2. Aparato de diálisis acorde a la reivindicación 1, caracterizado porque los medios para detectar la concentración de iones están ejecutados en forma de uno o múltiples sensores sensibles a iones.
3. Aparato de diálisis acorde a la reivindicación 2, caracterizado porque está previsto un dispositivo de evaluación que realiza la verificación de la función del o de los sensores a intervalos temporales o al ser activado por un operador.
4. Aparato de diálisis acorde a una de las reivindicaciones 1 a 3, caracterizado porque los medios para la adición de una sustancia mediante la cual se puede modificar el valor del pH del producto dializado están en contacto con el conducto de producto dializado.
5. Aparato de diálisis acorde a la reivindicación 4, caracterizado porque los medios están dispuestos de modo tal que la adición se efectúa corriente abajo del dializador respecto de la dirección de flujo del producto dializado.
6. Aparato de diálisis acorde a una de las reivindicaciones 1 a 5, caracterizado porque están previstos los medios mediante los cuales el flujo de producto dializado puede reducirse temporalmente.
7. Aparato de diálisis acorde a una de las reivindicaciones 1 a 6, caracterizado porque está prevista una unidad de control que inicia la adición de citrato a la sangre a intervalos temporales o al ser accionada por el operador, de modo tal que la adición se interrumpe temporalmente, y que registra continuamente, o a intervalos temporales, el valor de concentración determinado en el producto dializado al inicio de la interrupción de la adición de citrato, para la detección de una concentración de iones.
8. Aparato de diálisis acorde a una de las reivindicaciones 1 a 7, caracterizado porque está prevista una unidad de regulación conectada con los medios para detectar una concentración de iones en el producto dializado así como con los medios para la adición de citrato y/o con los medios para la adición de una solución sustituta que contiene iones y que, dependiendo de la comparación entre un valor nominal o un rango de valor nominal y un valor real determinado de la concentración de iones, provoca un incremento o una reducción de citrato y/o de una solución sustituta que contiene iones.
9. Aparato de diálisis acorde a la reivindicación 8, caracterizado porque la unidad de regulación y/o los medios para la adición de citrato están acondicionados de modo tal que la concentración de citrato no pueda bajar por debajo de un valor límite.
10. Aparato de diálisis acorde a una de las reivindicaciones 1 a 9, caracterizado porque está previsto un dispositivo de alarma que acciona una alarma al determinar una medición individual crítica de la concentración de iones o al determinar una tendencia crítica de mediciones individuales.
Patentes similares o relacionadas:
Aparatos de intercambio de masa y métodos para su uso, del 22 de Julio de 2020, de Haemair Limited: Método de uso de un intercambiador de masa, en donde el intercambiador de masa comprende: un primer canal para acomodar el flujo de un líquido a tratar; y un segundo canal […]
Dispositivo y método para para generar y visualizar códigos gráficos específicos de aparatos médicos y tratamientos médicos, del 22 de Julio de 2020, de FRESENIUS MEDICAL CARE DEUTSCHLAND GMBH: Procedimiento para la creación de una asociación de una identidad del paciente a una estación de tratamiento, comprendiendo la estación de tratamiento […]
Sistema de diálisis que incluye coordinación de energía del calentador múltiple, del 22 de Julio de 2020, de BAXTER INTERNATIONAL INC.: Un sistema de diálisis (10a, 10b) que comprende: un primer calentador de fluido; un segundo calentador de fluido; una fuente de alimentación principal para […]
Equipo de membrana de fibras huecas para el intercambio de sustancias y procedimiento para fabricarlo, del 3 de Junio de 2020, de enmodes GmbH: Paquete de fibras huecas enrollado sobre un núcleo, compuesto por una pluralidad de fibras huecas permeables a unas sustancias de al menos una estera de fibras huecas, […]
Sistemas de contenedores múltiples y usos de los mismos, del 22 de Abril de 2020, de Lo, Richard W.C: Un aparato de sistema de contenedores múltiples para preparar una formulación final de un medio de dializado peritoneal para administrar a un paciente para diálisis peritoneal, […]
Aparato de tratamiento de sangre con soporte de monitor de múltiples ejes, del 22 de Abril de 2020, de GAMBRO LUNDIA AB: Aparato de tratamiento de sangre extracorpóreo que comprende: una o más bombas situadas en una cara frontal de una carcasa , en el que las una […]
Predicción y optimización de terapia para hemoterapia de insuficiencia renal, especialmente hemodiálisis domiciliaria, del 15 de Abril de 2020, de BAXTER INTERNATIONAL INC.: Un dispositivo para su uso con una máquina de hemoterapia de insuficiencia renal que es operable para ejecutar una prescripción terapéutica para un paciente que […]
Catéter de membrana, del 25 de Marzo de 2020, de CCore Technology GmbH: Dispositivo que comprende un catéter para uso intravascular, en donde el catéter tiene una entrada de sangre y una salida de sangre y comprende una […]