Antígenos Neisseriales conservados.
Una proteína que comprende un fragmento de una proteína de Neisseria,
la proteína de Neisseria tiene la secuencia de aminoácidos de cualquiera de las SECs ID Nº 1 a 6, en la que dicho fragmento comprende una región antigénica de la proteína de Neisseria y consiste en 7 o más aminoácidos conservados consecutivos, en la que los aminoácidos conservados se encuentran en al menos el 50 % o más de las SECs ID Nº 1 a 6, con la condición de que dicha proteína no es una proteína completa de Neisseria que tiene la secuencia de aminoácidos de cualquiera de las SECs ID Nº 1 a 41.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10180438.
Solicitante: NOVARTIS VACCINES AND DIAGNOSTICS S.R.L..
Nacionalidad solicitante: Italia.
Dirección: VIA FIORENTINA 1 53100 SIENA (SI) ITALIA.
Inventor/es: RAPPUOLI, RINO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/095 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Neisseria.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
- C07K14/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de Neisseriaceae (F), p. ej. Acinetobacter.
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/31 C12N 15/00 […] › Genes que codifican proteínas microbianas, p. ej. enterotoxinas.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
PDF original: ES-2522667_T3.pdf


Fragmento de la descripción:
Campo de la invención La presente invención se refiere a antígenos de bacterias del género Neisseria conservados.
Antecedentes de la técnica Las bacterias Neisseria meningitidis y Neisseria gonorrhoeae son diplococos gram negativos, inmóviles, que son patógenos en seres humanos.
Basándose en el polisacárido capsular del organismo, se han identificado 12 serogrupos de N. meningitidis. El grupo A es el patógeno más frecuentemente implicado en enfermedades epidémicas en el Ã?frica subsahariano. Los serogrupos B y C son los responsables de la inmensa mayoría de los casos en los Estados Unidos y en países más desarrollados. Los serogrupos W135 e Y son responsables del resto de los casos en los Estados Unidos y en países desarrollados.
La vacuna meningocócica actualmente en uso es una vacuna polisacárida tetravalente compuesta por los serogrupos A, C, Y y W135. Sin embargo, esta estrategia no puede usarse para el Meningoco B, porque el polisacárido capsular del menB es un polímero de ácido N-acetil neuramínico unido a α (2-8) que está también presente en el tejido de mamíferos. Una estrategia de una vacuna para el menB utiliza mezclas de proteínas de membrana externa (PME) . Para superar la variabilidad antigénica, se han construido vacunas multivalentes que contienen hasta nueve porinas diferentes [por ejemplo, Poolman (1992) Development of a meningococcal vaccine. Infect. Agents Dis. 4: 13-28]. Otras proteínas utilizadas en vacunas de membrana externa han sido las proteínas opa y opc, pero ninguna de estas estrategias han podido superar la variabilidad antigénica [por ejemplo, Ala’Aldeen y Borriello (1996) The meningococcal transferrin-binding proteins 1 and 2 are both surface exposed and generate bactericidal antibodies capable of killing homologous and heterologous strains. Vaccine 14 (1) : 49-53].
En los documentos WO99/24578, WO99/36544, WO99/57280 y WO00/22430 se desvela una gran cantidad de proteínas y secuencias de nucleótidos de Neisseria. Tettelin y col. en [Science (2000) 287: 1809-1815] desvelan datos exhaustivos de secuencias de la cepa MC58.
Descripción de la invención Para garantizar un reconocimiento y una reactividad máximos de cepas cruzadas, pueden usarse regiones de proteínas que están conservadas entre diferentes especies, serogrupos y cepas de Neisseria. Por lo tanto, la invención proporciona proteínas que comprenden tramos de secuencias de aminoácidos compartidos en la mayor parte del género Neisseria, particularmente en N. meningitidis y N. gonorrhoeae.
La invención presenta una proteína que comprende un fragmento de una proteína de Neisseria según se define en las reivindicaciones.
El fragmento comprende una región antigénica o inmunogénica de la proteína de Neisseria.
Un aminoácido “conservado” es un aminoácido que, en una proteína de Neisseria concreta, está presente al menos en un x % de Neisseria. El valor de x puede ser de 50% o mayor, por ejemplo de 66%, 75%, 80%, 90%, 95% o incluso de 100% (es decir, el aminoácido se encuentra en la proteína en cuestión en todo el género Neisseria) .
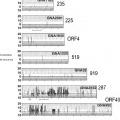
Para determinar si un aminoácido está “conservado” en una proteína Neisserial concreta, es necesario comparar este resto de aminoácido en las secuencias de la proteína en cuestión a partir de una pluralidad de diferentes especies de Neisseria (una “población de referencia”) . La población de referencia puede incluir diversas especies de Neisseria diferentes (preferentemente N. meningitidis y N.gonorrhoeae) o puede incluir una sola especie. La población de referencia puede incluir diversos serogrupos diferentes de una especie concreta (tales como los serogrupos A, B, C, W135, X, Y, Z y 29E de N. meningitidis) o un solo serogrupo. La población de referencia también puede incluir diversas cepas diferentes de un serogrupo concreto (tales como las cepas NG6/88, BZ198, NG3/88, 297-0, BZ147, BZ169, 528, BZ133, NGE31, NGH38, NGH15, BZ232, BZ83 y 44/76 de N. meningitidis B) . Una población de referencia preferida consta de las 5 cepas más comunes de N. meningitidis y/o de las 5 cepas más comunes de N. gonorrhoeae.
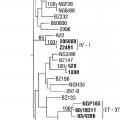
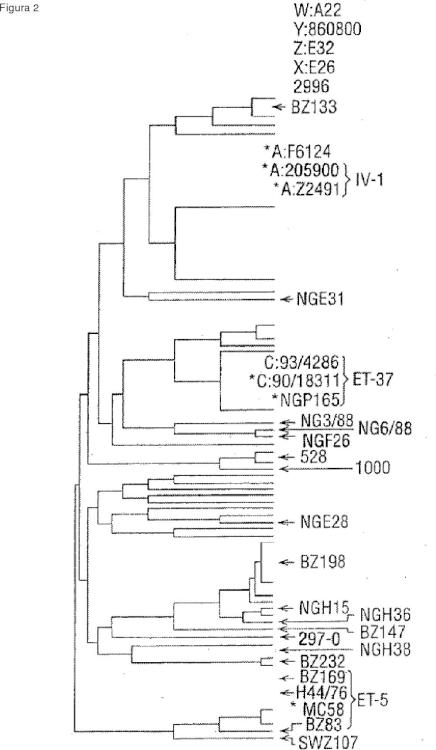
La población de referencia comprende preferentemente cepas k extraídas de diferentes ramas k de un árbol filogenético adecuado, tales como los descritos en (a) Ni y col. (1992) Epidemiol Infect 109: 227-239 (b) Wolff y col. (1992) Nucleic Acids Res 20: 4657 (c) Bygraves y Maiden (1992) J. Gen. Microbiol. 138: 523-531 (d) Caugant y col. (1987) J. Bacteriol. 69: 2781-2792. Otro árbol filogenético que puede usarse se muestra en la Figuras 8 y 9b del presente documento. Otro árbol filogenético que puede utilizarse se muestra en la Figura 2 del presente documento,
y otro en la Figura 4.
Se apreciará que, en la población de referencia, sólo se incluirá una especie, serogrupo o cepa concretos, si ésta codifica la proteína en la cual se localiza el aminoácido en cuestión. En el caso de aminoácidos incluidos en la ORF40, descrita más adelante, la población de referencia no debe incluir N. gonorrhoeae porque esta especie no contiene la ORF40.
Para proteínas solo encontradas en N. meningitidis, una población de referencia preferida comprende:
• N. meningitidis A, cepa Z2491
• N. meningitidis B, cepa NG6/88
• N. meningitidis W, cepa A22
¢N. gonorrhoeae, cepa Ng F62
Estas se describen en (a) Seiler A. et al. (1996) Mol. Microbiol. 19 (4) : 841 -856 (b) Maiden et al. (1998) Proc. Natl. Acad. Sci. USA 95: 3140 -3145 (c) Virji et al. (1992) Mol. Microbiol. 6: 1271 -1279 (d) Dempsey et al. (1991) J. Bacteriol. 173: 5476 -5486.
Sin embargo, para las proteínas encontradas únicamente en N. meningitidis, una población de referencia preferente comprende:
• N.meningitidis A, cepa Z2491
• N.meningitidis B, cepas NG6 / 88
• N.meningitidis W, cepas A22
Las secuencias de aminoácidos de diferentes Neissierias pueden compararse fácilmente usando ordenadores. Típicamente esto implicará el alineamiento de diversas secuencias usando un algoritmo tal como CLUSTAL [Thompson y col. (1994) Nucleic “Acids Res 22: 4673=4680; Trends Biochem Sci (1998) 23: 403-405] o, preferentemente, PILEUP [parte del paquete informático GCG de Wisconsin, preferentemente la versión 9.0].
Los aminoácidos conservados se aprecian fácilmente en un alineamiento de secuencias múltiple -en la posición del aminoácido en cuestión un gran parte de las secuencias alineadas contendrán el aminoácido en particular. Los aminoácidos conservados pueden apreciarse más visualmente usando un programa tal como BOXSHADE [disponible, por ejemplo, on-line en el NIH], PRETYBOX [GCG] Wisconsin, versión 10] o JALVIEW [disponible online en el EBI].
La invención presenta también una proteína que comprende una de las secuencias que se muestran en las Figuras.
Preferentemente, la proteína comprende un fragmento de una de las proteínas desveladas en los documentos WO99/24578, WO99/36544, WO99/57280 o WO00/22430, o un fragmento de una de las 2158 ORF desveladas por Tettelin y col. en [Science (2000) 287:1809-1815]. Más particularmente, la proteína comprende preferentemente un fragmento de la ORF40. La proteína de la invención no comprenderá ninguna secuencia de las proteínas explícitamente desveladas en los documentos WO99/24578, WO99/36544, WO99/57280, WO00/22430 o por Tettelin y col.
La invención también proporciona una proteína que comprende una de las secuencias mostradas en las Figuras.
Las proteínas de la invención pueden prepararse, por supuesto, mediante diversos medios (por ejemplo, por expresión recombinante, expresión natural, purificación a partir de cultivo celular, síntesis química, etc.) y en diversas formas (por ejemplo, natural, fusiones, etc.) . Preferentemente, se preparan de una forma sustancialmente pura (es decir, sustancialmente libre de otras proteínas Neisseriales o células huésped) .
También se desvelan anticuerpos que se unen a estas proteínas. Éstos pueden ser policlonales o monoclonales y pueden producirse mediante cualquier medio adecuado.
De acuerdo con un aspecto adicional, la invención proporciona ácido nucleico que codifica las proteínas de la invención. También debe apreciarse que la invención proporciona ácidos nucleicos que comprenden secuencias complementarias a éstos (por ejemplo para fines antisentido o exploración) .
Adicionalmente, la invención proporciona ácido nucleico que puede hibridarse con el ácido nucleico de N. meningitidis desvelado en los ejemplos, preferentemente en condiciones de “alta rigurosidad” (por ejemplo 65 º C en una solución... [Seguir leyendo]
Reivindicaciones:
1. Una proteína que comprende un fragmento de una proteína de Neisseria, la proteína de Neisseria tiene la secuencia de aminoácidos de cualquiera de las SECs ID Nº 1 a 6, en la que dicho fragmento comprende una región antigénica de la proteína de Neisseria y consiste en 7 o más aminoácidos conservados consecutivos, en la que los aminoácidos conservados se encuentran en al menos el 50 % o más de las SECs ID Nº 1 a 6, con la condición de que dicha proteína no es una proteína completa de Neisseria que tiene la secuencia de aminoácidos de cualquiera de las SECs ID Nº 1 a 41.
2. Una proteína según la reivindicación 1, en la que los aminoácidos conservados se encuentran en al menos el 50% omás delas SECs IDNº 1 a 41.
3. La proteína de la reivindicación 1, en la que dicho fragmento consiste en 20 o más aminoácidos conservados consecutivos.
4. Una proteína según la reivindicación 1, que comprende una o más de las siguientes secuencias de aminoácidos: (a) MFKRSVIAMACI; (b) ALSACGGGGGGSPDVKSADT; (c) SKPAAPVV; (d) QDMAAVS; (e) ENTGNGGAATTD; (f) DGPSQNITLTHCK; (g) RRSARSRRSLPAEMPLIPVNQADTLIVDGEAVSLTGHSGNIFAPEGNYRYLTYGA EKL; (h) VQGEPAKGEMLAGTAVYNGEVLHFH; (i) GRFAAKVDFGSKSVDGIIDS GDDLHMG; (j) QKFKAAIDGNGFKGTWTENGGGDVSG (R / K) FYGPAGEEVAGK YSYRPTDAEKGGFGVFAGKKDRD.
5. Un ácido nucleico que codifica una proteína según cualquiera de las reivindicaciones anteriores.
6. Un vector que comprende el ácido nucleico de la reivindicación 5.
7. El vector de la reivindicación 6, que es un vector de expresión.
8. Una célula huésped transformada con el vector de las reivindicaciones 6 o 7.
9. Una proteína según cualquiera de las reivindicaciones 1 a 4, o el ácido nucleico según la reivindicación 5, para su uso como medicamento.
10. El uso de una proteína según cualquiera de las reivindicaciones 1 a 4, o el ácido nucleico según la reivindicación 5, en la fabricación de un medicamento para tratar o prevenir la infección debido a la bacteria Neisseria.
11. El uso de una proteína según cualquiera de las reivindicaciones 1 a 4, o el ácido nucleico según la reivindicación 5, en la fabricación de un reactivo de diagnóstico multiespecífico.
Figura 1 Figura 1 Cont. Figura 1 Cont. Figura 2
Figura 3
Posición de aminoácidos Figura 4 Figura 5 Figura 5 Cont. Figura 5 Cont. Figura 5 Cont. Figura 5 Cont. Figura 5 Cont. Figura 5 Cont. Figura 5 Cont. Figura 5 Cont.
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Métodos de tratamiento y prevención de infecciones por staphylococcus aureus y afecciones asociadas, del 15 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición para uso en un método de inmunización de un sujeto contra la infección por S. aureus, comprendiendo dicha composición: (i) un fragmento de polipéptido […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]