Anticuerpos monoclonales contra CD30 que carecen de restos fucosilo.
Un anticuerpo anti-CD30 monoclonal, desfucosilado, aislado que comprende una CDR1 de región variable de cadena pesada que comprende la SEC ID Nº:
7, una CDR2 de región variable de cadena pesada que comprende la SEC ID Nº: 10, una CDR3 de región variable de cadena pesada que comprende la SEC ID Nº: 13, una CDR1 de región variable de cadena ligera que comprende la SEC ID Nº: 16, una CDR2 de región variable de cadena ligera que comprende la SEC ID Nº: 19, y una CDR3 de región variable de cadena ligera que comprende la SEC ID Nº: 22.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/005854.
Solicitante: Medarex, L.L.C.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Route 206 and Province Line Road Princeton, NJ 08540 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CARDARELLI,Josephine,M, BLACK,AMELIA NANCY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/30 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › de células tumorales.
PDF original: ES-2498794_T3.pdf




Fragmento de la descripción:
Anticuerpos monoclonales contra CD30 que carecen de restos fucosilo Antecedentes de la invención La molécula de superficie celular CD30 es un miembro de la superfamilia del receptor del factor de necrosis tumoral (TNF-R) . Esta familia de moléculas tiene homología variable entre sus miembros e incluye el receptor del factor de crecimiento nervioso (NGFR) , CD120 (a) , CD120 (b) , CD27, CD40 y CD95. Estas moléculas se caracterizan típicamente por la presencia de repeticiones múltiples ricas en cisteína en la región extracitoplasmática (de Bruin, P.C., y col. Leukemia 9:1620-1627 (1995) ) . Los miembros de esta familia se consideran cruciales para regular la proliferación y diferenciación de linfocitos.
La CD30 es una glucoproteína transmembrana de tipo I con seis (ser humano) o tres (murino y rata) repeticiones ricas en cisteína con una secuencia bisagra central. La CD30 existe como una molécula de membrana de 120 kDa que se desarrolla a partir de una proteína precursora intercelular de 90 kDa. Se desprende de la superficie celular como una proteína soluble (sCD30) de aproximadamente 90 kDa. El desprendimiento de sCD30 sucede como un proceso activo de células CD30 viables y no está simplemente ocasionado por la liberación de células que se están muriendo o que están muertas. Los ADNc que codifican la proteína CD30 se han clonado de bibliotecas de expresión de la línea de linfocitos T humanos HLTV-1 HUT-102 por inmunoexploración con anticuerpos monoclonales Ki-1 y Ber-H2 (Schwab, U., y col. Nature 299:65 (1982) ) . El ADNc de CD30 de ratón y rata se ha descubierto que codifica 498 y 493 aminoácidos, respectivamente. El ADNc de CD30 de ser humano codifica 90 aminoácidos adicionales, parcialmente duplicados desde uno de los dominios ricos en cisteína. El gen de CD30 se ha mapeado en 1p36 en seres humanos y en 5q36.2 en ratas.
La CD30 se expresa preferentemente por células linfoides activadas. Específicamente, la estimulación de CD30 en células linfoides ha demostrado inducir efectos biológicos pleiotrópicos, que incluyen proliferación, activación, diferenciación y muerte celular, dependiendo del tipo de célula, fase de diferenciación y presencia de otros estímulos (Gruss, H.J. y col., Blood 83:2045-2056 (1994) ) . La CD30 se identificó originalmente por el anticuerpo monoclonal Ki1, que es el reactivo con antígenos expresados en células de Hodgkin y Reed-Sternberg de la enfermedad de Hodgkin (Schwab y col., Nature 299:65 (1982) ) . Por consiguiente, CD30 se usa ampliamente como marcador clínico para linfoma de Hodgkin y neoplasias hematológicas relacionadas (Froese y col., J. Immunol. 139:2081 (1987) ; Carde y col., Eur. J. Cancer 26:474 (1990) ) .
Posteriormente, CD30 mostró ser expresado en un subconjunto de linfomas no Hodgkin (LNH) , incluyendo el linfoma de Burkitt, linfomas de células grandes anaplásicas (LCGA) , linfomas cutáneos de linfocitos T, linfomas de células escindidas pequeñas nodulares, linfomas linfocíticos, linfomas de linfocitos T periféricos, linfomas de Lennert, linfomas inmunoblásticos, leucemia/linfomas de linfocitos T (LLLT) , leucemia de linfocitos T en adulto (LLT-A) y linfomas foliculares eritroblásticos/centrocíticos (eb/cc) (Stein y col., Blood 66:848 (1985) ; Miettinen, Arch. Pathol. Lab. Med. 116:1197 (1992) ; Piris y col., Histopathology 17:211 (1990) ; Burns y col., Am. J. Clin. Pathol. 93:327 (1990) ; y Eckert y col., Am. J. Dermatopathol. 11:345 (1989) ) , así como diversas líneas viralmente transformadas tales como linfocitos T transformados con virus linfotrófico de linfocitos T humanos I o II y linfocitos B transformados con el virus de Epstein-Barr (Stein y col., Blood 66:848 (1985) ; Andreesen y col., Blood 63:1299 (1984) ) . Además, la expresión de CD30 se ha documentado en carcinomas embrionarios, carcinomas no embrionarios, melanomas neoplásicos, tumores mesenquimáticos, y líneas celulares mieloides y macrófagos en fases de diferenciación tardías (Schwarting y col., Blood 74:1678 (1989) ; Pallesen y col., Am J. Pathol. 133:446 (1988) ; Mechtersheimer y col., Cancer 66:1732 (1990) ; Andreesen y col., Am. J. Pathol. 134:187 (1989) ) .
Dado que el porcentaje de células CD30 positivas en individuos normales es bastante pequeño, la expresión de CD30 en células tumorales la convierte en una diana importante para la terapia mediada por anticuerpos para dirigir específicamente agentes terapéuticos contra células neoplásicas CD30 positivas (Chaiarle, R., y col. Clin. Immunol. 90 (2) :157-164 (1999) ) . La terapia mediada por anticuerpos ha mostrado que aumenta la citotoxicidad de células CD30 positivas tanto por la activación del complemento como por la citotoxicidad celular dependiente de anticuerpo (CCDA) (Pohl C., y col. Int J Cancer 54:418 (1993) ) . Sin embargo, aunque los resultados obtenidos hasta ahora establecen claramente a CD30 como una diana útil para inmunoterapia, también muestran que anticuerpos murinos disponibles actualmente no constituyen agentes terapéuticos ideales. La terapia pasiva con anticuerpos no ha sido eficaz in vitro o in vivo contra pacientes con enfermedad de Hodgkin refractaria. Un ensayo clínico del anticuerpo anti-CD30 Ber-H2 mostró la localización del anticuerpo, pero sin respuestas (Falini B. y col. (1992) Brit J Haematol. 82:38-45; Koon, H.B. y col. (2000) Curr Opin in Oncol. 12:588-593) . A través del acoplamiento de un anticuerpo anti-CD30 a una toxina de ricina desglucosilada-toxina de cadena A, se mostró citotoxicidad en el tratamiento de enfermedad de Hodgkin humana en un modelo de ratón SCID, aunque también se observaron toxicidades de grado 3 en los sujetos (Schell, R. y col. (2002) Annals of Oncology 13:57-66) .
Por consiguiente, existe la necesidad de anticuerpos terapéuticos mejorados contra CD30 que sean más eficaces para el tratamiento y/o prevención de enfermedades mediadas por CD30.
Sumario de la Invención La presente invención proporciona anticuerpos desfucosilados aislados (es decir, anticuerpos que carecen de restos de fucosa) que se unen a la CD30 humana y que presentan destrucción de citotoxicidad celular dirigida por anticuerpos (CCDA) potenciada de células que expresan CD30 en comparación con la forma no desfucosilada del anticuerpo (es decir, anticuerpos que contienen restos de fucosa) . También se proporcionan procedimientos para el tratamiento de diversas enfermedades en las que interviene la expresión de CD30 usando los anticuerpos y las composiciones de la invención.
El anticuerpo monoclonal desfucosilado aislado, o una parte de unión a antígeno del mismo, puede unirse a CD30 humana con una KD de 10 x 10-8 M o menor, más preferentemente 1 x 10-8 M o menor, más preferentemente 5 x 10-9
o menor o incluso más preferentemente, 1 x 10-9 o menor.
Los anticuerpos desfucosilados pueden unirse a CD30 e inhibir el crecimiento de células que expresan CD30 potenciando la citotoxicidad celular dependiente de anticuerpos (CCDA) en presencia de células efectoras humanas (por ejemplo, monocitos o células mononucleares) , en comparación con la forma fucosilada del anticuerpo. El anticuerpo desfucosilado puede mediar la CCDA aumentada de células que expresan CD30 en presencia de células efectoras humanas pero en presencia de células efectoras de ratón.
Un anticuerpo desfucosilado puede inducir la CCDA de células L1236 in vitro en la que la forma fucosilada del anticuerpo no induce CCDA, en condiciones de una concentración de anticuerpo de 0, 1 μg/ml y a una proporción de células diana con respecto a células efectoras de 1:50. Un anticuerpo desfucosilado puede potenciar la CCDA de células L540, L428 y Karpas in vitro en comparación con la forma fucosilada del anticuerpo, en condiciones de una concentración de anticuerpo de 0, 1 μg/ml y a una proporción de células diana con respecto a células efectoras de 1:50. Por consiguiente, los anticuerpos proporcionaron un medio mejorado para el tratamiento de trastornos caracterizados por la expresión de CD30.
El anticuerpo desfucosilado de la invención es un anticuerpo monoclonal. El anticuerpo puede ser un anticuerpo monoclonal humano, humanizado o quimérico. Preferentemente, el anticuerpo humanizado o quimérico se prepara a partir de un anticuerpo anti-CD30 de ratón seleccionado del grupo que consiste en: AC10, HeFi-1, Ber-H2, Ki-1, Ki-4, HRS-3, Irac, HRS-4, M44, M67, Ber-H8. En otro aspecto, la invención se refiere a un anticuerpo monoclonal humano.
La invención proporciona un anticuerpo anti-CD30 monoclonal, desfucosilado, aislado, que comprende una CDR1 de región variable de cadena pesada que comprende la SEC ID Nº : 7, una CDR2 de región variable de cadena pesada que comprende la SEC ID Nº : 10, una CDR3 de región variable de cadena pesada que comprende la... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo anti-CD30 monoclonal, desfucosilado, aislado que comprende una CDR1 de región variable de cadena pesada que comprende la SEC ID Nº : 7, una CDR2 de región variable de cadena pesada que comprende la SEC ID Nº : 10, una CDR3 de región variable de cadena pesada que comprende la SEC ID Nº : 13, una CDR1 de región variable de cadena ligera que comprende la SEC ID Nº : 16, una CDR2 de región variable de cadena ligera que comprende la SEC ID Nº : 19, y una CDR3 de región variable de cadena ligera que comprende la SEC ID Nº : 22.
2. El anticuerpo de la reivindicación 1, en el que:
(a) la región variable de cadena pesada comprende la secuencia de aminoácidos SEC ID Nº : 1; y
(b) la región variable de cadena ligera comprende la secuencia de aminoácidos SEC ID Nº : 4.
3. El anticuerpo de la reivindicación 1 o 2, que es un anticuerpo humano.
4. El anticuerpo de una cualquiera de las reivindicaciones 1 a 3 conjugado con una citotoxina.
5. Una célula hospedadora que comprende genes de cadena pesada y ligera de inmunoglobulina que codifican un anticuerpo anti-CD30 como se define en una cualquiera de las reivindicaciones 1 a 4, en la que dicha célula hospedadora carece de una fucosiltransferasa, de tal manera que el anticuerpo anti-CD30 expresado por dicha célula hospedadora carece de restos de fucosa.
6. La célula hospedadora de la reivindicación 5, en la que los genes de cadena pesada y ligera de inmunoglobulina son genes de cadena pesada y ligera de inmunoglobulina humana.
7. La célula hospedadora de la reivindicación 5 o 6, en la que dicha fucosiltransferasa es FUT8.
8. La célula hospedadora de una cualquiera de las reivindicaciones 5 a 7, que es una célula CHO.
9. Un procedimiento de inhibición in vitro del crecimiento de células CD30+ que comprende poner en contacto dichas células con un anticuerpo anti-CD30 desfucosilado como se define en una cualquiera de las reivindicaciones 1 a 4, en condiciones suficientes para inducir citotoxicidad celular dependiente de anticuerpos (CCDA) de dichas células.
10. El procedimiento de la reivindicación 9, en el que dichas células son células tumorales y/o dicho anticuerpo anti-CD30 es un anticuerpo humano.
11. Un anticuerpo como se define en las reivindicaciones 1 a 4, para su uso en un procedimiento de inhibición del crecimiento de células tumorales que expresan CD30 en un sujeto.
12. El anticuerpo de la reivindicación 11, en el que las células tumorales son de una enfermedad seleccionada de enfermedad de Hodgkin (EH) , linfoma de células grandes anaplásicas (LCGA) , linfoma no Hodgkin, linfoma de Burkitt, linfomas cutáneos de linfocitos T, linfomas de células escindidas pequeñas nodulares, linfomas linfocíticos, linfomas de linfocitos T periféricos, linfomas de Lennert, linfomas inmunoblásticos, leucemia/linfomas de linfocitos T (LLLT) , leucemia de linfocitos T en adulto (LLT-A) y cánceres de linfomas foliculares eritroblásticos/centrocíticos (eb/cc) , linfomas de células grandes difusas de linaje B, linfoma de linfocitos T de tipo linfadenopatía angioinmunoblástica (LDAI) , linfoma de linfocitos T en adulto (LTA) , linfomas basados en cavidad corporal asociada con VIH, carcinomas embrionarios, carcinomas indiferenciados de la rinofaringe (por ejemplo, tumor de Schmincke) , enfermedad de Castleman, sarcoma de Kaposi, linfomas de linfocitos T CD30+ y linfomas de linfocitos de B CD30+.
VH del anti-CD30 5F11 Segmento V: Locus: 4-34 Segmento D: Locus: -7-27 Segmento J: JH4b
VL del anti-CD30 5F11
Segmento V: Locus: L15
Segmento J: JK5
VH del anti-CD30 17G1 Segmento V: Locus: 3-07 Segmento D: No encontrado Segmento J: JH2
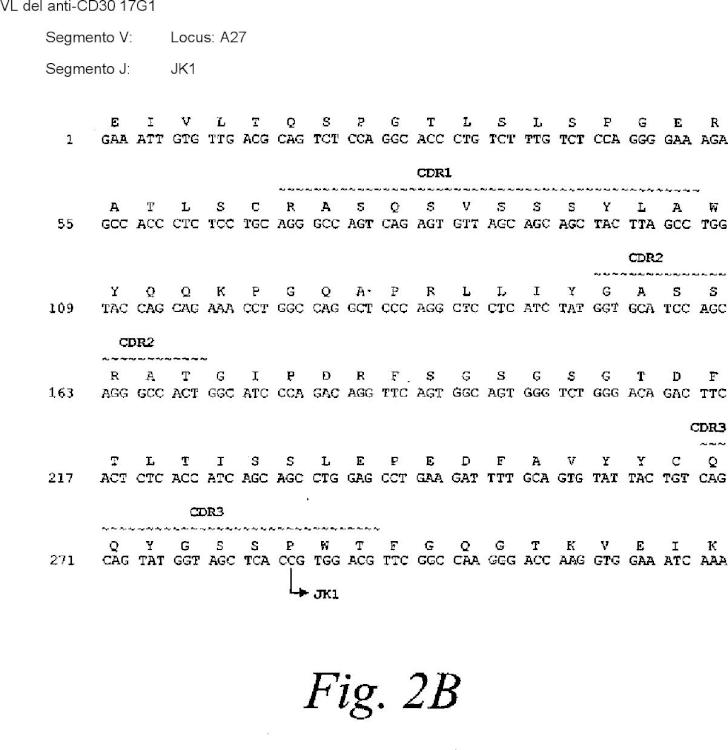
VL del anti-CD30 17G1 Segmento V: Locus: A27 Segmento J: JK1
VH del Anti-2H9 CD30 Segmento V: Locus: 4-34 Segmento D: Locus: 5-12 Segmento J: JH2
VL del anti-2H9 CD30 Segmento V: Locus: L6 Segmento J: JK1
Patentes similares o relacionadas:
Composiciones para la supresión del cáncer por inhibición de TMCC3, del 29 de Julio de 2020, de Development Center For Biotechnology: Un anticuerpo contra la proteína con dominios de superhélice transmembrana 3 (TMCC3), o un fragmento de unión de la misma, en donde el anticuerpo […]
Bloqueo de CD73, del 22 de Julio de 2020, de Innate Pharma: Un anticuerpo aislado que específicamente se une a un polipéptido CD73 humano en la superficie de una célula y que tiene capacidad de neutralizar […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Método para purificar anticuerpos, del 8 de Julio de 2020, de UNITED THERAPEUTICS CORPORATION: Método para purificar una composición biológica, que comprende someter a diafiltración la composición biológica con solución salina tamponada con fosfato (PBS) para […]
Redirectores de células T específicas de antígenos, del 1 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una nanoparticula que comprende en su superficie: (A) un anticuerpo que se une especificamente a un antigeno de celula diana o epitopo del mismo; y (B) un resto […]
Conjugados fármaco-anticuerpo anti-lrrc15 humano y métodos para su uso, del 17 de Junio de 2020, de AbbVie Inc: Un conjugado de farmaco-anticuerpo anti-huLRRC15 ("ADC") que comprende un agente antimitotico unido a un anticuerpo anti-huLRRC15 por medio de un conector, en donde […]
Cadenas ligeras comunes y procedimientos de uso, del 3 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Una molécula de unión a antígeno biespecífica activadora de linfocitos T que comprende un primer y un segundo resto de unión a antígeno, en la que el primer resto […]
Anticuerpos anti-CD3 y métodos de uso, del 27 de Mayo de 2020, de GENENTECH, INC.: Un anticuerpo biespecífico que comprende un brazo anti-CD3 que comprende un primer dominio de unión que comprende (a) un dominio VH que comprende una secuencia de aminoácidos […]