ANTICUERPOS PARA LA DETECCIÓN Y CUANTIFICACIÓN DE AGENTES ANTICOAGULANTES.
Anticuerpos para la detección y cuantificación de agentes anticoagulantes.
La presente invención se relaciona con el diseño de haptenos estructuralmente relacionados con compuestos anticoagulantes orales de tipo coumarínico (CAOC) con el objetivo de ser usados para la producción de anticuerpos específicos contra este tipo de sustancias y la posterior utilización de éstos para el desarrollo de herramientas de diagnóstico de uso en laboratorio o en dispositivos point-of-care (PoC). En particular, con los anticuerpos producidos se ha desarrollado una herramienta de diagnóstico que permite la cuantificación de los niveles plasmáticos de CAOC en pacientes tratados con este tipo de fármacos.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201231836.
Solicitante: CENTRO DE INVESTIGACIÓN BIOMÉDICA EN RED EN BIOINGENIERÍA, BIOMATERIALES Y NANOMEDICINA.
Nacionalidad solicitante: España.
Inventor/es: MARCO COLAS,Mª PILAR, SALVADOR VICO,Juan Pablo.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D311/56 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 311/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que contienen un átomo de oxígeno como único heteroátomo, condensados con otros ciclos. › sin átomos de hidrógeno en la posición 3.
PDF original: ES-2472290_A1.pdf



Fragmento de la descripción:
Anticuerpos para la detecciïn y cuantificaciïn de agentes anticoagulantes
OBJETO DE LA INVENCIïN
La presente invenciïn se relaciona con compuestos, mïtodos y ensayos para la determinaciïn de los niveles de agentes anticoagulantes de tipo cumarïnico en una muestra biolïgica, asï como con mïtodos, ensayos y kits para la determinaciïn de la dosis adecuada de dichos agentes a administrar a un paciente en necesidad de dicho tratamiento.
ANTECEDENTES DE LA INVENCIïN
Los compuestos anticoagulantes de tipo cumarïnico (CAC) son ampliamente utilizados en todos los païses con el objetivo de prevenir o controlar ciertas cardiopatïas. Asï, la warfarina es empleada mayoritariamente en Norteamïrica, Escandinavia y Reino Unido, mientras que el acenocumarol y el fenprocumïn se emplean principalmente en Europa. Estos compuestos son antagonistas de la vitamina K que inhiben los factores de coagulaciïn II (protrombina) , VII, IX y X. Sin embargo, su estrecha ventana terapïutica sumada al hecho de que su efecto sea distinto segïn el genotipo del paciente, sus enfermedades u otros factores relacionados con el estilo de vida, plantean ciertas dificultades a la hora de fijar la dosis adecuada de dichos compuestos para cada paciente, resultando en un aumento de hemorragias (por exceso de dosis) o formaciïn de trombos (por defecto de dosis) . La dosis de anticoagulantes orales puede ir desde 0, 75 mg/dïa a 12 mg/dïa en funciïn del paciente y del tipo particular de anticoagulante.
Las tïcnicas analïticas que se emplean actualmente para determinar o para corregir la dosis de agente anticoagulante oral para un paciente comprenden la medida del tiempo de protrombina (PT) y correspondiente INR (International Normalized Ratio) , de modo que tales parïmetros determinan la tendencia de la sangre a coagular en presencia de posibles trastornos de la coagulaciïn. El rango normal de PT varïa entre 12 y 15 segundos y el de INR entre 0, 8 y 1, 2 (a mayor valor de INR, mayor tiempo necesario para la coagulaciïn) . Estudios en los que se evalïo el tratamiento a largo plazo de la trombosis venosa profunda (TVP) mostraron que las recurrencias se impiden por completo a valores de INR de entre 2, 0 y 3, 0, sin embargo se recomienda que el tratamiento anticoagulante de tipo cumarïnico resulte en valores de INR por debajo de 2, 0.
Los compuestos anticoagulantes se administran como mezclas racïmicas que son rïpidamente absorbidas por el tracto gastrointestinal, de modo que en pocas horas se tienen cantidades detectables en plasma de los anticoagulantes. Aunque hay biodisponibilidad de los dos enantiïmeros, la forma R del enantiïmero tiene una vida media superior a la forma S del enantiïmero, que es mïs susceptible de ser metabolizado.
Se han descrito diferentes metodologïas para la determinaciïn de anticoagulantes en plasma y en orina. La mayorïa de ellas se basan principalmente en tïcnicas cromatogrïficas acopladas a espectrometrïa de masas. El objetivo de estas tïcnicas es realizar un seguimiento de la concentraciïn de anticoagulante de tipo cumarïnico administrado y de sus metabolitos para confirmar la presencia del anticoagulante y establecer su farmacocinïtica. La tïcnica de HPLC-MS ha sido empleada en la determinaciïn selectiva de warfarina (W) , acenocumarol (ACL) y fenprocumïn (PPC) , con un lïmite de detecciïn (LOD) de 0, 5 ng/ml en la detecciïn del anticoagulante parental y de sus metabolitos derivados (Vecchione G et al. 2007 J Chromatogr B 850:507; Rentsch KM et al. 2000 J Chromatogr B 742: 131) . Asimismo, la tecnologïa basada en HPLC-espectrometrïa de masas de ionizaciïn por electrospray se ha empleado en la identificaciïn y cuantificaciïn de anticoagulantes tales como warfarina y acenocumarol en muestras de pacientes (Kollroser M & Schober C 2002 Clin Chem 48 (1) : 84-91) . Sin embargo, estas tïcnicas requieren un pretratamiento y derivatizaciïn de las muestras de plasma o de orina a analizar, lo cual hace mïs lento el proceso.
Por otro lado, aunque los mïtodos inmunoquïmicos son altamente especïficos y sensibles y ademïs ofrecen la posibilidad de diferentes formatos de ensayo, no son muy empleados en la determinaciïn de anticoagulantes orales. Se han desarrollado anticuerpos monoclonales anti-warfarina asï como un biosensor de resonancia de plasmïn de superficie para la determinaciïn de warfarina en plasma (Fitzpatrick B & O'Kennedy R 2004 J Immunol Methods 291: 11) . El rango de precisiïn logrado mediante esta tïcnica es de 4-250 ng/ml, dentro del rango clïnico. Sin embargo, no se ha mostrado su selectividad de detecciïn de warfarina frente a otros metabolitos principales.
Tambiïn se han descrito metodologïas dirigidas a establecer una dosis adecuada de un tratamiento basado en un anticoagulante a administrar a un sujeto en necesidad de dicho tratamiento. La solicitud de patente internacional WO 2004/003550 estï dirigida a mïtodos, entre otros, para la caracterizaciïn fenotïpica metabïlica de agentes anticoagulantes y para la administraciïn a un sujeto de una dosis segura de un agente anticoagulante, asï como ensayos para la detecciïn de metabolitos especïficos de enzima en una muestra biolïgica. El documento de patente en Estados Unidos US 2010/0273203 estï dirigido a mïtodos para la determinaciïn de la dosis adecuada de warfarina para un sujeto, que comprende determinar el perfil metabïlico de warfarina del sujeto, comparar dicho perfil con una base de datos y seleccionar un perfil similar de la base de datos al perfil metabïlico del sujeto, en donde la dosis del perfil de la base de datos es conocida.
En los pacientes en tratamiento con anticoagulantes de tipo cumarïnico, pequeïas variaciones en la dosis del medicamento pueden ocasionar grandes variaciones en su efecto. Es precisamente por este motivo, que se debe monitorizar periïdicamente el efecto de los agentes anticoagulantes de tipo cumarïnico mediante anïlisis. Cada paciente requiere una dosis individualizada y adecuada a sus necesidades, la cual debe ser previamente ajustada para mantener el tiempo de coagulaciïn dentro del intervalo adecuado. Por otro lado, el nivel de coagulaciïn apropiado para cada paciente se determina segïn la enfermedad que padece. La monitorizaciïn y control del paciente bajo tratamiento con anticoagulantes de tipo cumarïnico son especialmente crïticos al inicio de dicho tratamiento. Efectos adversos derivados del tratamiento con anticoagulantes son las hemorragias leves, tales como pequeïas hemorragias (sangrado de las encïas, nariz, etc.) , menstruaciïn mïs abundante de lo habitual, moratones o hematomas en la piel.
Por lo tanto, es necesario desarrollar metodologïas alternativas a las descritas en la tïcnica para la detecciïn especïfica y sensible de anticoagulantes de tipo cumarïnico y de sus metabolitos en muestras tales como plasma y orina, asï como metodologïas que permitan establecer un rïgimen de dosis adecuado para un paciente en necesidad de un tratamiento basado en anticoagulantes de tipo cumarïnico.
COMPENDIO DE LA INVENCIïN
En un primer aspecto, la invenciïn se relaciona con un hapteno de fïrmula (I) :
(I)
donde R1 se selecciona de entre H, NO2, NH2, halïgeno, OH, O-C1-4 alquilo, NHCOCH3, CF3 y
OCF3; donde R2 se selecciona de entre halïgeno, OH, C1-4 alquilo y O-C1-4 alquilo; donde n es un nïmero entero entre 1 y 6. R3 se selecciona de entre COOH, CHO, halïgeno, NH2, N3, C=CH, OH y SH.
En otro aspecto, la presente invenciïn se dirige a un procedimiento para la preparaciïn de un hapteno de fïrmula (I) que comprende hacer reaccionar un compuesto de fïrmula (II) :
(II)
donde R1 y R2 se definen como anteriormente; con un compuesto de fïrmula (III) :
(III) 20 donde n y R3 se definen como anteriormente.
En otro aspecto, la invenciïn se relaciona con un conjugado que comprende un hapteno de fïrmula (I) y un segundo componente seleccionado del grupo formado por:
(a) una proteïna transportadora o un fragmento de la misma que confiere antigenicidad, 25 (b) un oligonucleïtido,
(c) una etiqueta detectable, y
(d) un polïmero o un soporte inorgïnico.
En otro aspecto, la invenciïn se relaciona con un anticuerpo que reconoce especïficamente 30 el conjugado anterior.
En otro aspecto, la invenciïn se relaciona con un antisuero que comprende el anticuerpo anterior.
En otro aspecto, la invenciïn se relaciona con el uso del anticuerpo anterior o del antisuero anterior en la detecciïn y/o cuantificaciïn de anticoagulantes de tipo cumarïnico en una muestra de un sujeto.
En otro aspecto, la invenciïn se relaciona con un mïtodo in vitro para la detecciïn y/o cuantificaciïn... [Seguir leyendo]
Reivindicaciones:
1. Un hapteno de fïrmula (I) :
5
R2
R3
donde R1 se selecciona entre H, NO2, NH2, halïgeno, OH, O-C1-4 alquilo, NHCOCH3, CF3 y OCF3; R2 se selecciona entre halïgeno, OH, C1-4 alquilo y O-C1-4 alquilo; n es un nïmero entero entre 1 y 6; y R3 se selecciona entre COOH, CHO, halïgeno, NH2, N3, C=CH, OH y SH.
2. Hapteno de fïrmula (I) donde R1 se selecciona entre H y NO2.
3. Hapteno segïn reivindicaciones 1 ï 2, donde R2 es H.
4. Hapteno segïn cualquiera de las reivindicaciones 1 a 3, donde R3 es COOH.
5. Hapteno segïn cualquiera de las reivindicaciones 1 a 4, donde n es 1.
6. Hapteno segïn reivindicaciïn 1, donde R1=H, R2=H, n=1 y R3=COOH con fïrmula (Ia) :
(Ia)
7. Hapteno segïn reivindicaciïn 1, donde R1=NO2, R2=H, n=1 y R3=COOH con fïrmula (Ib) :
5 (Ib)
8. Un procedimiento para la preparaciïn de un hapteno segïn se define en cualquiera de las reivindicaciones 1 a 7, que comprende hacer reaccionar un agente anticoagulante de tipo cumarïnico de fïrmula (II) : R1 R2
10
donde R1 se selecciona entre H, NO2, NH2, halïgeno, OH, O-C1-4 alquilo, NHCOCH3, CF3 y OCF3; R2 se selecciona entre halïgeno, OH, C1-4 alquilo y O-C1-4 alquilo;
con un compuesto de fïrmula (III) :
(III)
donde n es un nïmero entero entre 1 y 6; y R3 se selecciona entre COOH, CHO, halïgeno, NH2, N3, C=CH, OH y SH.
. 9. Procedimiento segïn reivindicaciïn 8, en donde el agente anticoagulante de fïrmula (II) tiene R1=R2=H, el compuesto de fïrmula (III) tiene R3=COOH y n=1, y el hapteno obtenido es un hapteno de fïrmula (I) donde R1=R2=H, R3=COOH y n=1.
10. Procedimiento segïn reivindicaciïn 8, en donde el agente anticoagulante de fïrmula (II) tiene R1=NO2 y R2=H, el compuesto de fïrmula (III) tiene R3=COOH y n=1 y el hapteno obtenido es un hapteno de fïrmula (I) donde R1=NO2, R2=H, R3=COOH y n=1.
11. Un conjugado que comprende un hapteno y un segundo componente seleccionado del grupo formado por a) una proteïna portadora o un fragmento de la misma que confiere antigenicidad, b) un oligonucleïtido, c) una etiqueta detectable, y d) un polïmero o un soporte inorgïnico, en donde el hapteno tiene la fïrmula (I)
R2
R3
(I)
donde R1 se selecciona entre H, NO2, NH2, halïgeno, OH, O-C1-4 alquilo, NHCOCH3, CF3 y
OCF3;; R2 se selecciona entre halïgeno, OH, C1-4 alquilo y O-C1-4 alquilo; n es un nïmero entero entre 1 y 6. R3 se selecciona entre COOH, CHO, halïgeno, NH2, N3, C=CH, OH y SH.
12. Conjugado segïn la reivindicaciïn 11, en donde la proteïna portadora se selecciona del grupo formado por hemocianina de cangrejo herradura (HCH) , albumina de suero bovino (BSA) , peroxidasa de rïbano (HRP) , ovoalbïmina (OVA) y conalbïmina (CONA) .
13. Conjugado segïn cualquiera de las reivindicaciones 11 ï 12, que comprende un hapteno de fïrmula (I) donde R1=R2=H, R3=COOH y n=1.
14. Conjugado segïn cualquiera de las reivindicaciones 11 ï 12, que comprende un hapteno de fïrmula (I) donde R1=NO2, R2=H, R3=COOH y n=1.
15. Conjugado segïn cualquiera de las reivindicaciones 13 a 14, en donde el hapteno y la proteïna portadora estïn unidos directamente entre sï mediante un enlace covalente resultante de la reacciïn entre el grupo carboxïlico del hapteno y el grupo amino de la proteïna.
16. Un procedimiento para la preparaciïn de un conjugado como se define en cualquiera de las reivindicaciones 11 a 15, que comprende la activaciïn del ïcido carboxïlico del hapteno y la reacciïn del hapteno activado con una proteïna.
17. Procedimiento segïn la reivindicaciïn 16, en donde la activaciïn del ïcido carboxïlico es mediada por un cloroformato de alquilo, por carbodiimida o por un ïster de Nhidroxisuccinimida.
18. Procedimiento segïn la reivindicaciïn 17, en donde el cloroformato de alquilo es el isobutilcloroformato.
19. Un anticuerpo que reconoce especïficamente un conjugado segïn cualquiera de las reivindicaciones 11 a 15.
20. Anticuerpo segïn la reivindicaciïn 19 que, adicionalmente, reconoce un agente anticoagulante de tipo cumarïnico.
21. Anticuerpo segïn cualquiera de las reivindicaciones anteriores 19 ï 20 que comprende una etiqueta detectable.
22. Un antisuero que comprende un anticuerpo segïn cualquiera de las reivindicaciones 19 a 21.
23. Uso de un anticuerpo segïn cualquiera de las reivindicaciones 19 a 21 o de un antisuero segïn la reivindicaciïn 22 o de un conjugado segïn cualquiera de las reivindicaciones 11 a 15 en la detecciïn y/o cuantificaciïn de anticoagulantes de tipo cumarïnico en una muestra de un sujeto.
24. Uso segïn la reivindicaciïn 23, en donde el sujeto estï bajo tratamiento con anticoagulantes de tipo cumarïnico.
25. Uso segïn cualquiera de las reivindicaciones 23 ï 24, en donde los anticoagulantes se seleccionan del grupo formado por warfarina, acenocumarol y fenprocumïn.
26. Uso segïn cualquiera de las reivindicaciones 23 a 25, en donde la muestra del sujeto es una muestra de plasma.
27. Mïtodo in vitro para la detecciïn y/o cuantificaciïn de agentes anticoagulantes de tipo cumarïnico en una muestra de un sujeto que comprende:
(i) poner en contacto dicha muestra con un anticuerpo segïn cualquiera de las reivindicaciones 19 a 21 o con un antisuero segïn la reivindicaciïn 22 o con un conjugado segïn cualquiera de las reivindicaciones 11 a 15, y
(ii) detectar la formaciïn de complejos anticoagulantes de tipo cumarïnicoanticuerpo segïn cualquiera de las reivindicaciones 19 a 21.
28. Mïtodo segïn la reivindicaciïn 27, en donde el sujeto estï bajo tratamiento con anticoagulantes de tipo cumarïnico.
29. Mïtodo segïn cualquiera de las reivindicaciones 27 ï 28, en donde la muestra del sujeto es una muestra de plasma.
30. Mïtodo segïn la reivindicaciïn 29, en donde la muestra de plasma es sometida a desproteinizaciïn.
31. Mïtodo segïn la reivindicaciïn 30, en donde la desproteinizaciïn se realiza mediante precipitaciïn con etanol.
32. Mïtodo segïn cualquiera de las reivindicaciones 27 a 31, en donde los anticoagulantes se seleccionan del grupo formado por warfarina, acenocumarol y fenprocumïn.
33. Mïtodo segïn la reivindicaciïn 32, en donde el agente anticoagulante es acenocumarol.
34. Mïtodo segïn la reivindicaciïn 32, en donde el agente anticoagulantes es warfarina.
35. Un kit para la detecciïn y o cuantificaciïn de agentes anticoagulantes de tipo
cumarïnico en una muestra de un sujeto que comprende al menos un anticuerpo segïn cualquiera de las reivindicaciones 19 a 21, un antisuero segïn la reivindicaciïn 22. o un conjugado segïn cualquiera de las reivindicaciïn 11 a 15.
36. Kit segïn la reivindicaciïn 35 en donde el anticuerpo estï inmovilizado sobre un 10 soporte sïlido.
37. Kit segïn la reivindicaciïn 35 en donde el conjugado estï inmovilizado sobre un soporte sïlido.
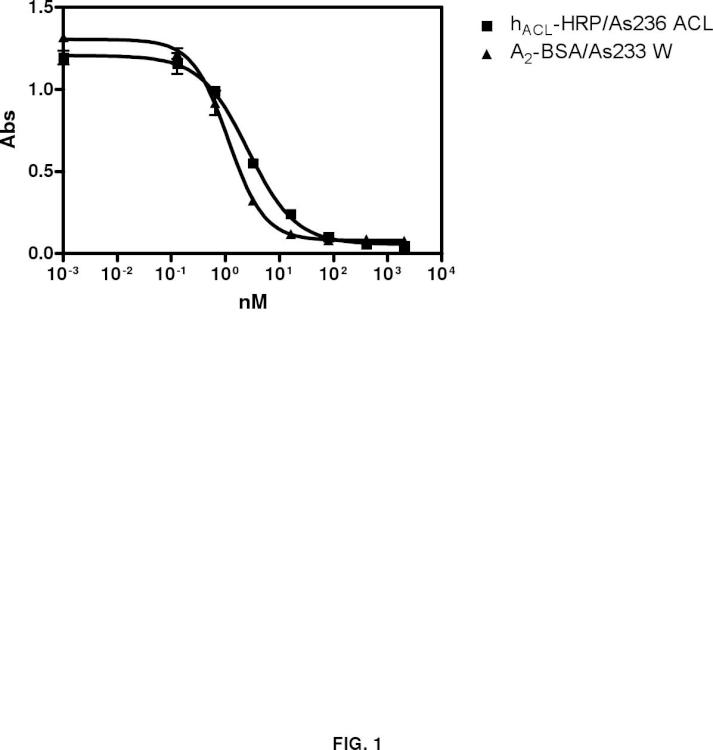
1.5
hACL-HRP/As236 ACL
A2-BSA/As233 W
1.0
0.5
0.0
FIG. 1
1.5
1.0
0.5
0.0
1.5
1.0
0.5
0.0
As236/hACL-HRP
A2-BSA/As233
Abs Abs FIG. 2
As236/hACL-HRP Tratamiento EtOH
10. 3 10-2 10-1 100 101 102 103 104 ACL nM
FIG. 3
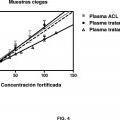
Muestras ciegas
Plasma ACL
Plasma tratam. EtOH ACL
Plasma tratam. EtOH W
Concentraciïn fortificada FIG. 4
IRACL, nM Abs PS-1PS-2PS-3PS-4PS-5PS-6PS-7PS-8PS-9PS-10PS-11PS-12PS-13PS-14
PS-51PS-52PS-53PS-54PS-55PS-56PS-57PS-58PS-59PS-60PS-61PS-62PS-63PS-64
PS-15PS-65PS-16PS-66PS-17PS-67PS-18PS-68PS-19PS-69PS-20PS-70PS-21PS-71PS-22PS-72PS-23PS-73PS-24PS-74PS-25PS-75PS-26PS-76PS-27PS-77PS-28PS-78PS-29PS-79PS-30PS-80PS-31PS-81PS-32PS-82
PS-33PS-34PS-35PS-36PS-37PS-38PS-39PS-40PS-41PS-42PS-43PS-44PS-45PS-46PS-47PS-48 PS-83PS-84PS-85PS-86PS-87PS-88PS-89PS-90PS-91PS-92PS-93PS-94PS-95PS-96PS-97PS-98
P ti Pacientes
FIG. 5
Patentes similares o relacionadas:
Derivados de piridina-3(2H)-ona en tanto que agentes de formación de imágenes para la detección de perfusión miocárdica, del 9 de Octubre de 2019, de LANTHEUS MEDICAL IMAGING, INC: compuesto A de la Fórmula (I): **Fórmula** o una sal farmacéuticamente aceptable del mismo, en donde: R1 se selecciona entre el […]
Compuestos como miméticos de hipoxia, y composiciones, y usos de estos, del 1 de Marzo de 2019, de Beijing Betta Pharmaceuticals Co., Ltd: Un compuesto de Fórmula I:**Fórmula** o una sal farmacéuticamente aceptable de este, solvato o quelato de este, en donde: n es de 1 a […]
USO DE MOLÉCULAS TRICOMONICIDAS, del 12 de Abril de 2018, de INSTITUTO POLITÉCNICO NACIONAL: Resumen. La presente invención describe nuevos compuestos químicos de fórmula (I) con estructura diferente a los nitroimidazoles, y sus usos igualmente novedosos para el […]
NUEVA COMPOSICIÓN PARA EL TRATAMIENTO DE LA TRICOMONIASIS, del 12 de Abril de 2018, de INSTITUTO POLITÉCNICO NACIONAL: La presente invención describe composiciones farmacéuticas útiles para el tratamiento de tricomoniasis que comprenden compuestos con la estructura […]
 Materiales poliméricos sólidos para la detección fluorogénica de explosivos nitroderivados y utilización de los mismos, del 28 de Julio de 2015, de UNIVERSIDAD DE BURGOS: Nuevos materiales poliméricos sólidos para la detección fluorogénica de explosivos nitroderivados basados en nuevos monómeros vinílicos derivados de la familia […]
Materiales poliméricos sólidos para la detección fluorogénica de explosivos nitroderivados y utilización de los mismos, del 28 de Julio de 2015, de UNIVERSIDAD DE BURGOS: Nuevos materiales poliméricos sólidos para la detección fluorogénica de explosivos nitroderivados basados en nuevos monómeros vinílicos derivados de la familia […]
ANTICUERPOS PARA LA DETECCIÓN Y CUANTIFICACIÓN DE AGENTES ANTICOAGULANTES, del 5 de Junio de 2014, de CENTRO DE INVESTIGACIÓN BIOMÉDICA EN RED EN BIOINGENIERÍA, BIOMATERIALES Y NANOMEDICINA: La presente invención se relaciona con el diseño de haptenos estructuralmente relacionados con compuestos anticoagulantes orales de tipo coumarínico (CAOC) con el objetivo […]
Compuestos rodenticidas, composición que los comprende y su utilización para luchar contra los roedores dañinos, del 9 de Abril de 2014, de LIPHATECH: Compuesto que responde a la fórmula (I): así como sus enantiómeros, diastereoisómeros, tautómeros o mezclas de estos últimos en cualquier proporción, en la […]
 MATERIALES Y METODOS PARA TRATAR TRASTORNOS DE COAGULACION, del 8 de Junio de 2010, de ARYX THERAPEUTICS: Compuesto de fórmula:
MATERIALES Y METODOS PARA TRATAR TRASTORNOS DE COAGULACION, del 8 de Junio de 2010, de ARYX THERAPEUTICS: Compuesto de fórmula: