Análogos de nitroimidazooxazina y sus usos.
Un compuesto que tiene una estructura general de fórmula I:**Fórmula**
en donde
n es 1,
V y W son independientemente H o CH3, y
uno de X o Y representa H y el otro representa uno de fórmula IIa o IIb, en donde las fórmulas IIa y IIb tienen las estructuras generales:**Fórmulas**
en donde la fórmula IIa comprende un solo anillo marcado en una posición 3 y una posición 4 y que tiene R1 como un sustituyente, y la fórmula IIb comprende un primer anillo marcado en una posición 3 y una posición 4 y que tiene como sustituyentes tanto R2 como un anillo terminal marcado en una posición 4 y que tiene R1 como un sustituyente, en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden C, CH o aza en cada posición de anillo, en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden independientemente como máximo dos aza,
Z en las fórmulas IIa y IIb representa CH2 o un enlace directo, y
R1 y R2 son independientemente uno cualquiera o dos de H, F, CI, I, CN, CF3, OCF3, OCH3, OCH2Ph.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/043908.
Solicitante: Global Alliance For Tb Drug Development.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 40 Wall Street, 24th Floor New York, NY 10005 ESTADOS UNIDOS DE AMERICA.
Inventor/es: THOMPSON, ANDREW, M., MA, ZHENKUN, DENNY, WILLIAM, ALEXANDER, BLASER,Adrian.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/424 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con sistemas heterocíclicos, p. ej. ácido clavulánico.
- A61K31/4439 A61K 31/00 […] › conteniendo un ciclo de cinco eslabones con el nitrógeno como heteroátomo del ciclo, p. ej. omeprazol (nicotina A61K 31/465).
- A61K31/497 A61K 31/00 […] › conteniendo otros heterociclos.
- A61K31/506 A61K 31/00 […] › no condensadas y conteniendo otros heterociclos.
- A61K31/5365 A61K 31/00 […] › condensadas en orto o en peri con sistemas heterocíclicos.
- A61P31/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para la tuberculosis.
- C07D498/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › Sistemas orto-condensados.
PDF original: ES-2530266_T3.pdf
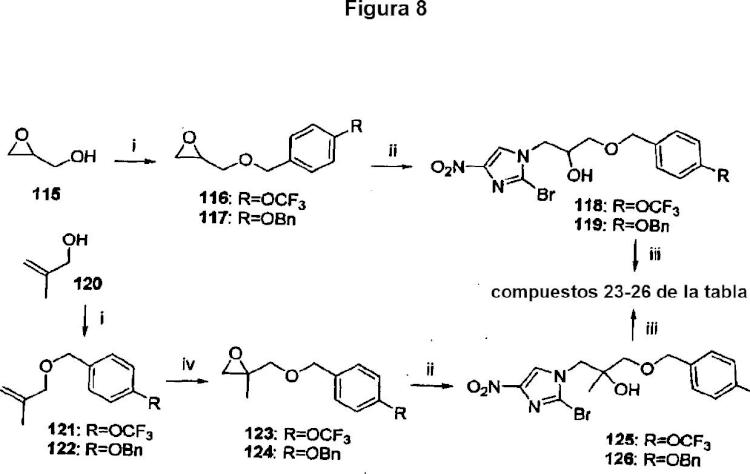
Fragmento de la descripción:
Análogos de nitroimidazooxazina y sus usos Antecedentes Esta solicitud reivindica prioridad respecto a la solicitud de patente provisional de EE.UU. nº de serie 61/230.422, titulada “Nitroimidazooxazine and Nitroimidazooxazole Analogues and Their Uses, ” presentada el 31 de julio, 2009,
La presente invención se refiere a análogos de nitroimidazooxazina, a su preparación y a su uso como fármacos eficaces contra Mycobacterium tuberculosis y como agentes antiprotozoarios, solos o en combinación con otros tratamientos.
La tuberculosis sigue siendo una causa de muerte por infección importante en todo el mundo (con una mortalidad calculada de 1, 3 millones en 2008) , con un resurgimiento reciente que se puede atribuir a una mayor susceptibilidad en paciente de VIH, así como a la incidencia creciente de cepas multirresistentes a fármacos y el surgimiento de cepas extensamente resistentes. La terapia con fármacos actual para la tuberculosis es larga y compleja, implicando combinaciones de multifármacos (normalmente isoniazida, rifampina, pirazinamida y etambutol) administrados diariamente durante más de 6 meses. Además, estos fármacos son relativamente ineficaces contra la forma persistente de la enfermedad, lo cual se sugiere que se produce en una proporción importante de los casos (Ferrara et al., 2006) . Los fármacos de segunda línea en terapias de combinación prolongadas para enfermedades multirresistentes a fármacos (típicamente a lo largo de 2 años) , la mayoría tienen una menor potencia o mayor toxicidad que los agentes de primera línea existentes. Con frecuencia se administra el tratamiento incompleto, conduciendo a tasas de recaída altas y mayor resistencia a fármacos, subrayando la necesidad urgente de nuevos fármacos más eficaces.
La enfermedad de Chagas afecta a aproximadamente 9 millones de persones, principalmente en Sudamérica, y produce aproximadamente 14.000 muertes anualmente. Es causada por el parásito protozoario Tr y panosoma cruzi, que es transmitido a seres humanos por insectos hematófogos. Los dos fármacos actualmente disponibles para el tratamiento, nifurtimox y benznidazol, muestran eficacia que está limitada a la fase aguda de la enfermedad y a solo a algunas cepas de patógenos. Estos fármacos también producen efectos secundarios graves, y esto, junto con el tratamiento prolongado y caro requerido, conduce al cumplimiento inadecuado del paciente y al desarrollo de resistencia a fármacos (Cavalli et al., 2009) .
La leishmaniasis afecta a casi 12 millones de personas en unos 90 países y produce aproximadamente 51.000 muertes anuales. Son particularmente prevalentes en el subcontinente indio y en Ã?frica del este, donde el agente causante es el parásito Leishmania donovani. Este parásito es transmitido a los seres humanos por la picadura de la hembra de la mosca de arena y es responsable de la forma más grave, la leishmaniasis visceral (kala-azar) , que produce enfermedad crónica en el hígado y bazo y es mortal salvo que se trata con quimioterapia. Los tratamientos de primera línea son los antimoniales antimoniato de meglumina (Glucantime) y estibogluconato de sodio (Pentostam) , descubiertos hace más de 50 años, que presentan efectos secundarios graves indeseables. Su administración en dosis bajas durante un periodo más largo ha dado como resultado el aumento de la resistencia al fármaco, de modo que ya no se pueden usar en la India (Cavalli et al., 2009) . Los agentes de segunda línea tienen problemas de toxicidad similares, lo que ilustra la necesidad real de tratamientos más seguros y más eficaces.
Por lo tanto, es muy deseable proporcionar nuevos análogos de nitroimidazooxazina con potencia inesperadamente alta tanto contra cultivos aerobios (que se multiplican) como hipóxicos (latentes o persistentes) de Mycobacterium tuberculosis, para usar como fármacos antituberculosos, y/o con potencia inesperadamente alta contra Tr y panosoma cruzi o Leishmania donovani, para usar como agentes antiprotozoarios, y para el tratamiento de otras infecciones microbianas.
Compendio La presente invención se refiere a análogos de nitroimidazooxazina, sus métodos de preparación y usos de los compuestos como tratamiento para Mycobacterium tuberculosis, para usar como fármacos antituberculosos, para usar como agentes antiprotozoarios con potencia inesperadamente alta contra Tr y panosoma cruzi o Leishmania donovani, y para el tratamiento de otras infecciones microbianas.
La introducción reciente de la nitroimidazooxazina PA-824 en ensayos clínicos es importante, ya que este compuesto presenta una buena actividad in vitro e in vivo contra Mycobacterium tuberculosis tanto en su forma activa como persistente (Tyagi et al., 2005) . Un 2-nitroimidazo[2, 1-b]oxazol relacionado, OPC-67683 también está en ensayos clínicos (Sasaki et al., 2006) . Las estructuras de estos compuestos se muestran en la figura 1. Sin querer estar ligados por la teoría, se sugiere que el mecanismo de acción de PA-824 implica la liberación de óxido nítrico (Singh et al., 2008) , después de una etapa reductora, en un proceso que depende de la glucosa-6-fosfato deshidrogenasa bacteriana (FGD1) y su cofactor F420 (Stover et al., 2000) . Estudios en micromatrices de cepas mutantes naturales tanto para FGD1 como F420 muestran que una proteína de 151 aminoácidos (17, 37 kDa) de función desconocida, Rv3547, parece que es crítica para su activación (Manjunatha et al., 2006) . Estudios mecanísticos recientes de química reductora de PA-824 apoyan este argumento (Anderson et al., 2008) . Los
análogos de nitroimidazooxazina y análogos de nitroimidazooxazol y sus usos en tuberculosis se han descrito previamente (patentes de EE.UU. nº 5.668.127 y 6.087.358; Jiricek et al., WO 2007075872A2; Li et al., 2008; Kim et al., 2009; Nagarajan et al., 1989; Ashtekar et al., 1993; Sasaki et al., 2006; Matsumoto et al., 2006; Tsubochi et al., WO 2005042542A1 y WO 2004033463A1; JP 2005330266A; EP 1555267A1) .
En un primer aspecto, la presente invención se refiere a un compuesto que tiene una estructura general de fórmula I:
en donde n es 1, V y W son independientemente H o CH3, y uno de X o Y representa H y el otro representa uno de fórmula IIa o IIb, en donde las fórmulas IIa y IIb tienen las estructuras generales:
en donde la fórmula IIa comprende un solo anillo marcado en una posición 3 y una posición 4 y que tiene R1 como un sustituyente, y la fórmula IIb comprende un primer anillo marcado en una posición 3 y una posición 4 y que tiene como sustituyentes tanto R2 como un anillo terminal marcado en una posición 4 y que tiene R1 como un sustituyente,
en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden C, CH o aza en cada posición de anillo, en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden independientemente como máximo dos aza,
Z en las fórmulas IIa y IIb representa CH2 o un enlace directo, y R1 y R2 representa cada uno, uno cualquiera o dos de H, F, CI, I, CN, CF3, OCF3, OCH3, OCH2Ph. Una subclase más preferida de compuestos incluye los que tienen una estructura general de fórmula I como se ha
definido antes, en donde: n es 1, V y W son independientemente H o CH3, y uno de X o Y representa H y el otro representa uno de fórmula IIa o IIb, en donde las fórmulas IIa y IIb tienen las
estructuras generales:
en donde la fórmula IIa comprende un solo anillo marcado en una posición 3 y una posición 4 y que tiene R1 como un sustituyente, y
la fórmula IIb comprende un primer anillo marcado en una posición 3 y una posición 4 y que tiene como sustituyentes tanto R2 como un anillo terminal marcado en una posición 4 y que tiene R1 como un sustituyente,
en donde el primer anillo de la fórmula IIb comprenden C, CH o aza en cada posición del anillo, en donde el primer anillo de la fórmula IIb comprende como máximo dos aza, y tanto el anillo único de la fórmula IIa como el anillo terminal de la fórmula IIb comprenden C o CH en cada posición del anillo cuando R1 no es 4-OMe, o comprende aza en la posición 3 y C o CH en cada posición restante del anillo cuando R1 es 4-OMe.
Z en las fórmulas IIa y IIb representa CH2 o un enlace directo, y
R1 representa 4-F, 4-CN, 4-I, 4-CF3, 3-OCF3, 4-OCF3, 4-OCH2Ph o 4-OMe, y
R2 representa H.
Estos compuestos, así como mezclas de los mismos y sales fisiológicamente funcionales de los mismos, son útiles para la prevención o terapia para tratar Mycobacterium tuberculosis, para usar como fármacos antituberculosos, para usar como agentes antiprotozoarios con potencia inesperadamente alta contra Tr y panosoma cruzi... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto que tiene una estructura general de fórmula I:
en donde n es 1, V y W son independientemente H o CH3, y uno de X o Y representa H y el otro representa uno de fórmula IIa o IIb, en donde las fórmulas IIa y IIb tienen las estructuras generales:
en donde la fórmula IIa comprende un solo anillo marcado en una posición 3 y una posición 4 y que tiene R1 como un sustituyente, y la fórmula IIb comprende un primer anillo marcado en una posición 3 y una posición 4 y que tiene como sustituyentes tanto R2 como un anillo terminal marcado en una posición 4 y que tiene R1 como un sustituyente,
en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden C, CH o aza en cada posición de anillo, en donde el anillo único de la fórmula IIa y el primer anillo y el anillo terminal de la fórmula IIb comprenden independientemente como máximo dos aza,
Z en las fórmulas IIa y IIb representa CH2 o un enlace directo, y
R1 y R2 son independientemente uno cualquiera o dos de H, F, CI, I, CN, CF3, OCF3, OCH3, OCH2Ph.
2. El compuesto de la reivindicación 1, en donde: n es 1, 20 V y W son independientemente H o CH3, y
uno de X o Y representa H y el otro representa uno de fórmula IIa o IIb, en donde las fórmulas IIa y IIb tienen las estructuras generales:
en donde la fórmula IIa comprende un solo anillo marcado en una posición 3 y una posición 4 y que tiene R1 como un sustituyente, y la fórmula IIb comprende un primer anillo marcado en una posición 3 y una posición 4 y que tiene como sustituyentes tanto R2 como un anillo terminal marcado en una posición 4 y que tiene R1 como un sustituyente,
en donde el primer anillo de la fórmula IIb comprenden C, CH o aza en cada posición del anillo, en donde el primer anillo de la fórmula IIb comprende como máximo dos aza, y tanto el anillo único de la fórmula IIa como el anillo terminal de la fórmula IIb comprenden C o CH en cada posición del anillo cuando R1 no es 4-OMe, o comprende aza en la posición 3 y C o CH en cada posición restante del anillo cuando R1 es 4-OMe.
Z en las fórmulas IIa y IIb representa CH2 o un enlace directo, y
R1 representa 4-F, 4-CN, 4-I, 4-CF3, 3-OCF3, 4-OCF3, 4-OCH2Ph o 4-OMe, y
R2 representa H.
3. Una composición farmacéutica que comprende una cantidad terapéuticamente eficaz del compuesto de la reivindicación 1.
4. La composición farmacéutica de la reivindicación 3, que además comprende un excipiente, adyuvante, vehículo, tampón, estabilizante farmacéuticamente activo, o una mezcla de los mismos.
5. La composición farmacéutica de la reivindicación 3, que además comprende uno o más tratamientos antiinfecciosos adicionales.
6. La composición farmacéutica de la reivindicación 3, para usar y tratar una infección microbiana.
7. La composición farmacéutica para usar según la reivindicación 6, en donde la infección microbiana es causada por Mycobacterium tuberculosis, Tr y panosoma cruzi o Leishmania donovani.
8. Un compuesto de la reivindicación 1, seleccionado del grupo que consiste en
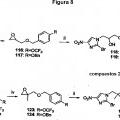
A. 2-Nitro-7-{[4- (trifluorometoxi) fenoxi]metil}-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
B. 7-{[4- (Benciloxi) fenoxi]metil}-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
C. 7-{[ (4′-Fluoro[1, 1′-bifenil]-4-il) oxi]metil}-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
D. 2-Nitro-7- ({[4′- (trifluorometil) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
E. 2-Nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
F. 7- ({[5- (4-Fluorofenil) -2-piridinil]oxi}metil) -2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
G. 2-Nitro-7-[ ({1-[4- (trifluorometoxi) fenil]-2-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
H. 7- ({[6- (4-Fluorofenil) -3-piridinil]oxi}metil) -2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
I. 2-Nitro-7-[ ({6-[4- (trifluorometoxi) fenil]-3-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
J. 7-Metil-2-nitro-7-{[4- (trifluorometoxi) fenoxi]metil}-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
K. 7-{[4- (Benciloxi) fenoxi]metil}-7-metil-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
L. 7-{[ (4′-Fluoro[1, 1′-bifenil]-4-il) oxi]metil}-7-metil-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
M. 7-Metil-2-nitro-7- ({[4′- (trifluorometil) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
N. 7-Metil-2-nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
O. 7- ({[5- (4-Fluorofenil) -2-piridinil]oxi}metil) -7-metil-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
P. 7-Metil-2-nitro-7-[ ({5-[4- (trifluorometil) fenil]-2-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
Q. 7-Metil-2-nitro-7-[ ({5-[4- (trifluorometoxi) fenil]-2-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
R. 7- ({[6- (4-Fluorofenil) -3-piridinil]oxi}metil) -7-metil-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
S. 7-Metil-2-nitro-7-[ ({6-[4- (trifluorometil) fenil]-3-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
T. 7-Metil-2-nitro-7-[ ({6-[4- (trifluorometoxi) fenil]-3-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
U. 2-Nitro-7- ({[3- (trifluorometoxi) bencil]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
V. 2-Nitro-7- ({[4- (trifluorometoxi) bencil]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
W. 7- ({[4- (Benciloxi) bencil]oxi}metil) -2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
X. 2-Nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-3-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
Y. 2-Nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
Z. 7-Metil-2-nitro-7- ({[3- (trifluorometoxi) bencil]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; AA. 7-Metil-2-nitro-7- ({[4- (trifluorometoxi) bencil]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; BB. 7- ({[4- (Benciloxi) bencil]oxi}metil) -7-metil-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
CC. 7-Metil-2-nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-3-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; DD. 7-Metil-2-nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; EE. (7R) -7-Metil-2-nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1
b][1, 3]oxazina;
FF. (7S) -7-Metil-2-nitro-7- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]metoxi}metil) -6, 7-dihidro-5H-imidazo[2, 1b][1, 3]oxazina; GG. 2-Nitro-6-{[4- (trifluorometoxi) fenoxi]metil}-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; HH. (6R) -2-Nitro-6-{[4- (trifluorometoxi) fenoxi]metil}-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
II. (6S) -2-Nitro-6-{[4- (trifluorometoxi) fenoxi]metil}-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
JJ. 6-{[ (4′-Fluoro[1, 1′-bifenil]-4-il) oxi]metil}-2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; KK. 2-Nitro-6- ({[4′- (trifluorometil) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; LL. 2-Nitro-6- ({[4′- (trifluorometoxi) [1, 1′-bifenil]-4-il]oxi}metil) -6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; MM. 6- ({[5- (4-Fluorofenil) -2-piridinil]oxi}metil) -2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; NN. 2-Nitro-6-[ ({5-[4- (trifluorometil) fenil]-2-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina;
OO. 2-Nitro-6-[ ({5-[4- (trifluorometoxi) fenil]-2-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; PP. 6- ({[6- (4-Fluorofenil) -3-piridinil]oxi}metil) -2-nitro-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; QQ. 2-Nitro-6-[ ({6-[4- (trifluorometil) fenil]-3-piridinil}oxi) metil]-6, 7-dihidro-5H-imidazo[2, 1-b][1, 3]oxazina; RR. 2-Nitro-6-
Patentes similares o relacionadas:
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Terapias de combinación para el cáncer, del 22 de Julio de 2020, de MERCK SHARP & DOHME CORP: Una combinación que comprende un anticuerpo anti-PD-1 humano y un Compuesto A y un Compuesto B, en donde: el anticuerpo anti-PD-1 humano comprende […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Formas en estado sólido de sales de Nilotinib, del 15 de Julio de 2020, de PLIVA HRVATSKA D.O.O: Una forma cristalina de fumarato de Nilotinib designada como Forma III, caracterizada por datos seleccionados de uno o más de los siguientes: a. un patrón de […]
Isotopólogos de 3-(5-amino-2-metil-4-oxoquinazolin-3(4H)-il) piperidina-2-6-diona y métodos de preparación de los mismos, del 15 de Julio de 2020, de CELGENE CORPORATION: Un compuesto de la fórmula: **(Ver fórmula)** o una sal farmacéuticamente aceptable, solvato o hidrato del mismo, en donde: por lo menos uno de Y1,Y2 e Y5 es […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]