Acetato de eslicarbazepina y su uso.
El uso de acetato de eslicarbazepina en la fabricación de una composición farmacéutica para el tratamiento del dolor neuropático diabético.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11174415.
Solicitante: BIAL - PORTELA & CA., S.A.
Nacionalidad solicitante: Portugal.
Dirección: Avenida da Siderurgia Nacional 4745-457 S. Mamede do Coronado PORTUGAL.
Inventor/es: VIEIRA ARAUJO SOARES DA SILVA, PATRICIO MANUEL, DE ALMEIDA,JOSÉ LUÍS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/55 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con siete eslabones, p. ej. azelastina, pentilentetrazol.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2534560_T3.pdf
Fragmento de la descripción:
Acetato de eslicarbazepina y su uso Antecedentes
La presente divulgación se refiere a una composición farmacéutica y a un método de tratamiento usando acetato de eslicarbazepina y en particular al uso del acetato de eslicarbazepina en la fabricación de una composición farmacéutica para el tratamiento del dolor neuropático diabético.
La epilepsia, los trastornos de dolor como la neuralgia del trigémino y los trastornos cerebrales afectivos tales como el trastorno bipolar se tratan frecuentemente con carbamazepina. El tratamiento con carbamazepina, sin embargo, puede dar lugar a efectos secundarios graves debido a la producción de metabolitos tóxicos. La oxcarbazepina se desarrolló para reducir la gravedad de estos efectos secundarios, pero la oxcarbazepina tiene una potencia muy reducida. Ver, por ejemplo, Almeida, L. & Soares-da-Silva, P., "Safety, Tolerability, and Pharmacokinetic Profile of BIA 2-093, a Novel Putative Antiepileptic, in a Rising Multiple-Dose Study in Young Healthy Humans", J. Clin. Pharmacol., 44, 906-918 (2004) (en lo sucesivo denominado "Almeida i).
Por lo tanto, hay una necesidad de una composición farmacéutica y un método para el tratamiento de diversos trastornos o enfermedades tales como, por ejemplo, epilepsia, neuralgia del trigémino y trastornos cerebrales afectivos, que tiene una alta potencia y una baja incidencia de efectos secundarios.
Sumario
El acetato de eslicarbazepina, (S)-(-)-10-acetoxi-10,11-dihidro-5H-dibenzo/b,f/azepina-5-carboxamida ("BIA 2-093"), es un nuevo medicamento en fase de desarrollo que es útil para el tratamiento de diversos trastornos, tales como, por ejemplo, la epilepsia y trastornos cerebrales afectivos, así como trastornos de dolor y alteraciones de la función nerviosa en enfermedades degenerativas y post-isquémicas. Aunque químicamente relacionada con la carbamazepina y la oxcarbazepina, se cree que el acetato de eslicarbazepina evita la producción de ciertos metabolitos tóxicos (tales como, por ejemplo, epóxidos) y evita la producción innecesaria de enantiómeros o diastereoisómeros de metabolitos y conjugados, sin perder actividad farmacológica. Ver Benes et al., J. Med "Anticonvulsant and Sodium Channel-Blocking Properties of Novel 10,11-Dihydro-5H-dibenz[b,f]azepine-5- carboxamide Derivatives", J. Med. Chem., 42, 2582-2587 (1999).
Al igual que la carbamazepina y la oxcarbazepina, se cree que el acetato de eslicarbazepina es un bloqueador del canal de sodio dependiente de voltaje (VGSC) que interactúa de manera competitiva con el sitio 2 del estado inactivado del canal de sodio. La afinidad por este estado del canal es similar a la de la carbamazepina, mientras que la afinidad por el estado de reposo del canal es aproximadamente 3 veces menor que la de la carbamazepina. Este perfil puede sugerir una selectividad inhibidora mejorada del acetato de eslicarbazepina para activar rápidamente neuronas respecto a las que presentan actividad normal. Ver Bonifacio y otros, "Interaction of the Novel Anticonvulsant, BIA 2-093, with Voltage-Gated Sodium Channels: Comparison with Carbamazepine", Epilepsia, 42, 600-608 (2001).
Se observó que la evaluación del perfil metabólico del acetato de eslicarbazepina, tras el análisis quiral, en microsomas de hígado de ratas, perros, monos y seres humanos daba el enantiómero S(+) de licarbazepina, (S)-(+)- 10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida (también conocida como "eslicarbazepina") y no la forma R(-) de licarbazepina, (R)-(-)-10,11-dihidro-10-hidroxi-5H-dibenz/b,f/azepina-5-carboxamida (también conocida como "R-licarbazepina").
Los estudios en humanos han demostrado que, después de la administración oral, el acetato de eslicarbazepina parece metabolizarse rápida y extensamente en el metabolito activo eslicarbazepina y, en una menor medida, en R- licarbazepina. Ver Silveira et al., "BIA 2-093 Pharmacokinetics in Healthy Elderly Subjects", Epilepsy, 45 (supl. 3), 157 (2004). Por ejemplo, las concentraciones plasmáticas del fármaco original (acetato de eslicarbazepina) se han observado sistemáticamente por debajo del límite de cuantificación (LC) del ensayo (10 ng/ml). Ver Almeida I; Almeida, L. & Soares-da-Silva, P., "Safety, Tolerability and Pharmacokinetic Profile of BIA 2-093, a Novel Putative Antiepileptic Agent, during First Administration to Humans", Drugs R&D, 4, 269-284 (2003) (en lo sucesivo denominado "Almeida lt). Cuando se utiliza un método no quiral, el ensayo no distingue entre eslicarbazepina y el enantiómero R y la mezcla se denominó "BIA 2-005" o "licarbazepina racémica".
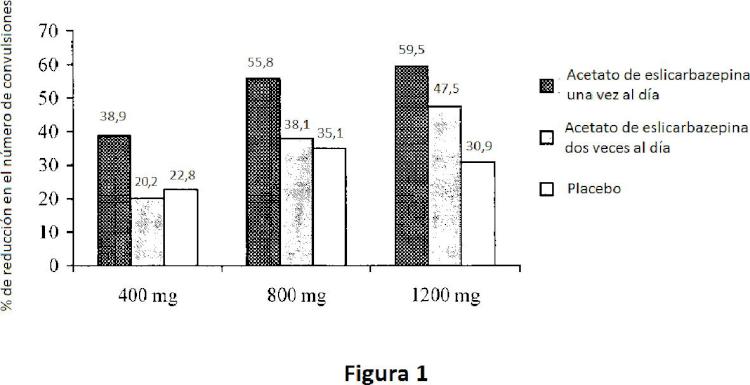
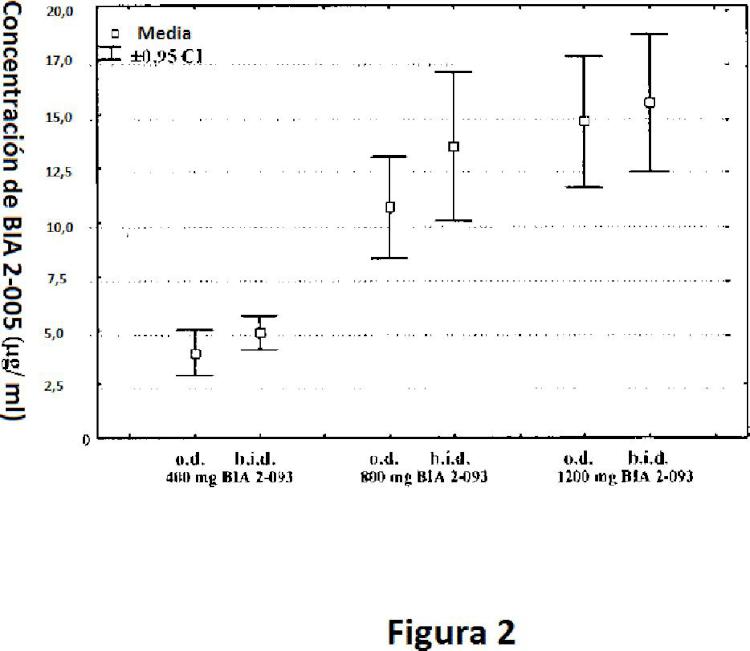
Los inventores llevaron a cabo estudios realizados por primera vez en el ser humano en sujetos sanos, cuyos resultados se describen en los artículos de Almeida I y Almeida II. En estos estudios, los sujetos sanos recibieron una dosis oral única de acetato de eslicarbazepina en el que la dosis varió de 20 mg a 1.200 mg (ver Almeida II) y dosis diarias múltiples de acetato de eslicarbazepina que van desde 200 mg dos veces al día a 1.200 mg una vez al día (ver Almeida I). Otros estudios (todavía no publicados) por los inventores han investigado dosis más altas de acetato de eslicarbazepina, incluyendo, por ejemplo, las dosis que van hasta 2.400 mg una vez al día. Los estudios mostraron que la concentración plasmática máxima (Cmax) observada de BIA 2-005 se alcanzó a aproximadamente 1
hora a aproximadamente 4 horas después de la dosis (tmax), el grado de exposición sistémica a BIA 2-005 fue aproximadamente proporcional a la dosis y las concentraciones plasmáticas en el estado estacionario de BIA 2-005 se alcanzó en aproximadamente de 4 a 5 días. La eliminación renal media de BIA 2-005 del plasma fue de aproximadamente 20-30 ml/min y la cantidad total de BIA 2-005 recuperada en la orina fue de aproximadamente 20 % y 40 % en el plazo de 12 horas y 24 horas después de la dosis, respectivamente.
Los estudios también demostraron que la semivida terminal aparente de BIA 2-005 variaba de aproximadamente 8 horas a aproximadamente 17 horas. Ver, por ejemplo, Almeida II.
La patente US-6.296.873 divulga un sistema de administración de liberación sostenida para la carbamazepina, que tiene una semivida que va desde 25 horas hasta 85 horas. Para evitar los efectos adversos, la patente US-6.296.873 enseña que la carbamazepina debe administrarse en forma de comprimidos hasta dos o más veces al día para liberar lentamente el compuesto para mantener los niveles de concentración entre 4-12 pg/ml. Un sistema de este tipo de administración requiere una forma que es capaz de administrar el compuesto durante un período de tiempo prolongado, tal como una forma de comprimido.
El documento WO 2004/071513 se refiere al uso de una mezcla de enantiómeros de licarbazepina para el tratamiento del dolor neuropático.
D. Hainzl et al. Epilepsy Research, 2001, vol.44, N2 2/03, 197-206, divulga un estudio para evaluar el metabolismo del acetato de eslicarbazepina y otro agente antiepiléptico, BIA-2 059.
E. Carrazana et al., Journal of Pain and Symptom Management, 2003, vol. 25, N2 5, S31-S35 se refiere a la justificación y pruebas para el uso de la oxcarbazepina en el tratamiento del dolor neuropático.
El documento EP 1477480A divulga un método para la racemización de (S)-(+)- y (R)-(-)-10,11 -dihidro-10-hidroxi-5H dibenz/b,f/azepina-5-carboxam¡da y mezclas ópticamente enriquecidas de los mismos.
El documento US 2004/038874 se refiere a un método para el tratamiento del dolor persistente mediante la inhibición de la inflamación usando, por ejemplo, un inhibidor de TNF-alfa.
J. Benes et al., J. Med. Chem., 1999, vol. 42, 2582-2587 divulga las propiedades de anticonvulsivo y de bloqueador de canal de sodio de una serie de derivados 10,11-dihidro-5H-dibenzo[b,f]azepina-5-carboxamida.
En un aspecto de la presente divulgación, los inventores han descubierto inesperadamente una mayor eficacia del acetato de eslicarbazepina en el tratamiento de diversos trastornos utilizando la administración una vez al día en comparación con la administración dos veces al día. Este descubrimiento es particularmente sorprendente porque la semivida aparente del acetato de eslicarbazepina (ti/2 = aproximadamente 8 horas a aproximadamente 17 horas) es significativamente más corta que la semivida de la carbamazepina (ti/2 = 25 horas a 85 horas), un compuesto que se administra normalmente 3-4 veces al día.
En otro aspecto de la presente divulgación, los inventores también han descubierto inesperadamente una mayor exposición a eslicarbazepina después de la administración una vez al día de acetato de eslicarbazepina en comparación con el régimen de dos veces al día en los seres humanos. La administración una vez al día de... [Seguir leyendo]
Reivindicaciones:
1. El uso de acetato de eslicarbazepina en la fabricación de una composición farmacéutica para el tratamiento del dolor neuropático diabético.
2. El uso de acuerdo con la reivindicación 1, en el que la composición farmacéutica es para administración una vez al día.
3. El uso de acuerdo con la reivindicación 2, en el que la dosis una vez al día se administra en una cantidad que da como resultado una concentración plasmática máxima observada, Cmax, de eslicarbazepina mayor de aproximadamente 7.400 ng/ml.
4. El uso de acuerdo con la reivindicación 3, en el que la dosis una vez al día se administra en una cantidad que da como resultado una Cmax de eslicarbazepina mayor de aproximadamente 12.000 ng/ml.
5. El uso de acuerdo con la reivindicación 2, en el que la dosis una vez al día se administra en una cantidad que da como resultado un área bajo la curva de concentración, AUC0-X, de eslicarbazepina mayor de aproximadamente 111.000 ng-h/ml, en el que x es el intervalo de administración.
6. El uso de acuerdo con la reivindicación 5, en el que la dosis una vez al día se administra en una cantidad que da como resultado una AUC0 xde eslicarbazepina mayor de aproximadamente 240.000 ng-h/ml.
7. El uso de acuerdo con una cualquiera de las reivindicaciones 2 a 5, en el que la dosis una vez al día se administra en una dosificación que comprende al menos aproximadamente 400 mg de acetato de eslicarbazepina.
8. El uso de acuerdo con la reivindicación 6, en el que la dosis una vez al día se administra en una dosificación que comprende al menos 800 mg de acetato de eslicarbazepina.
9. El uso de acuerdo con cualquier reivindicación anterior, en el que el principio activo en la composición farmacéutica consiste esencialmente en acetato de eslicarbazepina.
10. El uso de acuerdo con cualquier reivindicación anterior, en el que la composición farmacéutica se formula para administración oral.
11. El uso de acuerdo con cualquier reivindicación anterior, en el que la composición farmacéutica está en forma de comprimido.
12. El uso de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en el que la composición farmacéutica está en forma de suspensión oral.
13. El uso de acuerdo con la reivindicación 12, en el que la composición farmacéutica comprende al menos un excipiente, una sustancia auxiliar y/o un material vehículo.
14. El uso de acuerdo con la reivindicación 13, en el que el al menos un excipiente, una sustancia auxiliar y/o un material vehículo se seleccionan entre goma de xantano, estearato de macrogol, metilparabeno, propilparabeno, sacarina sódica, sorbitol, tampones, aromatizantes y combinaciones de los mismos.
Patentes similares o relacionadas:
Tratamientos de combinación que comprenden imidazopirazinonas para el tratamiento de trastornos psiquiátricos y/o cognitivos, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de Fórmula (I) **(Ver fórmula)** en donde n es 0 o 1; q es 0 o 1; R1 se selecciona del grupo que consiste en bencilo, indanilo, indolina y heteroarilos […]
Combinación de agonistas inversos del receptor de histamina-3 con inhibidores de acetilcolinesterasa, del 24 de Junio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un agonista inverso del receptor de histamina-3 y un inhibidor de acetilcolinesterasa; en donde el agonista inverso del receptor de histamina-3 […]
Amidas heterocíclicas como inhibidores de quinasa, del 3 de Junio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto que es **(Ver fórmula)** o un tautómero del mismo o una sal del mismo.
INHIBIDORES DE TGF-ß1 Y PRODUCTORES DE ENDOGLINA PARA SU USO EN EL TRATAMIENTO DE EPIDERMÓLISIS BULLOSA, del 14 de Mayo de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a un fármaco inhibidor de la ruta de TGF-ß1 y estimulador de endoglina o una composición farmacéutica del mismo, […]
Inhibidores de EZH2 (potenciador del homólogo Zeste 2), del 13 de Mayo de 2020, de Glaxosmithkline Intellectual Property (No. 2) Limited: Un compuesto según la Fórmula (I) o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la que: representa un enlace sencillo […]
INHIBIDORES DE TGF-ß1 Y PRODUCTORES DE ENDOGLINA PARA SU USO EN EL TRATAMIENTO DE EPIDERMÓLISIS BULLOSA, del 8 de Mayo de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Inhibidores de TGF-{beta}1 y productores de endoglina para su uso en el tratamiento de epidermólisis bullosa. La presente invención se refiere a un fármaco inhibidor […]
Benzazepinas fusionadas para el tratamiento de la tartamudez, del 29 de Abril de 2020, de Emalex Biosciences, Inc: Un antagonista selectivo para el receptor D1 y/o selectivo para D5 para su uso en el tratamiento de la tartamudez en un sujeto.
Compuesto de pirimidina condensado o sal del mismo, del 15 de Abril de 2020, de TAIHO PHARMACEUTICAL CO., LTD.: Un compuesto de pirimidina condensado representado por la siguiente fórmula (I): **(Ver fórmula)** en el que, en la fórmula, X representa un grupo […]