N,N",N"-TRIS(3-DIMETILAMINOPROPIL)GUANIDINA, PROCEDIMIENTO DE PREPARACION A PARTIR DE CARBODIIMIDA Y SU APLICACION EN REACCIONES DE TRANSESTERIFICACION DE ACEITES.
Preparación de N,N'',N''''-tris(3-dimetilaminopropil)guanidina que comprende la adición de 3-dimetilaminopropil-1-amina a N 1 ,
N 3 -bis(3-dimetilaminopropil)carbodiimida, caracterizada porque cada uno de los átomos de nitrógeno de la fracción guanidina está sustituido con un grupo 3-dimetilaminopropilo
Tipo: Resumen de patente/invención. Número de Solicitud: W05000026HR.
Solicitante: RUDJER BOSKOVIC INSTITUTE.
Nacionalidad solicitante: Croacia.
Dirección: BIJENICKA CESTA 54,HR-10002 ZAGREB.
Inventor/es: MAKSIC,MIRJANA, GLASOVAC,ZORAN.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- C07C277/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 277/00 Preparación de guanidina o sus derivados, es decir, de compuestos que contienen el grupo en que los átomos de nitrógeno unidos por enlaces sencillos no forman parte de grupos nitro o nitroso. › de guanidinas sustituidas.
Clasificación PCT:
- C07C277/08 C07C 277/00 […] › de guanidinas sustituidas.
- C07C279/12 C07C […] › C07C 279/00 Derivados de guanidina, es decir, compuestos que contienen el grupo en que los átomos de nitrógeno unidos por enlaces sencillos no forman parte de grupos nitro o nitroso. › que está sustituida por átomos de nitrógeno que no forman parte de grupos nitro o nitroso.
- C11C3/10 C […] › C11 ACEITES, GRASAS, MATERIAS GRASAS O CERAS ANIMALES O VEGETALES; SUS ACIDOS GRASOS; DETERGENTES; VELAS. › C11C ACIDOS GRASOS OBTENIDOS A PARTIR DE GRASAS, ACEITES O CERAS; VELAS; GRASAS, ACEITES O ACIDOS GRASOS OBTENIDOS POR MODIFICACION QUIMICA DE GRASAS, ACEITES O ACIDOS GRASOS. › C11C 3/00 Grasas, aceites o ácidos grasos obtenidos por modificación química de grasas, aceites o ácidos grasos, p. ej. por ozonólisis (grasas o aceites sulfonados C07C 309/62; grasas epoxidadas C07D 303/42; aceites vulcanizados, p.ej. pseudocaucho C08H 3/00). › por interesterificación.
Clasificación antigua:
- C07C277/08 C07C 277/00 […] › de guanidinas sustituidas.
- C07C279/12 C07C 279/00 […] › que está sustituida por átomos de nitrógeno que no forman parte de grupos nitro o nitroso.
- C11C3/10 C11C 3/00 […] › por interesterificación.
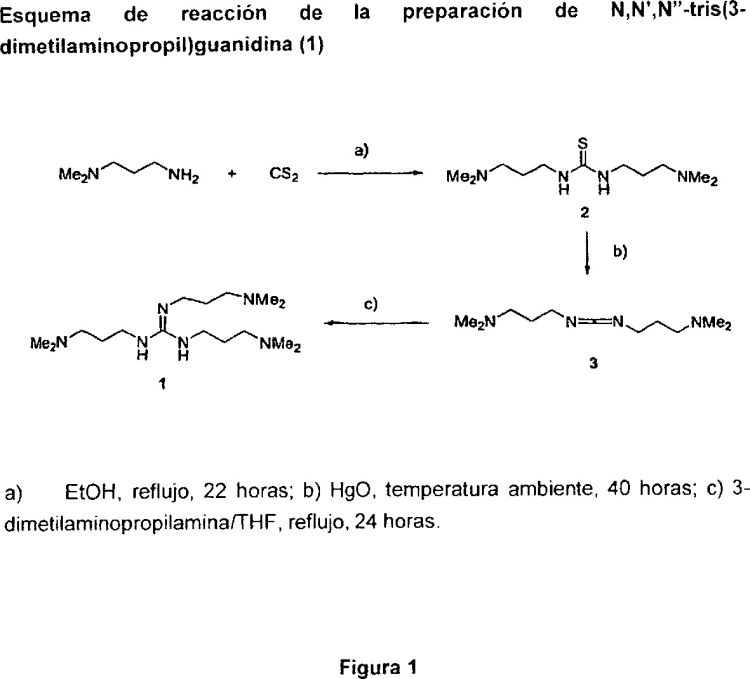
Fragmento de la descripción:
N,N',N''-tris(3-dimetilaminopropil)guanidina, procedimiento de preparación a partir de carbodiimida y su aplicación en reacciones de transesterificación de aceites.
La presente invención se refiere a la preparación de N,N',N''-tris(3-dimetilaminopropil)guanidina a partir de N1,N3-bis(3-dimetilaminopropil)carbodiimida y su utilización como catalizador para la transesterificación de aceites vegetales.
La transesterificación de aceites vegetales por medio de alcoholes orgánicos ligeros, tales como, por ejemplo, metanol o etanol, que proporciona una base para la producción tecnológicamente del importante combustible "BiodieselTM", se lleva a cabo habitualmente en presencia de catalizadores inorgánicos altamente básicos. Se revisan los procedimientos en F. Ma, M.A. Hanna, Biores. Technol. 1999, 70, 1-15. De entre ellos, el más activo es el metóxido de sodio que, sin embargo, no es adecuado para su uso industrial, ya que requiere condiciones de absoluta ausencia de agua (U. Schuchardt, R.M. Vargas, G. Gelbard, J. Mol. Catal. A: Chemical, 1995, 99, 65-70). Así, la mayoría de los procedimientos comerciales actualmente utilizados emplean hidróxido o carbonato de sodio o de potasio o una mezcla de estos compuestos, ya que son muy activos y relativamente baratos. Sin embargo, la eficacia de estos procesos depende de forma crítica de la presencia de ácidos libres en el aceite y del contenido de agua en el alcohol, lo que puede provocar una hidrólisis de los ésteres con formación posterior de jabones o emulsiones de la mezcla alcohol/aceite (F. Ma, M.A. Hanna, Biores. Technol. 1999, 70, 1-15; U. Schuchardt, R.M. Vargas, G. Gelbard, J. Mol. Catal. A: Chemical, 1995, 99, 65-70; G. Vicente, M. Martínez, J. Aracil, Biores. Technol. 2004, 92, 297-305).
En diversos documentos científicos ya publicados se discute la posibilidad de utilizar derivados de guanidina como catalizadores en la transesterificación de aceites vegetales (G. Gelbard, F. Vielfaure-Joly, React. Funct. Polym. 2001, 48, 65-74; G. Gelbard, F. Vielfaure-Joly, Tetrahedron Lett. 1998, 39, 2743-2746). La mayor parte de estos estudios se limitó al uso de derivados de guanidina penta-sustituida (G. Gelbard, F. Vielfaure-Joly, React. Funct. Polym. 2001, 48, 65-74; G. Gelbard, F. Vielfaure-Joly, Tetrahedron Lett. 1998, 39, 2743-2746; G. Gelbard, F. Vielfaure-Joly, React. Funct. Polym. 2001, 48, 65-74; U. Schuchardt, R.M. Vargas, G. Gelbard, J. Mol Catal. A: Chemical, 1996, 109, 37-44; G. Gelbard, F. Vielfaure-Joly, C.R. Acad. Sci. Paris, Ser. Ilc, Chimie/Chemistry, 2000, 3, 563-567) y biguanidinas polisustituidas (U. Schuchardt, R.M. Vargas, G. Gelbard, J. Mol. Catal. A: Chemical, 99 (1995) 65-70). Recientemente, se ha descrito el uso de ciertos derivados de guanidina unidos a un soporte de poliestireno (G. Gelbard, F. Vielfaure-Joly, React. Funct. Polym. 2001, 48, 65-74; U. Schuchardt, R.M. Vargas, G. Gelbard, J. Mol. Catal. A: Chemical, 1996, 109, 37-44; G. Gelbard, F. Vielfaure-Joly, C.R. Acad. Sci. París, Ser. Ilc, Chimie/Chemistry, 2000, 3, 563-567). Este primer trabajo proporcionó la firme evidencia de que la eficacia de la actividad catalítica de los derivados de la guanidina se incrementa con el aumento de la basicidad, así como con el aumento del número y la naturaleza de los sustituyentes en la fracción de guanidina. Entre las guanidinas tri-sustituidas, sólo se ha sometido a prueba hasta ahora, que se sepa, la actividad catalítica de la N,N,N'-triciclohexilguanidina y la N1,N3-diciclohexil-N2-n-octilguanidina.
Estudios teóricos recientes han demostrado que las guanidinas tri-sustituidas, con posibilidad de formar un enlace de hidrógeno intramolecular (IMHB) entre la subunidad de guanidina y el sustituyente de cadena lateral, por ejemplo la N,N',N''-tris(3-dimetilaminopropil)guanidina (1), que se prepara de acuerdo con la invención, poseen una basicidad intrínseca más alta que los derivados sin IMHB, convirtiéndolas en objetivos interesantes para investigar la actividad catalítica en la reacción de transesterificación. Por ejemplo, según los recientes cálculos ab initio, se descubrió que el compuesto 1 tenía una basicidad en fase gaseosa de 275 kcal/mol, mientras se preveía que su valor pKa en acetonitrilo era de 29. Ambos valores son más altos que los de los catalizadores de guanidina estudiados anteriormente (B. Kova
El objeto primario de esta invención consiste en la preparación de N,N',N''-tris(3-dimetilaminopropil)guanidina (1), que se prevé, según los cálculos, tiene una alta basicidad. El segundo objeto es la utilización de este nuevo derivado de guanidina tri-sustituida como catalizador en reacciones de transesterificación de aceites vegetales, tales como aceite de colza, de girasol y de soja.
La preparación de N,N',N''-tris(3-dimetilaminopropil)guanidina (1) descrita en esta solicitud de patente implica tres pasos, dos de los cuales han sido descritos anteriormente en la literatura: A.F. McKay, D.L. Garmaise, H. A. Baker, L.R. Hawkins, V. Falta, R. Gaudry, G.Y. Paris, J. Med. Chem. 1963, 6, 587-595, la desulfurización se desarrolló de acuerdo con J.C. Sheehan, P.A. Cruickshank, G.L. Boshart, J. Org. Chem. 1961, 26, 2525-2528. El primer paso incluye la preparación de N1,N3-bis(3-dimetilaminopropil)tiourea (2) a partir de 3-dimetilaminopropilamina y disulfuro de carbono. Posteriormente, la N1,N3-bis(3-dimetilaminopropil)tiourea se transforma en N1,N3-bis(3-dimetilaminopropil)-carbodiimida (3) mediante reacción con óxido de mercurio amarillo. El tercer paso, que representa el asunto de la presente invención, comprende la adición de 3-dimetilaminopropilamina a la N1,N3-bis(3-dimetilaminopropil)carbodiimida (3). Figura 1.
La actividad catalítica de la N,N',N''-tris(3-dimetilaminopropil)guanidina así obtenida se sometió a prueba en reacciones de transesterificación de aceites vegetales tal como se ilustra en los Ejemplos siguientes.
Otro objeto de la presente invención consiste en la transesterificación de aceite de colza, aceite de girasol, aceite de soja y otros aceites vegetales utilizando como catalizador la N,N',N''-tris(3-dimetilaminopropil)guanidina preparada de acuerdo con la presente invención.
Descripción detallada de la preparación de N,N',N''-tris(3-dimetilaminopropil)guanidina
Preparación de los materiales de partida
N1,N3-bis(3-dimetilaminopropil)tiourea (2)
A una solución de CS2 (6,0 cm3, 7,60 g, 0,100 mol) en 100 cm3 de etanol enfriado a aproximadamente 10ºC se añadió gota a gota 3-dimetilaminopropilamina (25,2 cm3, 20,50 g, 0,200 mol). Al finalizar la adición, la mezcla de reacción se llevó a reflujo durante 22 horas. El H2S desarrollado durante la reacción fue absorbido en NaOH acuoso diluido. Se eliminaron bajo presión reducida el disolvente y los compuestos volátiles. Se utilizó el aceite viscoso obtenido (20,5 g, 0,083 mol, rendimiento = 83%) en el siguiente paso sin más purificación. 1H NMR (CDCl3) d/ppm: 1,65-1,71 (m) 4H; 2,20 (s) 12H; 2,28-2,36 (m) 4H; 3,4 (multiplete ancho) 4H; 13C NMR (CDCl3) d/ppm: 25,8 (d); 40,6 (d); 45,0 (t); 57,8 (d); 181,3 (q).
N1,N3-bis(3-dimetilaminopropil)carbodiimida (3)
A una solución de la tiourea 2 (23,04 g, 0,094 mol) en 150 cm3 de CH2Cl2 previamente secado en CaH2 se añadió HgO amarillo (80,0 g, 0,369 mol) de una sola vez. La mezcla heterogénea se agitó durante 22 horas a temperatura ambiente, luego se añadió una segunda porción de HgO amarillo (20,0 g, 0,092 mol) y se continuó la agitación durante 18 horas más. Después, se enfrió la mezcla de reacción a temperatura ambiente, se filtró y se evaporó el disolvente a presión reducida. El producto aceitoso se destiló a 0,1 Pa (10-4 mm de Hg) manteniendo la temperatura del baño de aceite por debajo de 100ºC. El análisis por GLC del destilado incoloro mostró la presencia de la carbodiimida 3 como un producto único (7,33 g, 0,035 mol, rendimiento = 37%, p.eb. = 48-50ºC/3 x 10-4 mm de Hg). GC-MS (M+ m/z = 212); IR (KBr) (v/cm-1 = 2130, N=C=N);...
Reivindicaciones:
1. Preparación de N,N',N''-tris(3-dimetilaminopropil)guanidina que comprende la adición de 3-dimetilaminopropil-1-amina a N1,N3-bis(3-dimetilaminopropil)carbodiimida, caracterizada porque cada uno de los átomos de nitrógeno de la fracción guanidina está sustituido con un grupo 3-dimetilaminopropilo.
2. Transesterificación de aceite de colza, aceite de girasol, aceite de soja y otros aceites vegetales en metanol, caracterizada porque la N,N',N''-tris(3-dimetilaminopropil)guanidina preparada según la reivindicación 1 se utiliza como catalizador.
Patentes similares o relacionadas:
Método para preparar D-arginina, del 27 de Noviembre de 2019, de Aminologics Co., Ltd: Método de preparación de D-arginina, que comprende las etapas de: depositar una sal de ácido D-3-bromocanfor-8-sulfónico de D-arginina mediante la resolución […]
Procedimiento para producir sales de biguanida y s-triazinas, del 24 de Abril de 2019, de BAYER CROPSCIENCE AKTIENGESELLSCHAFT: Procedimiento para producir sales de biguanidina de fórmula (III), que está caracterizado porque a) se convierte una amina de fórmula (I) en una sal […]
Procedimiento para la preparación de poliguanidinas, del 7 de Febrero de 2019, de Sealife Pharma GmbH: Procedimiento para la preparación de productos de policondensación de guanidina, aminoguanidina o diaminoguanidina G con uno o varios derivados de […]
Método para preparar ésteres grasos de creatina, ésteres grasos de creatina preparados de este modo y usos de los mismos, del 8 de Junio de 2016, de COMMISSARIAT A L'ENERGIE ATOMIQUE ET AUX ENERGIES ALTERNATIVES: Método para preparar un éster graso de creatina o derivado del mismo que comprende al menos una etapa que consiste en hacer reaccionar una creatinina […]
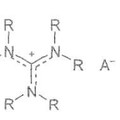 Proceso para preparar sales de guanidinio, del 21 de Octubre de 2013, de MERCK PATENT GMBH: Proceso para preparar sales de guanidinio de la fórmula **Fórmula**
donde los sustituyentes R tiene respectivamente, independientemente entre sí, […]
Proceso para preparar sales de guanidinio, del 21 de Octubre de 2013, de MERCK PATENT GMBH: Proceso para preparar sales de guanidinio de la fórmula **Fórmula**
donde los sustituyentes R tiene respectivamente, independientemente entre sí, […]
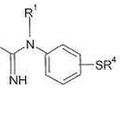 Alquiltiofenil guanidinas marcadas con 18F o 11C para obtención de imágenes médicas, del 16 de Octubre de 2013, de HAMMERSMITH IMANET, LTD: Un compuesto de fórmula (I):**Fórmula**
o una sal o solvato del mismo, en donde:
R1 es hidrógeno o alquilo C1-4;
R2 y R4 se seleccionan […]
Alquiltiofenil guanidinas marcadas con 18F o 11C para obtención de imágenes médicas, del 16 de Octubre de 2013, de HAMMERSMITH IMANET, LTD: Un compuesto de fórmula (I):**Fórmula**
o una sal o solvato del mismo, en donde:
R1 es hidrógeno o alquilo C1-4;
R2 y R4 se seleccionan […]
Procedimiento para producir 1-(3,4-diclorobencil)-5-octilbiguanida o una sal de la misma, del 9 de Septiembre de 2013, de OTSUKA PHARMACEUTICAL CO., LTD.: Procedimiento para producir 1-(3,4-diclorobencil)-5-octilbiguanida representada por la fórmula :**Fórmula** o una sal de la misma, comprendiendo […]
Compuestos orgánicos, del 16 de Mayo de 2012, de NOVARTIS AG: Mesilato de casmostato, o un solvato del mismo, para el tratamiento de fibrosis quística.