Procedimiento para la preparación de lercanidipina amorfa.
Un procedimiento para preparar lercanidipina amorfa que comprende las etapas de:
(1) disolver lercanidipina en un disolvente orgánico para preparar una solución;
(2) formar precipitados vertiendo la solución en un disolvente orgánico seleccionado del grupo constituido por ciclohexano, ciclopentano, hexano y éter de petróleo y agitando; y
(3) filtrar los precipitados, lavar con el disolvente orgánico usado en la etapa 2 y secar al vacío.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/KR2005/003576.
Solicitante: RECORDATI IRELAND LIMITED.
Inventor/es: CHOO,SO MI, HA,HONG JOO, AN,JUNG GI, LEE,WON JUNG, LEE,S. G, BYUN,YOUNG-SEOK, MOON,YOUNG IL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D211/90 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 211/00 Compuestos heterocíclicos que contienen ciclos hidrogenados de piridina, no condensados con otros ciclos. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo sumo un enlace a halógeno.
PDF original: ES-2546930_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de lercanidipina amoría.
Campo técnico
La presente invención versa sobre un procedimiento para preparar lercanidipina amoría y, más en particular, sobre un procedimiento para preparar una lercanidipina amoría que tiene una solubilidad y una biodisponibilidad 5 superiores, de gran pureza y rendimiento, controlando los disolventes fundamentales y su proporción volumétrica durante la preparación.
Técnica antecedente La lercanidipina [metil-1, 1, N-trimetil-N- (3, 3-difenilpropil) -2-aminoetil-1, 4-dihidro-2, 6-dimetil-4- (3-nitrofenil) piridina-3, 5-dicarboxilato] y, especialmente, su sal de clorhidrato son uno de los agentes terapéuticos más recientes para la 10 hipertensión. Son calcioantagonistas (bloqueadores de los canales de calcio) sumamente lipófilos de la dihidropiridina que tienen gran selectividad de los vasos sanguíneos y presentan una acción de larga duración. Provocan la vasodilatación de los vasos sanguíneos y menor presión sanguínea al actuar en los canales de calcio de las membranas celulares de los vasos sanguíneos. Los calcioantagonistas suprimen la fuerza contráctil del corazón y disminuyen la frecuencia de latido del mismo al actuar en los canales de calcio del corazón. Los 15 calcioantagonistas muestran diferencias en las propiedades farmacocinéticas y farmacológicas porque diversos tipos de calcioantagonistas tienen diferentes propiedades fisicoquímicas.
En comparación con otros calcioantagonistas, la lercanidipina presenta una acción de larga duración a pesar de una aparición y una disminución graduales en su concentración en el plasma sanguíneo. Según experimentos in vitro, incluso después de la supresión de una medicina de la periferia del tejido aórtico, la lercanidipina debilita la reacción 20 al ion K+ de la aorta de rata que lleva 6 horas separada.
La patente estadounidense nº 4.705.797 dio a conocer que la lercanidipina es un antagonista de los canales de calcio de tipo T y un material usado para el tratamiento de las anginas (tales como en la amigdalitis de garganta) , de la hipertensión y de la enfermedad arterial coronaria.
Los procedimientos de preparación de la lercanidipina son dados a conocer en las patentes estadounidenses nos 25 5.767.136, 4.968.832 y 5.696.139.
En la patente estadounidense nº 5.912.351 se da a conocer un procedimiento de preparación de la lercanidipina más mejorado como sigue: se halogena ácido 2, 6-dimetil-5-metoxicarbonil-4- (3-nitrofenil) -1, 4-dihidropiridina-3-carboxílico por medio de un halogenante en un disolvente aprótico y se añade 2, N-dimetil-N- (3, 3-difenilpropil) -1-amino-2-propanol disuelto en disolvente aprótico al ácido halúrico preparado para sintetizar la lercanidipina como un 30 clorhidrato anhidro.
La lercanidipina se clasifica en los tipos cristalinos I, II, III y IV según la posición y la intensidad de los picos en la difracción de rayos X (DRX) , y también existe como forma amoría carente de picos en la DRX.
La solicitud de patente coreana nº 2004-7001558 da a conocer una forma en bruto de clorhidrato de lercanidipina y un procedimiento de preparación de formas cristalinas novedosas de (I) y (II) . 35
Además, la solicitud de patente coreana nº 2004-7001791 (patente europea nº 1423367) da a conocer procedimientos de síntesis de formas cristalinas novedosas de (III) y (IV) y composiciones farmacéuticas que contienen al menos una de las formas cristalinas novedosas de (III) y (IV) .
En muchas composiciones farmacéuticas, se sabe de forma generalizada que la forma amoría tiene una solubilidad y una biodisponibilidad diferente de una forma cristalina. 40
Entre los indicadores terapéuticos, la biodisponibilidad es uno de los parámetros más importantes para determinar una forma de una sustancia usada para una formulación farmacéutica.
Generalmente, la solubilidad de una forma cristalina en un organismo es menor que la de una forma amoría. El clorhidrato lercanidipina tiene una hidrosolubilidad sumamente baja, y su forma cristalina tiene una solubilidad menor que la forma amoría del mismo, y, por lo tanto, puede causar problemas en la biodisponibilidad de la lercanidipina. 45 Además, una forma amoría causa graves problemas de filtrado, porque la forma amoría tiene un tamaño de partícula pequeño y gran área superficial.
Así, los inventores han completado un procedimiento para preparar un compuesto novedoso de lercanidipina amoría que no pertenece a las formas cristalinas de (I) , (II) , (III) o (IV) . La solubilidad, la biodisponibilidad y la propiedad de filtrado pueden ser mejoradas transformando una forma cristalina de la lercanidipina en una forma amoría. 50
Divulgación de la invención Problema técnico Un objeto de la presente invención es proporcionar un procedimiento para preparar lercanidipina amoría que tiene una solubilidad, una biodisponibilidad y una propiedad de filtrado excelentes.
Solución técnica Para lograr el objeto anterior, la presente invención proporciona un procedimiento para preparar lercanidipina amoría 5 que comprende las etapas de: (1) disolver lercanidipina en un disolvente orgánico para preparar una solución; (2) formar precipitados vertiendo la solución en un disolvente orgánico seleccionado del grupo constituido por ciclohexano, ciclopentano, hexano y éter de petróleo y agitando; y (3) filtrar los precipitados, lavar los precipitados con el disolvente orgánico usado en la etapa (2) y secar al vacío.
La presente invención proporciona otro procedimiento para preparar lercanidipina amoría que comprende las etapas 10 de: (1) disolver lercanidipina en al menos un disolvente orgánico seleccionado del grupo constituido por dimetilsulfóxido, dimetilformamida, 1, 4-dioxano y metanol, y enfriar hasta 0°C; (2) formar precipitados añadiendo agua a 0 ~ 5°C y agitando; y (3) filtrar los precipitados, lavar los precipitados con agua y secar al vacío.
La presente invención proporciona otro procedimiento para preparar lercanidipina amoría que comprende las etapas de: (1) disolver lercanidipina en metanol y añadir éter diisopropílico para obtener una solución diluida; (2) formar 15 precipitados añadiendo la solución en éter diisopropílico y agitando; y (3) filtrar los precipitados, lavar los precipitados con éter diisopropílico y secar al vacío.
En lo que sigue, la presente invención será descrita en detalle. Un procedimiento para preparar lercanidipina amoría según la presente invención comprende las etapas de: (1) disolver lercanidipina en un disolvente orgánico para preparar una solución; (2) formar precipitados vertiendo la solución en un disolvente orgánico seleccionado del grupo 20 constituido por ciclohexano, ciclopentano, hexano y éter de petróleo y agitando; y (3) filtrar los precipitados, lavar los precipitados con el disolvente orgánico usado en la etapa (2) y secar al vacío.
En la etapa (1) de la presente invención, se usa el disolvente orgánico para disolver uniformemente la lercanidipina. Como ejemplos, pueden usarse como disolvente orgánico un disolvente orgánico mixto de cloruro de metileno y alcohol t-butílico o un disolvente orgánico mixto de tetrahidrofurano y alcohol t-butílico. Cuando se usa el disolvente 25 orgánico mixto de cloruro de metileno y alcohol t-butílico, la lercanidipina se disuelve en el disolvente orgánico mixto con un volumen de 4 a 10 veces el de la lercanidipina, preferentemente en el disolvente orgánico mixto con un volumen 6 veces el de la lercanidipina, y luego, en la etapa (2) , se vierte la solución en ciclohexano con un volumen de 15 a 40 veces el del cloruro de metileno, preferentemente en ciclohexano con un volumen 20 veces el del cloruro de metileno. 30
La etapa (1) de la presente invención puede comprender las etapas adicionales de: disolver uniformemente lercanidipina en al menos un disolvente orgánico seleccionado del grupo constituido por metanol, etanol y cloruro de metileno para preparar una solución; evaporar la solución para obtener una sustancia sólida; y disolver la sustancia sólida en tetrahidrofurano. El volumen de tetrahidrofurano es, preferentemente, de 5 a 10 veces el volumen de lercanidipina usado, más preferentemente 8 veces. Se obtiene la forma amoría de la lercanidipina mediante la 35 adición de tetrahidrofurano con un volumen más de 5 veces el de la lercanidipina. Sin embargo, el uso de tetrahidrofurano con un volumen más de 10 veces el de la lercanidipina no es rentable, porque la producción no aumenta significativamente a pesar del mayor uso de tetrahidrofurano.
En la etapa (2) de la presente invención, el volumen de un disolvente orgánico seleccionado del grupo constituido 40 por ciclohexano,... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para preparar lercanidipina amoría que comprende las etapas de:
(1) disolver lercanidipina en un disolvente orgánico para preparar una solución;
(2) formar precipitados vertiendo la solución en un disolvente orgánico seleccionado del grupo constituido por 5 ciclohexano, ciclopentano, hexano y éter de petróleo y agitando; y
(3) filtrar los precipitados, lavar con el disolvente orgánico usado en la etapa 2 y secar al vacío.
2. El procedimiento de la reivindicación 1 en el que el disolvente orgánico de la etapa (1) es una solución mixta de cloruro de metileno y alcohol t-butílico o una solución mixta de tetrahidrofurano y alcohol t-butílico. 10
3. El procedimiento de la reivindicación 1 en el que la etapa (1) comprende, además, las etapas de: disolver la lercanidipina en al menos un disolvente orgánico seleccionado del grupo constituido por metanol, etanol y cloruro de metileno para preparar una solución; evaporar la solución para obtener una sustancia sólida; y disolver la sustancia sólida en tetrahidrofurano.
4. El procedimiento de la reivindicación 3 en el que el volumen del tetrahidrofurano es de 5 a 10 veces el volumen 15 de la lercanidipina.
5. El procedimiento de la reivindicación 1 en el que el volumen del disolvente orgánico usado en la etapa (2) es de 5 a 40 veces el volumen del disolvente usado para disolver la lercanidipina.
6. El procedimiento de la reivindicación 1 en el que el disolvente orgánico de la etapa (1) es un disolvente orgánico mixto de cloruro de metileno y alcohol t-butílico, siendo el volumen del disolvente orgánico mixto de 4 a 10 veces el 20 volumen de la lercanidipina; el disolvente orgánico de la etapa (2) es ciclohexano, con un volumen de 15 a 40 veces el volumen del disolvente orgánico de la etapa (1) ; y el secado al vacío de la etapa (3) tiene lugar a 60 ~ 80°C durante 24 ~ 30 horas.
7. El procedimiento de las reivindicaciones 1 o 6 en el que el vertido de la etapa (2) se lleva a cabo a 0°C.
8. Un procedimiento para preparar lercanidipina amoría que comprende las etapas de: 25
(1) disolver lercanidipina en al menos un disolvente orgánico seleccionado del grupo constituido por dimetilsulfóxido, dimetilformamida, 1, 4-dioxano y metanol, y enfriar hasta 0°C;
(2) formar precipitados añadiendo agua a 0 ~ 5°C y agitando; y
(3) filtrar los precipitados, lavar con agua y secar al vacío.
9. El procedimiento de la reivindicación 8 en el que el volumen del disolvente orgánico de la etapa (1) es de 2 a 5 veces el volumen de la lercanidipina.
10. El procedimiento de la reivindicación 8 en el que el volumen del agua de la etapa (2) es de 15 a 30 veces el volumen del disolvente orgánico usado para disolver la lercanidipina. 35
11. Un procedimiento para preparar lercanidipina amoría que comprende las etapas de:
(1) disolver lercanidipina en metanol y añadir éter diisopropílico para obtener una solución diluida;
(2) formar precipitados añadiendo la solución en éter diisopropílico y agitando; y
(3) filtrar los precipitados, lavar con éter diisopropílico y secar al vacío.
12. El procedimiento de la reivindicación 11 en el que el volumen del éter diisopropílico de la etapa (3) es de 30 a 50 veces el volumen de la lercanidipina.
Patentes similares o relacionadas:
DERIVADOS DE 4-FENILDIHIDROPIRIDINA PARA EL TRATAMIENTO Y/O PREVENCIÓN DE UNA INFECCIÓN O ENFERMEDAD CAUSADA POR HELICOBACTER, del 23 de Abril de 2020, de FUNDACION INSTITUTO DE INVESTIGACION SANITARIA ARAGON: Derivados de 4-fenildihidropiridina de fórmula I y composiciones farmacéuticas de los mismos, donde el significado para R1, R2, […]
Derivados de 4-fenildihidropiridina para el tratamiento y/o prevención de una infección o enfermedad causada por Helicobacter, del 20 de Abril de 2020, de FUNDACION INSTITUTO DE INVESTIGACION SANITARIA ARAGON: Derivados de 4-fenildihidropiridina para el tratamiento y/o prevención de una infección o enfermedad causada por Helicobacter. Derivados de 4-fenildihidropiridina de fórmula […]
Clorhidrato de lercanidipino amorfo, del 13 de Noviembre de 2019, de RECORDATI IRELAND LIMITED: Hidrocloruro de lercanidipino amorfo que presenta una pureza de por lo menos el 95%.
Aril dihidropiridinonas y piperidinonas como inhibidores de MGAT2, del 13 de Febrero de 2019, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Formula (I):**Fórmula** o un estereoisomero, un tautomero o una sal farmaceuticamente aceptable, en la que: indica un enlace simple […]
Arilhidrazidas que contienen una fracción de 2-piridona como agentes antibacterianos selectivos, del 29 de Octubre de 2018, de ABAC THERAPEUTICS, S.L: Un compuesto de la fórmula (I): **Fórmula** una sal, solvato, isótopo, polimórfo o tautómero farmacéuticamente aceptable del mismo, en donde A es […]
Aril dihidropiridinonas y piperidinonas como inhibidores de MGAT2, del 18 de Mayo de 2016, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Formula (I):**Fórmula** o un estereoisomero, un tautomero, una sal farmaceuticamente aceptable o un solvato del mismo, en la que: […]
Preparación de dihidropiridinas, del 10 de Febrero de 2016, de LABORATORIOS LESVI, S.L.: Un proceso para la preparación de butirato de clevidipina que comprende la etapa: (i) hacer reaccionar un compuesto de fórmula (I): **Fórmula** […]
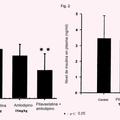 Agente reductor de triglicéridos y agente de mejora del hiperinsulinismo, del 8 de Febrero de 2016, de KOWA COMPANY LTD.: Uso de un compuesto de pitavastatina y amlodipino o una sal del mismo para
- producir un agente reductor de triglicéridos o
- para producir un agente preventivo y/o terapéutico […]
Agente reductor de triglicéridos y agente de mejora del hiperinsulinismo, del 8 de Febrero de 2016, de KOWA COMPANY LTD.: Uso de un compuesto de pitavastatina y amlodipino o una sal del mismo para
- producir un agente reductor de triglicéridos o
- para producir un agente preventivo y/o terapéutico […]