Nanofiltración de soluciones del factor VII para eliminar virus.
Un método para retirar virus de una composición líquida del factor VII recombinante,
donde dicha composición comprende uno o más polipéptidos del factor VII, donde la concentración de los polipéptidos del factor VII está comprendida en el intervalo de 0.01 a 5 mg/mL y donde la forma activada de los polipéptidos del factor VII representa un 50-100% de la masa del polipéptido o de los polipéptidos del factor FVII en la composición;
donde dicho método comprende someter dicha solución a nanofiltración utilizando un nanofiltro que tiene un tamaño de poro de 80 nm como máximo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/053206.
Solicitante: NOVO NORDISK HEALTH CARE AG.
Nacionalidad solicitante: Suiza.
Dirección: Thurgauerstrasse 36/38 8050 Zürich SUIZA.
Inventor/es: HANSEN,THOMAS BUDDE, CHRISTENSEN,JESPER, HALKJAER,ERIK, PREUSS,TURID, TOMODA,LENE VAEDELE MADSEN, JOHANSEN,NINA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K1/34 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › por filtración, ultrafiltración u ósmosis inversa.
- C07K14/745 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factores de coagulación sanguínea o de fibrinolisis.
- C12N7/06 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › por tratamiento químico.
- C12N9/64 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › que provienen de tejido animal, p. ej. renina.
PDF original: ES-2507091_T3.pdf
Fragmento de la descripción:
Nanofiltración de soluciones del factor Vil para eliminar virus
La presente invención se refiere a un método novedoso para mejorar la seguridad viral de composiciones líquidas del factor Vil que comprenden polipéptidos del factor Vil activos (un polipéptido del factor VIla).
ANTECEDENTES DE LA INVENCIÓN
Se han identificado una serie de factores que participan en el proceso de coagulación sanguínea, incluido el factor Vil (FVII), una glucoproteína plasmática. La hemostasia se inicia por la formación de un complejo entre el factor tisular (TF, por sus siglas en inglés), cuando este se expone a la sangre circulante tras una herida en la pared del vaso, y el factor Vlla que está presente en la circulación en una cantidad correspondiente a aproximadamente un 1% de la masa proteica del factor Vil total. El factor Vil existe en el plasma principalmente como un zimógeno monocatenario al que FXa escinde en su forma activada bicatenaria, el factor Vlla. El factor Vlla activado recombinante (rFVIIa) se ha desarrollado como un agente prohemostásico. La administración de rFVIIa ofrece una respuesta prohemostásica rápida y sumamente eficaz en los sujetos hemofílicos con hemorragias a los que no se puede tratar con otros productos de factores de la coagulación debido a la formación de anticuerpos. Asimismo, la hemorragia en sujetos con una deficiencia en el factor Vil o sujetos que tienen un sistema de coagulación normal pero que experimentan una hemorragia excesiva se pueden tratar con éxito con el factor Vlla.
La purificación y manipulación del factor Vil debe ser cuidadosa, debido a la posibilidad de degradación de la molécula. El factor Vil y el factor Vlla, que son moléculas grandes (peso molecular de aproximadamente 5 kD), pueden sufrir degradación mecánica debido a las fuerzas de cizalladura durante la purificación y filtración. Además, el factor Vlla es una enzima proteolítica activa que degrada otras proteínas, incluido el factor Vlla. La degradación del factor Vlla conlleva principalmente una escisión en la cadena pesada del factor Vlla, particularmente en los aminoácidos n.2 29 y 315 de la molécula. Finalmente, se pueden oxidar los residuos de metionina del factor Vil y el factor Vlla.
Un objeto de la presente invención consiste en proporcionar un método para retirar o inactivar virus de las composiciones líquidas de factor Vil, método por el cual se preserva sustancialmente la integridad de los componentes del factor Vil.
El documento WO 96/237 describe un método de filtración de virus de una solución que contiene un componente macromolecular, p. ej., una proteína tal como el factor IX proteico plasmático.
El documento WO 98/3786 describe la retirada de virus de soluciones proteicas derivadas de plasma por nanofiltración utilizando una membrana que tiene un tamaño de poro promedio de 15 nm.
Tomokiyo et al., Vox Sanguinis, 23, 84, 54-64 , describen la producción a gran escala de un concentrado del factor Vil activado derivado del plasma. El método de producción conlleva el paso de filtración de virus de una solución que comprende el factor Vil inactivo.
BREVE DESCRIPCIÓN DE LA INVENCIÓN
En un aspecto amplio, la presente invención se refiere a métodos para retirar virus de la composición del factor Vil. El término "virus" tal como se emplea en la presente se refiere a cualquier agente infeccioso ultramicroscópico que se replica a sí mismo únicamente dentro de células de hospedadores vivos o partículas no infecciosas derivadas de este. En una realización, el virus es infeccioso. En una realización, el virus es una partícula vírica no infecciosa.
Un primer aspecto de la presente invención se refiere a un método para retirar virus de una composición líquida del factor Vil recombinante, donde dicha composición comprende uno o más polipéptidos del factor Vil, donde la concentración de los polipéptidos del factor Vil está comprendida en el intervalo de.1 a 5 mg/mL, y donde la forma activada de los polipéptidos del factor Vil representa un 5-1% de la masa del polipéptido o de los polipéptidos del factor Vil en la composición, donde dicho método comprende someter dicha solución a nanofiltración utilizando un nanofiltro con un tamaño de poro de 8 nm como máximo.
Un segundo aspecto de la invención se refiere a un método del primer aspecto, donde dicha composición líquida está sustancialmente exenta de suero.
Un aspecto adicional de la invención se refiere a un método tal como se ha descrito anteriormente, donde dicho nanofiltro tiene una membrana producida a partir de uno o más materiales seleccionados entre celulosa regenerada de cupramonio, fluoruro de polivinilideno (PVDF, por sus siglas en inglés) hidrófilo, PVDF compuesto, PVDF modificado superficialmente y poliéter sulfona.
En un aspecto adicional de la invención, el método comprende además un método para inactivar virus en una composición líquida del factor Vil, donde dicho método comprende el paso de combinar dicha composición con un detergente.
Un aspecto adicional de la invención se refiere a un método para una eliminación de alto nivel de la presencia de virus activos en una composición líquida de factor Vil, donde el método comprende los pasos de (i) inactivar virus y (ii) retirar virus.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
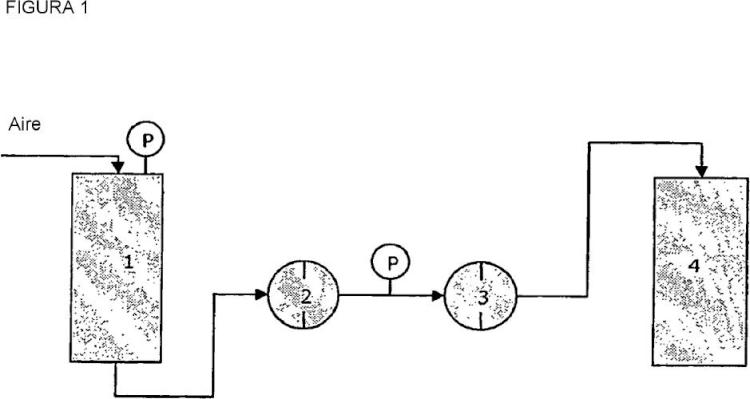
La Figura 1 es una ilustración esquemática de un sistema adecuado para los métodos de la invención. El sistema incluye un depósito a presión (1) con un suministro de aire comprimido, un prefiltro (2) para retirar partículas que de otra manera podrían obstruir el filtro de virus, un manómetro (P), un filtro de virus (3) y un depósito de recogida (4).
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
La presente invención proporciona métodos para retirar virus, incluidos los virus sin envoltura, de una composición 1 líquida del factor Vil que comprende una proporción significativa de polipéptidos activados, y de este modo activos proteolíticamente, del factor Vil, donde dicha composición comprende uno o más polipéptidos del factor Vil, donde la concentración de los polipéptidos del factor Vil está comprendida en el intervalo de.1 a 5 mg/mL y donde la forma activada de los polipéptidos del factor Vil representa un 5-1% de la masa del polipéptido o de los polipéptidos del factor Vil en la composición. El método incluye el paso de someter la composición líquida del factor Vil a 15 nanofiltración utilizando un nanofiltro que tiene un tamaño de poro de 8 nm como máximo.
El método es particularmente útil para retirar virus con envoltura así como de virus sin envoltura tales como el virus de la leucemia murina (con envoltura) que se puede retirar con filtros con un tamaño de poro de aproximadamente 5 nm y el parvovirus porcino (sin envoltura) que se puede retirar con filtros con un tamaño de poro de aproximadamente 2 nm.
Las composiciones líquidas de factor Vil, p. ej., aquellas que comprenden una proporción significativa de polipéptidos activados del factor Vil, puede prepararse, en principio, a partir de los componentes del factor Vil secos, pero más normalmente se obtienen a partir de procesos de producción a gran escala, p. ej., procesos que conllevan técnicas recombinantes. En este tipo de procesos, normalmente se recolecta el sobrenadante del cultivo celular y se somete posteriormente a uno o más pasos de procesamiento para obtener la proteína deseada, incluidas, sin 25 carácter limitante, la centrifugación o filtración para retirar células que no se han inmovilizado sobre los portadores; cromatografía de afinidad, cromatografía de interacción hidrófoba; cromatografía de intercambio iónico; cromatografía de exclusión por tamaño; procedimientos electroforéticos (p. ej., isoelectroenfoque preparativo (IEF, por sus siglas en inglés), solubilidad diferencial (p. ej., precipitación con sulfato amónico) o extracción y similares. Remítase a, en general, Scopes, Protein Purification, Springer-Verlag, Nueva York, 1982; y Protein Purification, J.-C. 3 Janson y Lars Ryden, editores, VCH Publishers, Nueva York, 1989. La purificación de los polipéptidos del factor Vil también puede conllevar, p. ej., cromatografía de afinidad sobre una columna con un anticuerpo contra el factor Vil (remítase a, p. ej., Wakabayashi et al., J. Biol. Chem. 261:1197, 1986; y Thim et al., Biochem. 27:7785, 1988) y la activación por escisión proteolítica, utilizando el factor XIla y otras proteasas que tienen una especificidad similar a la tripsina tales como, p. ej., el factor IXa, kalikreína, factor Xa y trombina. Remítase a, p. ej., Osterud et al., Biochem. 35 11:2853 (1972); Thomas, patente de EE. UU. N.2 4.456.591; y Hedner et al., J. Clin. Invest. 71:1836... [Seguir leyendo]
Reivindicaciones:
1. Un método para retirar virus de una composición líquida del factor Vil recombinante, donde dicha composición comprende uno o más polipéptidos del factor Vil, donde la concentración de los polipéptidos del factor Vil está comprendida en el intervalo de.1 a 5 mg/mL y donde la forma activada de los polipéptidos del factor Vil representa un 5-1% de la masa del polipéptido o de los polipéptidos del factor FVII en la composición;
donde dicho método comprende someter dicha solución a nanofiltración utilizando un nanofiltro que tiene un tamaño de poro de 8 nm como máximo.
2. El método de acuerdo con la reivindicación 1, donde la forma activada del polipéptido del factor Vil representa un 7-1% o un 8-1% de la masa del polipéptido o de los polipéptidos del factor Vil.
3. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde la composición líquida tiene un pH comprendido en el intervalo de 5.5-1, tal como en el intervalo de 7.-9.5, en el intervalo de 7.6-9.4, en el intervalo de 7.7-9.3, en el intervalo de 8.-9. o en el intervalo de 8.3-8.7.
4. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde la concentración del polipéptido o de los polipéptidos del factor Vil en la composición líquida está comprendida en el intervalo de.5-2. mg/mL.
5. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde el tamaño de poro del nanofiltro es de 5 nm como máximo, p. ej., de 3 nm como máximo, tal como comprendido en el intervalo de 1-3 nm.
6. El método de acuerdo con cualquiera de las reivindicaciones precedentes, donde la membrana del nanofiltro está producida a partir de uno o más materiales seleccionados entre celulosa regenerada de cupramonio, fluoruro de polivinilideno (PVDF) hidrófilo, PVDF compuesto, PVDF modificado superficialmente y poliéter sulfona.
7. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde la composición líquida del factor Vil se obtiene a partir de un sobrenadante de un cultivo celular.
8. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde la composición líquida está sustancialmente exenta de suero.
9. El método de acuerdo con cualquiera de las reivindicaciones 1-7, donde el polipéptido o los polipéptidos del factor Vil está/están producido/producidos por cultivos celulares en presencia de suero bovino fetal o bovino.
1. El método de acuerdo con cualquiera de las reivindicaciones anteriores, donde el polipéptido o los polipéptidos del factor Vil está/están producido/producidos por cultivos celulares en células CHO.
11. Un método para la eliminación de alto nivel de la presencia de virus activos en una composición líquida del factor Vil recombinante que comprende uno o más polipéptidos del factor Vil, donde la concentración de los polipéptidos del factor Vil está comprendida en el intervalo de.1 a 5 mg/mL y donde la forma activada de los polipéptidos del factor Vil representa un 5-1% de la masa del polipéptido o de los polipéptidos del factor Vil en la composición, donde el método comprende los pasos de (i) inactivar virus mediante un método que comprende el paso de combinar dicha composición con un detergente y (ii) separar virus mediante cualquiera de los métodos definidos en cualquiera de las reivindicaciones 1-1, en cualquier orden.
12. El método de acuerdo con la reivindicación 11, donde el paso de inactivar virus precede al paso de retirar virus.
Patentes similares o relacionadas:
Cadena ligera de enteroquinasa modificada, del 22 de Julio de 2020, de NOVO NORDISK A/S: Un análogo de la cadena ligera de la enteroquinasa bovina que comprende una secuencia de aminoácidos establecida en la SEQ ID NO: 1, en donde dicho análogo comprende […]
Formulaciones liofilizadas para antídoto del factor Xa, del 1 de Julio de 2020, de PORTOLA PHARMACEUTICALS, INC.: Una formulación acuosa, que comprende de 10 mM a 55 mM de arginina, de 1% a 3% de sacarosa (p/v), de 2% a 8% de manitol (p/v), y al menos 5 mg/ml de un polipéptido […]
Antídotos para inhibidores del factor Xa y procedimientos de uso de los mismos, del 24 de Junio de 2020, de PORTOLA PHARMACEUTICALS, INC.: Una composición farmacéutica que comprende un transportador y un polipéptido para uso en terapia donde el polipéptido comprende una secuencia de aminoácidos que tiene […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Proteínas prohemostáticas para el tratamiento del sangrado, del 3 de Junio de 2020, de ACADEMISCH ZIEKENHUIS LEIDEN: Una proteína recombinante que comprende un polipéptido del factor Xa de coagulación de mamífero, teniendo dicho polipéptido una alteración en la región de los […]
Ratones ADAM6, del 22 de Abril de 2020, de REGENERON PHARMACEUTICALS, INC.: Un ratón que ha experimentado reordenación de secuencia génica de inmunoglobulina de modo que exprese un linfocito B que comprende una secuencia de inmunoglobulina reordenada […]
Procedimiento de purificación de polipéptidos, del 22 de Abril de 2020, de CSL LIMITED: Procedimiento de purificación de un polipéptido de interés por cromatografía de intercambio catiónico en el que un compuesto químico se añade en una concentración de al menos […]
Proteínas de fusión recombinantes para la prevención o el tratamiento de adherencias en tejidos u órganos, del 8 de Abril de 2020, de Akesion GmbH: Proteína de fusión recombinante que incluye una enzima fibrinogenolítica con una secuencia de aminoácidos, que está unida en el extremo C y/o en el extremo […]