Proceso para el aislamiento de bisaril triazinas monofenólicas.
Un proceso para aislar un compuesto de Fórmula 1 a partir de una mezcla de productos que comprende un compuesto de triazina polifenólica o un compuesto de triazina poliresorcinol y un compuesto de Fórmula 1**Fórmula**
en el que Ar1 y Ar2 son iguales o diferentes y son radicales del compuesto de Fórmula 2**Fórmula**
y en el que
R1 es hidrógeno;
R1, R3, R4 y R5, son iguales o diferentes y se eligen de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, OR, NRR', CONRR', OCOR, CN, SR, SO2R, y opcionalmente con R3 y R4 o R4 y R5 tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado;
R, R', R6, R7, R8, R9, y R10 son iguales o diferentes y cada uno se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, y opcionalmente con R6 y R7, R7 y R8, R8 y R9, o R9 y R10, tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado que contiene opcionalmente átomos de O, N, o S en el anillo, y R6, R7, R8, R9, y R10, pueden ser alcoxi de 1 a 24 átomos de carbono, e Y es un enlace directo, O, NR", o S, en el que R" se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2002/016055.
Solicitante: CYTEC TECHNOLOGY CORP..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 300 DELAWARE AVENUE WILMINGTON, DELAWARE 19801 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CAPPADONA, RUSSELL, C., GUPTA, RAM, BABOO, SINGH,HARGURPREET.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D251/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 251/00 Compuestos heterocíclicos que contienen ciclos de triazina-1,3,5. › a tres átomos de carbono del ciclo.
PDF original: ES-2455271_T3.pdf
Fragmento de la descripción:
Proceso para el aislamiento de bisaril triazinas monofenólicas Campo de la invención Esta invención se refiere a un proceso nuevo, eficiente, económico y de propósito general para aislar compuestos de bisaril triazina monofenólica a partir de compuestos de triazinas polifenólicas y otras impurezas. Más específicamente, esta invención se refiere a un proceso para aislar los compuestos de bisaril triazina monofenólica poniéndolos en contacto con una base, un alcohol y/o un disolvente hidrocarbonado.
Antecedentes de la invención La exposición a la luz solar y a otras fuentes de radiación ultravioleta (UV) se sabe que causa la degradación de una amplia variedad de materiales, especialmente materiales poliméricos. Por ejemplo, los materiales poliméricos tales como plásticos frecuentemente se decoloran y/o se vuelven frágiles como resultado de la exposición prolongada a la luz UV. De acuerdo con esto, se ha desarrollado un gran volumen de técnica dirigida hacia materiales tales como absorbentes de luz UV y estabilizantes que son capaces de inhibir dicha degradación. Otras áreas de aplicaciones para los absorbentes de luz UV incluyen cosméticos (tales como agentes protectores solares) , fibras, spandex, tintas, materiales fotográficos y agentes de tinción.
Una clase de materiales que se sabe que son absorbentes de la luz UV son compuestos que tienen sustituyentes aromáticos en las posiciones 2, 4, y 6 del anillo 1, 3, 5-triazina, y en los que al menos uno de los anillos aromáticos tiene un sustituyente hidroxilo en la posición orto respecto al punto de unión al anillo triazina. En general, esta clase de compuestos es muy conocida en la técnica. Las descripciones de varios de dichos absorbentes de luz UV (UVA) de triazina así como los procesos para prepararlos pueden encontrarse en las referencias siguientes y referencias citadas en ellas, todas las cuales se incorporan por referencia como se muestra completamente en la presente memoria: Patente U.S. No. 6.239.275; Patente U.S. No. 6.239.276; Patente U.S. No. 6.242.597; Patente U.S. No.
6.225.468 y WO 00/29392.
Una clase preferida de UVA de triazina son UVA de bisaril triazinas monofenólicas asimétricas basadas en las 2 (2, 4-dihidroxiaril) -4, 6-bisaril-1, 3, 5-triazinas, por ejemplo, compuestos en los que hay dos grupos aromáticos no fenólicos y un grupo aromático fenólico que deriva del resorcinol, o resorcinol sustituido. El grupo 4-hidroxilo del compuesto parental, 2- (2, 4-dihidroxiaril) -4, 6-bisaril-1, 3, 5-triazina, generalmente se funcionaliza para preparar derivados 2- (2-hidroxi-4-oxiaril) -4, 6-bisaril-1, 3, 5-triazina para el uso final.
Existen varias estrategias reportadas en la bibliografía para preparar los UVA preferidos de 2- (2, 4-dihidroxiaril) -4, 6bisaril-1, 3, 5-triazina. (Para una revisión de los métodos conocidos previamente para preparar UVA de triazina, por favor véanse los artículos siguientes: 1. H. Brunetti y C. E. Luethi, Helvetica Chimica Acta, vol 55, 1972, páginas 1566-1595; 2. S. Tanimoto y M. Yamagata, Senr y o to Yakahin, vol. 40 (12) , 1995, páginas 325-339.)
Una mayoría de las estrategias consiste en tres etapas. La primera etapa, que puede implicar una única etapa o múltiples etapas a partir de materiales comerciales brutos, aborda la preparación del intermedio clave, 2-cloro-4, 6bisaril-1, 3, 5-triazina, que se arila posteriormente en la segunda etapa con 1, 3-dihidroxibenceno (resorcinol) o un 1, 3dihidroxibenceno sustituido en presencia de ácido de Lewis para formar el compuesto parental 2- (2, 4-dihidroxiaril) 4, 6-bisaril-1, 3, 5-triazina. El compuesto parental 2- (2, 4-dihidroxiaril) -4, 6-bisaril-1, 3, 5-triazina, como se ha mencionado anteriormente, generalmente se funcionaliza adicionalmente, por ejemplo, se alquila, para preparar el producto final 2- (2-hidroxi-4-oxiaril) -4, 6-bisaril-1, 3, 5-triazina.
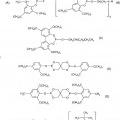
Esquema General para Preparar 2- (2-hidroxi-4-oxiaril) -4, 6-bisaril-triazinas Etapa 1: Preparación de 2-cloro-4, 6-bisaril-1, 3, 5-triazina
Etapa 2: Preparación de 2- (2, 4-dihidroxiaril) -4, 6-bisaril-1, 3, 5-triazina Etapa 3: Preparación de 2- (2, 4-dihidroxiaril) -4, 6-bisaril-1, 3, 5-triazina Se ha admitido que el método más versátil y económico para preparar UVA de bisaril triazina monofenólica asimétrica es usar una reacción de Friedel-Crafts en cloruro cianúrico con aromáticos no fenólicos para formar en primer lugar 2-cloro-4, 6-bisaril-1, 3, 5-triazina, seguido de otra reacción de Friedel-Crafts con el aromático fenólico, en este caso resorcinol, para preparar la bisaril triazina monofenólica deseada. Sin embargo, se ha puesto de manifiesto en la técnica anterior (véase, la Patente U.S. No. 3.394.134) que este proceso conocido como se describe en la Patente U.S. No. 3.268.474 da lugar, sólo en caso excepcionales, a los derivados disustituidos deseados de cloruro cianúrico con alguna selectividad. Incluso cuando el compuesto aromático y cloruro cianúrico se hacen reaccionar en proporciones molares (1:1) , el resultado es en general una mezcla que contiene productos mono, di, y tri-aril sustituidos, y, además, cloruro cianúrico que no ha reaccionado (Patente U.S. No. 3.394.134) (Esquema 1) .
Usando el proceso mencionado anteriormente, sólo se obtiene un rendimiento útil del intermedio deseado 2-cloro4, 6-bisaril-1, 3, 5-triazina con m-xileno como el reactante aromático (GB 884802) . Se preparó 2- (2, 4-dihidroxifenil) 4, 6-bis (2, 4-dimetilfenil) -1, 3, 5-triazina, desprovista de impurezas de poliresorcinol-triazina, a partir de la 2-cloro-4, 6bis (2, 4-dimetilfenil) -1, 3, 5-triazina aislada que se purificó por recristalización, antes de hacerla reaccionar con resorcinol en una segunda etapa (véase la Patente U.S. No. 3.244.708) . El aislamiento y recristalización de la 2cloro-4, 6-bis (2, 4-dimetilfenil) -1, 3, 5-triazina resulta en una pérdida de rendimiento. Con otros aromáticos, se forma una mezcla difícil de separar de todos los posibles productos sin selectividad para la 2-cloro-4, 6-bisaril-1, 3, 5-triazina deseada (Por ejemplo, véase H. Brunetti y C. E. Luethi, Helvetica Chimica Acta, vol 55, 1972, página 1575 y S. Tanimoto y M. Yamagata, Senr y o to Yakahin, vol. 40 (12) , 1995, páginas 325-339) .
Cuando la mezcla de reacción de la primera reacción de Friedel-Crafts (Esquema 1) sin ninguna purificación se trata en una reacción de Friedel-Crafts posterior con resorcinol, el derivado bisaril da lugar a la formación de la monoresorcinol-bisaril-triazina deseada, y el producto monoaril sustituido da lugar a la formación de derivado monoaril-bisresorcinol. Mientras, el cloruro cianúrico que no ha reaccionado da lugar a la formación de derivados bis y tris-resorcinol-triazina, es decir, poliresorcinol-triazinas (véase el Esquema 2) .
Estas impurezas poliresorcinol-triazina (anillo triazina con más de un resorcinol unido) dan lugar al amarilleo en el uso de los absorbentes de UV preparados a partir de la monoresorcinol-bisaril-triazina en varios sustratos poliméricos, por ejemplo, en policarbonatos, en barnices, en pintura de acabado para automóviles, etc. Así, es altamente deseable para muchas de dichas aplicaciones que el derivado monoresorcinol-bisaril-triazina esté desprovisto de estas impurezas. Desafortunadamente, no ha habido ningún proceso conocido en la bibliografía para aislar derivado monoresorcinol-bisaril-triazina a partir de la mezcla que contiene impurezas de poliresorcinol. La ausencia de selectividad para la sustitución bisaril en la reacción de Friedel-Crafts de cloruro cianúrico, acoplado con los problemas asociados con el aislamiento del intermedio bisaril y el derivado monoresorcinol-bisaril-triazina, ha limitado en gran medida la utilidad de la estrategia más versátil y económica para la clase preferida de UVA de triazina.
Para superar este obstáculo, y para excluir la formación de poliresorcinol-triazinas, se han desarrollado otras rutas económicamente menos atractivas en las que o no se usó cloruro cianúrico como material de parida y el anillo de triazina se sintetizó por diferentes métodos, o la formación de impurezas de poliresorcinol se excluyó mediante rutas tortuosas (Por ejemplo, véase: A. Ostrogovich, Chemiker-Zeitung No. 78, página 738, 1912; von R. Hirt, H. Nidecker y R. Berchtold, Helvitica Chimica Acta, vol. 33, página 1365, 1950; H. Brunetti y C. E. Luethi, Helvetica Chimica Acta, vol 55, 1972, página 1575; Patente U.S. No. 4.092.466; Patente U.S. No. 5.084.570; Patente U.S. No. 5.106.972; Patente U.S. No. 5.438.138; Patente U.S. No. 5.726.310; Patente U.S. No. 6.020.490; EP 0941989 y Patente Japonesa 09059263)
Una estrategia directa alternativa para la preparación de monoresorcinol-bisaril-triazina como se describe en la Patente U.S. No. 6.225.468... [Seguir leyendo]
Reivindicaciones:
1. Un proceso para aislar un compuesto de Fórmula 1 a partir de una mezcla de productos que comprende un compuesto de triazina polifenólica o un compuesto de triazina poliresorcinol y un compuesto de Fórmula 1
en el que Ar1 y Ar2 son iguales o diferentes y son radicales del compuesto de Fórmula 2
y en el que R1 es hidrógeno;
R1, R3, R4 y R5, son iguales o diferentes y se eligen de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, OR, NRR', CONRR', OCOR, CN, SR, SO2R, y opcionalmente con R3 y R4 o R4 y R5 tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado;
R, R', R6, R7, R8, R9, y R10 son iguales o diferentes y cada uno se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, y opcionalmente con R6 y R7, R7 y R8, R8 y R9, o R9 y R10, tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado que contiene opcionalmente átomos de O, N, o S en el anillo, y R6, R7, R8, R9, y R10, pueden ser alcoxi de 1 a 24 átomos de carbono, e Y es un enlace directo, O, NR", o S, en el que R" se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono;
en el dicho proceso comprende la etapa de:
- poner en contacto dicha mezcla de productos con una base inorgánica para formar una mezcla de aislamiento, y
- aislar el compuesto de fórmula 1 de la mezcla de aislamiento, aislamiento que se efectúa
- si la mezcla de productos está en forma sólida se pone en contacto con una base inorgánica que se disuelve en agua, en un disolvente o una mezcla de disolventes, por filtración, o
- si la mezcla de productos se disuelve en un disolvente que tiene base orgánica, y la base inorgánica se disuelve en un disolvente que tiene base acuosa, eliminando la capa de base inorgánica de las dos capas formadas, en el que el disolvente usado para disolver la base inorgánica es inmiscible con el disolvente usado para disolver la mezcla de productos.
2. El proceso de la reivindicación 1 en el que dicha mezcla de productos está en una forma sólida.
3. El proceso de la reivindicación 1 en el que dicha etapa de puesta en contacto es a una temperatura de entre 10°C a la temperatura de reflujo de la mezcla de aislamiento.
4. El proceso de la reivindicación 1 en el que dicha base se disuelve en al menos un primer disolvente y/o dicha mezcla de productos se disuelve en al menos un segundo disolvente.
5. El proceso de la reivindicación 1 en el que dicha etapa de puesta en contacto es a un pH entre 7 a 14.
6. El proceso de la reivindicación 2 que comprende además la etapa de poner en contacto el filtrado de la etapa de filtración con un ácido para aislar un compuesto de triazina polifenólica.
7. El proceso de la reivindicación 1 en el que dicha base se disuelve en al menos un primer disolvente y dicha mezcla de productos se disuelve en al menos un segundo disolvente, en el que dicho segundo disolvente es sustancialmente inmiscible en dicho primer disolvente y en el que se forman al menos dos capas diferentes.
8. Un proceso para aislar un compuesto de Fórmula 1 a partir de una mezcla de productos que comprende un compuesto de triazina polifenólica o un compuesto de triazina poliresorcinol y un compuesto de Fórmula 1
en el que Ar1 y Ar2 son iguales o diferentes y son radicales del compuesto de Fórmula 2
y en el que R1 es hidrógeno;
R2, R3, R4 y R5, son iguales o diferentes y se eligen de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, OR, NRR', CONRR', OCOR, CN, SR, SO2R, y opcionalmente con bien R3 y R4 o R4 y R5 tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado;
R, R', R6, R7, R8, R9, y R10 son iguales o diferentes y cada uno se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono, bifenileno sustituido o no sustituido, naftaleno sustituido o no sustituido, y opcionalmente con R6 y R7, R7 y R8, R8 y R9, o R9 y R10, tomados conjuntamente siendo una parte de un anillo carbocíclico fusionado saturado o insaturado que contiene opcionalmente átomos de O, N, o S en el anillo, y R6, R7, R8, R9, y R10, pueden ser un alcoxi de 1 a 24 átomos de carbono, e Y es un enlace directo, O, NR", o S, en el que R" se elige de hidrógeno, alquilo de 1 a 24 átomos de carbono, haloalquilo de 1 a 24 átomos de carbono, arilo de 6 a 24 átomos de carbono, alquenilo de 2 a 24 átomos de carbono, acilo de 1 a 24 átomos de carbono, cicloalquilo de hasta 24 átomos de carbono, cicloacilo de 5 a 24 átomos de carbono, aralquilo de 7 a 24 átomos de carbono, o aracilo de 6 a 24 átomos de carbono;
en el dicho proceso comprende la etapa de:
- poner en contacto una mezcla de productos con al menos dos componentes seleccionados del grupo que consiste en una base inorgánica, un alcohol y un disolvente hidrocarbonado, en el que uno de los componentes seleccionados es una base inorgánica y en el que dicha mezcla de productos comprende dicho compuesto de Fórmula 1 y un compuesto de triazina polifenólica, y
- aislar el compuesto de fórmula 1 de la mezcla de aislamiento, aislamiento que se efectúa
- si la mezcla de productos está en forma sólida se pone en contacto con una base inorgánica que se disuelve en agua, en un disolvente o una mezcla de disolventes, por filtración, o
- si la mezcla de productos se disuelve en un disolvente que tiene base orgánica, y la base inorgánica se disuelve en un disolvente que tiene base acuosa, eliminando la capa de base inorgánica de las dos capas formadas, en el que el
disolvente usado para disolver la base inorgánica es inmiscible con el disolvente usado para disolver la mezcla de productos.
9. El proceso de la reivindicación 8 en el que dichos componentes son una base inorgánica y un disolvente hidrocarbonado.
10. El proceso de la reivindicación 8 o de la reivindicación 9 en el que los disolventes hidrocarbonados son 10 compuestos que tienen de uno a veinte átomos de carbono.
Patentes similares o relacionadas:
Proceso novedoso para la eterificación de triazinas de bisresorcinilo, del 20 de Noviembre de 2019, de DSM IP ASSETS B.V.: Proceso para la preparación de triazinas de bisresorcinilo de fórmula (I),**Fórmula** en la que R1 es hidrógeno, un grupo alquilo C1-C18 o un grupo alquenilo C2-C18, […]
Proceso para la preparación de triazinas, del 3 de Abril de 2019, de DSM IP ASSETS B.V.: Un proceso para la preparación de bis-resorcinil-triazinas de fórmula (I)**Fórmula** en la que R1 es un grupo alquilo C1-C18 o un grupo alquenilo C2-C18, comprendiendo […]
Recubrimientos transparentes teñidos estabilizados para UV con 2-hidroxifenil triazina, del 21 de Febrero de 2018, de BASF SE: Una composición de recubrimiento clara teñida que comprende (a) al menos un absorbente de UV 2-hidroxifenil triazina, (b) al menos un pigmento seleccionado […]
Preparación de sustancias que absorben UV a escala nanométrica UV, del 5 de Abril de 2017, de BASF SE: Un método para preparar una composición que comprende una sustancia orgánica insoluble micronizada que absorbe UV, el cual comprende la molienda […]
Absorbentes UV especiales para recubrimientos de protección UV endurecibles, del 7 de Enero de 2015, de Bayer Intellectual Property GmbH: Compuestos de la fórmula general (I) A - X (- T)n (I), en la que A representa **Fórmula** en la que Y1 e Y2 representan independientemente uno de otro sustituyentes […]
 Forma cristalina de 2-(4,6-bis-bifenil-4-il-1,3,5-triazin-2-il)-5-(2-etil-(n)-hexiloxi)fenol, del 9 de Julio de 2014, de BASF SE: La forma cristalina de 2-(4,6-bis-bifenil-4-il-1,3,5-triazin-2-il)-5-(2-etil-(n)-hexiloxi)fenol, caracterizada por un patrón de difracción […]
Forma cristalina de 2-(4,6-bis-bifenil-4-il-1,3,5-triazin-2-il)-5-(2-etil-(n)-hexiloxi)fenol, del 9 de Julio de 2014, de BASF SE: La forma cristalina de 2-(4,6-bis-bifenil-4-il-1,3,5-triazin-2-il)-5-(2-etil-(n)-hexiloxi)fenol, caracterizada por un patrón de difracción […]
Hidroxifeniltriazinas con un sistema de anillos condensados carbocíclico aromático, del 18 de Septiembre de 2013, de BASF SE: Compuesto de fórmula (I) en la que E1 es un sistema de anillos condensados carbocíclico aromático sustituido o no sustituido que comprende […]
PIRIDINAS, PIRIMIDINAS, PIRAZINAS Y TRIAZINAS SUSTITUIDAS CON ARILO Y EL USO DE LAS MISMAS, del 20 de Diciembre de 2010, de EURO-CELTIQUE S.A.: Un compuesto que tiene la Fórmula I: **Fórmula** o una sal, éster, amida o solvato farmacéuticamente aceptable del mismo, en la que: Y es **Fórmula** o R7, con la condición […]