Procedimientos de preparación de la forma polimórfica A de acetato de bazedoxifeno.
Un procedimiento de preparación de la forma polimórfica A de acetato de bazedoxifeno,
comprendiendo elprocedimiento:
(a) poner en contacto 1-(4-(2-azepan-1-il)etoxi)bencil)-5-(benciloxi)-2-(4-(benciloxi)fenil)-3-metil-1H-indol con hidrógeno en un disolvente que comprende etanol y en presencia de un catalizador a temperatura elevada paraproporcionar una primera mezcla de reacción que comprende base libre de bazedoxifeno, en la que menos del 1 %del 1-(4-(2-azepan-1-il)etoxi)bencil)-5-(benciloxi)-2-(4-(benciloxi)fenil)-3-metil-1H-indol permanece en la mezcla dereacción;
(b) tratar dicha primera mezcla de reacción con un antioxidante, para proporcionar una segunda mezcla de reacción;
(c) filtrar dicha segunda mezcla de reacción, para proporcionar una solución que comprende base libre debazedoxifeno; y
(d) tratar dicha solución con ácido acético, para cristalizar la Forma A de acetato de bazedoxifenoen el que la temperatura elevada en la etapa (a) es una temperatura de 40 ºC hasta 60 ºC.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/033772.
Solicitante: WYETH LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CANNATA, VINCENZO, COTARCA, LIVIUS, BARRECA, GIUSEPPE, ALLEGRINI, PIETRO, SORIATO, GIORGIO, VERZINI, MASSIMO, BRESCELLO,ROBERTO, ANDREELLA,PAOLO, TASINATO,FRANCESCO, DEMO,MARCO, BASSAN,FABIO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/404 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Indoles, p. ej. pindolol.
- A61P19/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para la osteoporosis.
- C07D209/12 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 209/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros, condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Radicales sustituidos por átomos de oxígeno.
PDF original: ES-2436662_T3.pdf
Fragmento de la descripción:
Procedimientos de preparación de la forma polimórfica A de acetato de bazedoxifeno Campo de la invención La presente invención se refiere a procedimientos de preparación de la forma polimórfica A de acetato de bazedoxifeno; y a la forma polimórfica A de acetato de bazedoxifeno preparada por dichos procedimientos.
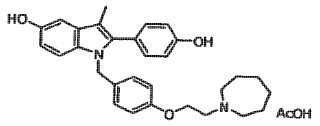
Antecedentes de la invención El acetato de bazedoxifeno tiene el nombre químico (ácido 1-[4- (2-azepan-1-il-etoxi) -bencil]-2- (4-hidroxi-fenil) -3metil-1H-indol-5-ol acético) y tiene la estructura química mostrada a continuación:
El acetato de bazedoxifeno pertenece a la clase de fármacos denominados típicamente moduladores selectivos del receptor de estrógenos (SERM) . De forma coherente con su clasificación, el bazedoxifeno demuestra afinidad porlos receptores de estrógenos (ER) pero muestra efectos estrogénicos selectivos en tejidos. Por ejemplo, el acetatode bazedoxifeno demuestra poca o ninguna estimulación de la respuesta uterina en modelos preclínicos de estimulación uterina. Por el contrario, el acetato de bazedoxifeno demuestra un efecto de tipo agonista de estrógenos en la prevención de la pérdida ósea y en la reducción del colesterol en un modelo de rata ovariectomizada de osteopenia. En una línea celular MCF-7 (línea celular de cáncer de mama humano) , el acetatode bazedoxifeno se comporta como un antagonista de estrógenos. Estos datos demuestran que el acetato debazedoxifeno es estrogénico sobre parámetros óseos y lipídicos cardiovasculares y antiestrogénico en tejido uterinoy mamario y por lo tanto, tiene el potencial de tratar numerosas enfermedades o estados similares a enfermedadesdiferentes, en los que está implicado el receptor de estrógenos.
Las Patentes de Estados Unidos N.ºs 5.998.402 y 6.479.535 informan de la preparación de acetato de bazedoxifenoy caracterizan la sal como poseedora de un punto de fusión de 174-178 ºC. La preparación sintética de acetato debazedoxifeno también ha aparecido en la literatura general. Véase, por ejemplo, Miller y col., J. Med. Chem., 2001, 44, 1654-1657, que informa sobre la sal como un sólido cristalino que tiene un punto de fusión de 170, 5-172, 5 ºC.También ha aparecido una descripción adicional de la actividad biológica del fármaco en la literatura general (por ejemplo, Miller y col., Drugs of the Future, 2002, 27 (2) , 117-121) .
Es bien conocido que la forma polimórfica cristalina de un fármaco particular es a menudo es un determinanteimportante de la facilidad de preparación, estabilidad, solubilidad, estabilidad durante el almacenamiento, facilidadde formulación y farmacología in vivo del fármaco. Las formas polimórficas se dan donde la misma composición demateria cristaliza en una disposición de red cristalina diferente, dando como resultado propiedades termodinámicas diferentes y estabilidades específicas para la forma polimórfica particular. En los casos en los que pueden producirsedos o más sustancias polimorías, es deseable tener un procedimiento para fabricar los dos polimorfos en forma pura.Para decidir qué polimorfo es preferible, deben compararse las numerosas propiedades de los polimorfos y elpolimorfo preferido, se elige basándose en las muchas propiedades físicas variables. Es totalmente posible que unaforma polimórfica pueda ser preferible en algunas circunstancias, en las que ciertos aspectos, tales como facilidad de preparación, estabilidad, etc. se consideran críticos. En otras situaciones, puede preferirse un polimorfo diferentepara una mayor solubilidad y/o una mejor farmacocinética.
La forma polimórfica A de acetato de bazedoxifeno se divulga en el documento US 2005/0227965, mientras que laforma polimórfica B de acetato de bazedoxifeno se divulga en el documento US 2005/0250762. La Forma A tienemayor solubilidad que la Forma B en sistemas disolventes tanto acuosos como orgánicos. Esto es particularmente ventajoso en formulaciones en las que la solubilidad de la composición particular es un punto a tener en cuenta. Porejemplo, una mayor solubilidad puede influir en la biodisponibilidad, que puede afectar a la absorción y distribuciónbiológica del fármaco, pudiendo asimismo facilitar la formulación en vehículos líquidos. Sin embargo, la Forma A esel polimorfo cinético (o meta-estable) , mientras que la Forma B es el polimorfo termodinámicamente más estable. LaForma A puede convertirse fácilmente en la Forma B después de entrar en contacto con un disolvente o una mezcla de disolventes (por ejemplo, acetato de etilo y etanol) , lo que presenta un desafío para la preparación de la Forma Apura, que está sustancialmente libre de la Forma B.
Debido a que la forma polimórfica A de acetato de bazedoxifeno proporciona una mejor biodisponibilidad en algunasformulaciones de fármacos, hay una necesidad de un procedimiento nuevo y práctico que produzca de forma fiablela forma polimórfica A de acetato de bazedoxifeno. Los procedimientos de preparación de la forma polimórfica A de acetato de bazedoxifeno descritos en el presente documento ayudan a satisfacer estas y otras necesidades. Unprocedimiento de preparación de la forma polimórfica A de acetato de bazedoxifeno se divulga también en unaSolicitud de Patente de Estados Unidos, transferida legalmente y en trámite como la presente, con N.º de Serie61/027.607, presentada el 11 de febrero de 2008.
A menos que se definan en contra, todos los términos técnicos y científicos usados en el presente documento tienen el mismo significado que el entendido habitualmente por un experto en la materia a la que pertenece esta invención.Aunque pueden usarse procedimientos y materiales similares o equivalentes a aquellos descritos en el presentedocumento en la puesta en práctica o ensayo de la presente invención, a continuación se describen procedimientosy materiales adecuados.
Sumario de la invención En un aspecto, la presente invención se refiere a un procedimiento de preparación de la forma polimórfica A deacetato de bazedoxifeno, comprendiendo el procedimiento:
(a) poner en contacto 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol con hidrógeno, en un disolvente que comprende etanol y en presencia de un catalizador a temperatura elevada paraproporcionar una primera mezcla de reacción que comprende base libre de bazedoxifeno, estando la primera mezcla de reacción sustancialmente libre de 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1Hindol;
(b) tratar dicha primera mezcla de reacción con un antioxidante, para proporcionar una segunda mezcla de reacción;
(c) filtrar dicha segunda mezcla de reacción, para proporcionar una solución que comprende base libre de bazedoxifeno; y
(d) tratar dicha solución con ácido acético, para cristalizar la forma polimórfica A de acetato de bazedoxifeno;
en el que la temperatura elevada en la etapa (a) es una temperatura de 40 ºC hasta 78 ºC.
Breves descripciones de los dibujos La Figura 1 muestra una superposición de espectros IR de las formas polimórficas A y B de acetato de bazedoxifeno (la parte inferior de la Figura 1 corresponde a la Forma A y la parte superior corresponde a la Forma B) .
La Figura 2 muestra un termograma de DSC para la forma polimórfica A de acetato de bazedoxifeno.
La Figura 3 muestra un termograma de DSC para la forma polimórfica B de acetato de bazedoxifeno.
La Figura 4 muestra una superposición de termogramas de DSC para las formas polimórficas A y B de acetato debazedoxifeno.
La Figura 5 es un termograma de DSC para la forma polimórfica A de acetato de bazedoxifeno, que muestra un ejemplo de un lote de Forma A con un contenido de Forma B menor del 0, 1 % p/p.
La Figura 6 muestra una curva de TGA para la forma polimórfica A de acetato de bazedoxifeno.
La Figura 7 muestra una curva de TGA para la forma polimórfica B de acetato de bazedoxifeno.
La Figura 8 muestra el contenido de la forma polimórfica B frente al tiempo y frente a la temperatura, para unamuestra de la forma polimórfica A de acetato de bazedoxifeno que está humedecida con ETOH.
La Figura 9 muestra el contenido de la forma polimórfica B frente al tiempo y frente a la temperatura, para unamuestra de la forma polimórfica A de acetato de bazedoxifeno que está humedecida con EtOAc
Descripción detallada de la invención La forma polimórfica A de acetato de bazedoxifeno tiene mayor solubilidad tanto en sistemas disolventes acuososcomo orgánicos, que la forma polimórfica B de acetato de bazedoxifeno. Como resultado, la Forma A de acetato de bazedoxifeno proporciona una mejor biodisponibilidad en formulaciones de fármaco. Sin embargo, la Forma A es elpolimorfo... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento de preparación de la forma polimórfica A de acetato de bazedoxifeno, comprendiendo elprocedimiento:
(a) poner en contacto 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol con hidrógeno en un disolvente que comprende etanol y en presencia de un catalizador a temperatura elevada para proporcionar una primera mezcla de reacción que comprende base libre de bazedoxifeno, en la que menos del 1 % del 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol permanece en la mezcla dereacción;
(b) tratar dicha primera mezcla de reacción con un antioxidante, para proporcionar una segunda mezcla de reacción;
(c) filtrar dicha segunda mezcla de reacción, para proporcionar una solución que comprende base libre de bazedoxifeno; y
(d) tratar dicha solución con ácido acético, para cristalizar la Forma A de acetato de bazedoxifeno en el que la temperatura elevada en la etapa (a) es una temperatura de 40 ºC hasta 60 ºC.
2. El procedimiento de la reivindicación 1, en el que en la etapa (a) el disolvente comprende adicionalmente al15 menos un disolvente seleccionado entre el grupo que consiste en acetato de etilo, acetona, ciclohexano y metanol.
3. El procedimiento de la reivindicación 1 o 2, en el que en la etapa (a) el 1- (4- (2-azepan-1-il) etoxi) bencil) -5 (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol se pone en contacto con hidrógeno durante menos de 10 horas.
4. El procedimiento de la reivindicación 1 o 2, en el que en la etapa (a) el 1- (4- (2-azepan-1-il) etoxi) bencil) -5 (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol se pone en contacto con hidrógeno durante menos de 6 horas.
5. El procedimiento de la reivindicación 1 o 2, en el que en la etapa (a) el 1- (4- (2-azepan-1-il) etoxi) bencil) -5 (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol se pone en contacto con hidrógeno durante menos de 4 horas.
6. El procedimiento de una cualquiera de las reivindicaciones 1-5, en el que en la etapa (a) , el catalizador esun catalizador de Pd/C; el catalizador de Pd/C se usa en una cantidad menor de aproximadamente 10 mmol pormol de 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol, tal como menos de 6 mmol
por mol de 1- (4- (2-azepan-1-il) etoxi) bencil) -5- (benciloxi) -2- (4- (benciloxi) fenil) -3-metil-1H-indol usado; y el catalizador de Pd/C tiene un área superficial total (B.E.T) de más de aproximadamente 1100 m2/g, tal como más de aproximadamente 1500 m2/g.
7. El procedimiento de una cualquiera de las reivindicaciones 1-6 en el que la etapa (a) se realiza a una temperatura de 50 ºC.
8. El procedimiento de una cualquiera de las reivindicaciones 1-7 en el que en la etapa (b) , dicho antioxidante es ácido ascórbico.
9. El procedimiento de una cualquiera de las reivindicaciones 1-8 en el que la etapa (d) se facilita sembrando con la forma polimórfica A de acetato de bazedoxifeno.
10. El procedimiento de una cualquiera de las reivindicaciones 1-9, en el que en la etapa (d) se realiza a una
temperatura de 40 ºC o menor, tal como a una temperatura de 30 ºC o menor, a una temperatura que varía de 20 ºC a 35 ºC, a una temperatura que varía de 25 ºC a aproximadamente 30 ºC, o a una temperatura que varía de 28 ºC a 30 ºC.
11. El procedimiento de una cualquiera de las reivindicaciones 1-10, en el que las etapas (a) a (d) se realizan en atmósfera inerte.
12. El procedimiento de una cualquiera de las reivindicaciones 1-11 que comprende adicionalmente aislar la forma polimórfica A de acetato de bazedoxifeno por filtración, lavado y secado.
13. El procedimiento de la reivindicación 12, en el que dicho secado se realiza en una secadora de filtro agitado o una secadora de tambor.
Figura 1 Figura 2 Figura 3 Figura 4 Figura 5 Figura 6 Figura 7
(Experimento 5.0)
Figura 8 Figura 9
Patentes similares o relacionadas:
Composiciones que comprenden una proteína de fusión de VIP-ELP para su uso en el tratamiento de fibrosis quística, del 29 de Julio de 2020, de Phasebio Pharmaceuticals, Inc: Una composición farmacéutica que comprende una proteína de fusión que comprende un péptido intestinal vasoactivo (VIP) y uno o más péptidos de tipo elastina (ELP), que […]
Análogos de indolina y usos de los mismos, del 8 de Julio de 2020, de Oncternal Therapeutics, Inc: Un compuesto que tiene la fórmula (I): **(Ver fórmula)** o un estereoisómero, una sal farmacéuticamente aceptable, o solvato del mismo, donde A se […]
Tratamiento de disfunción eréctil y otras indicaciones, del 1 de Julio de 2020, de STRATEGIC SCIENCE & TECHNOLOGIES, LLC: Una composición para su uso en un método de tratamiento de la disfunción sexual en un sujeto, preferiblemente un sujeto humano, comprendiendo la composición: […]
Forma de dosificación para su inserción en la boca, del 17 de Junio de 2020, de Nal Pharmaceutical Group Limited: Composición farmacéutica para aplicación a la mucosa oral que comprende: una matriz soluble en agua que comprende una cantidad eficaz de un agente farmacéuticamente […]
Composiciones para el tratamiento del síndrome X frágil, del 8 de Abril de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Un abridor de un canal de potasio maxi-K para su uso en el tratamiento del síndrome X frágil, donde dicho abridor de canal de potasio […]
Compuestos heterocíclicos y métodos para su uso, del 8 de Abril de 2020, de NOVARTIS AG: Un compuesto de formula (I): **(Ver fórmula)** donde: X esta ausente e Y es -CHR3CH2-, -CH2CHR3-, -CHR3CHR4CH2-, -CH2CHR3CHR4-, -CH2CH2CHR3-, -CR3=CHCH2-, […]
ACILHIDRAZONAS PARA EL TRATAMIENTO DE ENFERMEDADES NEUROLÓGICAS, del 2 de Abril de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a un grupo de compuestos con un núcleo estructural de acilhidrazona que presentan capacidad moduladora de la interacción […]
Medicamentos para el tratamiento o la prevención de enfermedades fibróticas, del 25 de Marzo de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: 3-Z-[1-(4-(N-((4-metil-piperazin-1-il)-metilcarbonil)-N-metil-amino)-anilino)-1-fenil-metilen]-6-metoxicarbonil-2- indolinona, los tautómeros, los diastereómeros,…