USO DE CLASIFICADORES DE ACTIVIDAD GÉNICA PARA LA CLASIFICACIÓN IN VITRO DE PERFILES DE EXPRESIÓN GÉNICA DE PACIENTES CON FALLO MULTIORGÁNICO INFECCIOSO/NO INFECCIOSO.
Uso de polinucleótidos que se seleccionan del grupo constituido por:
SEQ ID I.1, SEQ ID I.2, SEQ ID I.3, SEQ ID I.4, SEQ ID I.5, SEQ ID I.6, SEQ ID I.7, SEQ ID I.8 y SEQ ID I.9 o secuencias parciales de los mismos con una longitud de 20 a 200 nucleótidos como marcadores de actividad génica para la clasificación de pacientes como "no infectados sin fallo multiorgánico" o como "no enfermos de fallo multiorgánico infeccioso" o como "enfermos de fallo multiorgánico infeccioso"
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/060780.
Solicitante: SIRS-LAB GMBH.
Nacionalidad solicitante: Alemania.
Dirección: WINZERLAER STRASSE 2A 07745 JENA ALEMANIA.
Inventor/es: RUSSWURM,Stefan, REINHART,Konrad.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Marzo de 2006.
Clasificación Internacional de Patentes:
- C12Q1/68M6
Clasificación PCT:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2357853_T3.pdf
Fragmento de la descripción:
La presente invención se refiere al uso de marcadores de actividad génica para la clasificación de pacientes que están enfermos de un fallo multiorgánico infeccioso o no infeccioso.
La invención se refiere además al uso de estos clasificadores de actividad génica como valiosos parámetros guardados en dispositivos que se usan para el diagnóstico in vitro de pacientes con fallo multiorgánico infeccioso o no infeccioso. Además, la invención se refiere a un dispositivo para el diagnóstico in vitro de pacientes que están enfermos de un fallo multiorgánico infeccioso o no infeccioso.
Además, la invención se refiere al uso de los marcadores/clasificadores de actividad génica para la clasificación de perfiles de expresión génica de pacientes para evaluar el efecto terapéutico de principios activos contra fallo multiorgánico infeccioso o no infeccioso.
A pesar de los avances en el entendimiento patofisiológico y el tratamiento de apoyo, el síndrome del fallo multiorgánico (SFMO) o el fallo multiorgánico (FMO) representa en pacientes que requieren cuidados intensivos la causa más frecuente de muerte y mundialmente sigue aumentando. Las consecuencias de este desarrollo no sólo son considerables para los pacientes individuales, sino que tienen enormes repercusiones sobre los costes de la sanidad y el avance médico en muchos campos de la medicina.
Como fallo multiorgánico se designa el fallo que se produce al mismo tiempo o en un corto periodo de tiempo de dos o más sistemas de órganos vitales. El síndrome del fallo multiorgánico (SFMO) precede al FMO como fallo orgánico inicial [1]. Actualmente se habla de fallo multiorgánico cuando dos o más órganos presentan al mismo tiempo o sucesivamente fallos, descartándose un fallo orgánico crónicamente persistente [2]. El pronóstico del FMO depende estrechamente del número de sistemas orgánicos implicados. La mortalidad asciende en el fallo de un órgano dentro de las primeras 24 horas al 22%, después de 7 días al 41%. En el caso de fallo de tres sistemas de órganos la mortalidad asciende en el primer día al 80% y después de 4 días al 100% [3].
Para la puntuación clínica del grado de gravedad de SFMO e FMO se usa regularmente la puntuación de fallo multiorgánico (Multiple-Organ-Failure-Score) (puntuación de FMO, de MOF-Score) de GORIS y col. [4] o alternativamente también la puntuación de la evaluación de fallo multiorgánico relacionada con sepsis (EIMRS) (Sepsisrelated Organ Failure Assessment (SOFA) Score) [5]. La puntuación de FMO permite una clasificación rápida y clínicamente sencilla de la función de los órganos en tres grados. Una puntuación de FMO > 4 designa regularmente en la bibliografía clínica FMO [6]. La puntuación de IMRS es un sistema de puntos que valora la rápida evaluación clínica de la función respectivamente en cuatro grados de gravedad, los siguientes sistemas de órganos: respiración (pulmones), coagulación, hígado, aparato circulatorio, sistema nervioso central y riñón.
El FMO transcurre clínicamente en tres fases [7]
1. Órgano de choque: El mecanismo patofisiológico desencadenante es un déficit de perfusión de distinta génesis. Este acontecimiento se produce en el plazo de horas y todavía no deja daños permanentes.
2. Disfunción orgánica: Un déficit de perfusión persistente en el plazo de los siguientes días conduce a la formación de un SRIS (síndrome de respuesta inflamatoria sistémica, de Systemic Inflammatory Response Syndrome, clasificado según [8]) con edemas locales y lesiones celulares. Esta fase se designa síndrome de fallo multiorgánico (SFMO).
3. Fallo orgánico: El déficit de perfusión persistente conduce a estasis en el área visceral, por lo que se produce superinfección y translocación de las endotoxinas del intestino. Esto conduce a una potenciación de los síntomas clínicos y al cuadro completo de sepsis. De la disfunción orgánica resulta un fallo orgánico.
El SFMO y el FMO son cuadros clínicos con una complicada patofisiología. Hasta hoy en día sólo se han entendido insuficientemente las exactas causas moleculares de la aparición y la complejidad de la respuesta huésped inmunológica-inflamatoria en infección grave y traumatismo que puede conducir al desencadenamiento de un SRIS y a las correspondientes repercusiones cardiocirculatorias [9].
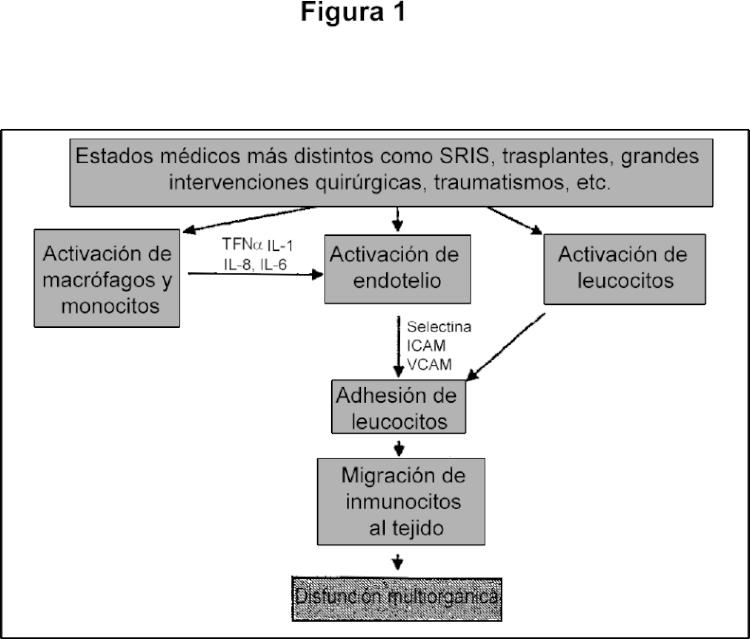
El SFMO y el FMO pueden ser de génesis tanto infecciosa como no infecciosa. El SFMO y el FMO aparecen regularmente como complicación clínicamente importante en pacientes con sepsis, después de choque traumático, en pacientes después de operaciones utilizando el sistema de circulación extracorporal, después de trasplantes de órganos, y otros (Figura 1). Un importante patomecanismo para la aparición del SFMO y el FMO es el desarrollo de un síndrome inflamatorio sistémico (SRIS, [8]). Los procesos patofisiológicos iniciados en el marco de un SRIS no implican sólo todos los componentes del sistema inmunitario, sino que perjudican al aparato cardiocirculatorio en todos los niveles y no sólo se limitan a depresión miocárdica y vasodilatación. Los cambios cardiocirculatorios, sobre todo en el plano de la microcirculación, forman la distancia final común y producen una hipoxia de tejidos que se considera un cofactor importante en la patogénesis del fallo multiorgánico.
La Figura 1 describe a modo de ejemplo los mecanismos más importantes desde el punto de vista actual de la aparición del SFMO y el FMO [10]: un sistema inmunitario hiperactivo parece que desempeña una función central en la aparición del fallo multiorgánico. A este respecto, el endotelio asume una función clave central mediante la secreción de citocinas mediante la mediación de la adhesión de leucocitos. En las células endoteliales se activan cascadas de transducción de señales que por último lugar conducen a la expresión y a la activación de factores de transcripción.
El conocimiento todavía incompleto de los procesos en la fase temprana del SFMO y el FMO es el motivo por el que hasta hoy en día no existe ningún diagnóstico sensible/específico que pueda discriminar entre causas infecciosas y no infecciosas. Los novedosos biomarcadores y diagnósticos, a partir de ahora también en el plano de la expresión génica, pueden proporcionar informaciones diagnósticas esenciales para el reconocimiento temprano de fallo multiorgánico, así como para diferenciar entre causas infecciosas y no infecciosas, de un SFMO y un FMO, y además representan una contribución importante para la aclaración de los mecanismos patofisiológicos de inflamaciones sistémicas.
Los síntomas tempranos frecuentemente usados clínicamente como fiebre, leucocitosis, taquicardia y taquipnea son completamente inespecíficos en el diagnóstico de un SFMO o un FMO, así como en la diferenciación entre causas infecciosas y no infecciosas de un SFMO y un FMO. Los parámetros que registran precozmente los trastornos de la microcirculación como cambios de pH de la mucosa intestinal [11] y el nivel de lactato en el lecho capilar [12,13], la aparición de un fallo respiratorio cuya causa no se encuentra en los pulmones [2], la subida de leucocitoselastasa [14,15], la altura del nivel de neopterina [16], la activación de leucocitos polimorfonucleares y la altura del nivel de IL-6 [17] son adecuados con limitaciones como parámetros tempranos para la aparición tardía de SFMO e FMO, pero pueden no contribuir a la diferenciación entre causas infecciosas y no infecciosas de un SFMO y un FMO. Por tanto, existe una necesidad urgente de un nuevo procedimiento diagnóstico que mejore la capacidad del experto para diferenciar precozmente SFMO o FMO no infeccioso de infeccioso y para obtener información de la respuesta a tratamientos específicos.
Pero precisamente la diferenciación entre causas infecciosas y no infecciosas de un SFMO y una FMO es de suma importancia médica ya que mediante una diferenciación tal pueden utilizarse más específicamente, por ejemplo, antibióticos, lo que, además de evitar efectos secundarios debido a la utilización inespecífica de antibióticos, también contribuye a un considerable ahorro de costes. Igualmente, en el caso de presencia de un SFMO o un FMO no infeccioso pueden evitarse medidas diagnósticas muy estresantes para los pacientes, así como que requieren mucho tiempo y personal (por ejemplo, transporte al CT/MRI), para la identificación del sitio de infección respectivo, la realización de amplios procedimientos microbiológicos (por ejemplo, la investigación de cultivos de sangre que también está asociada a la extracción de grandes... [Seguir leyendo]
Reivindicaciones:
1. Uso de polinucleótidos que se seleccionan del grupo constituido por: SEQ ID I.1, SEQ ID I.2, SEQ ID I.3, SEQ ID I.4, SEQ ID I.5, SEQ ID I.6, SEQ ID I.7, SEQ ID I.8 y SEQ ID I.9 o secuencias parciales de los mismos con una longitud de 20 a 200 nucleótidos como marcadores de actividad génica para la clasificación de pacientes como “no infectados sin fallo multiorgánico” o como “no enfermos de fallo multiorgánico infeccioso” o como “enfermos de fallo multiorgánico infeccioso”.
2. Uso según la reivindicación 1, en el que las secuencias parciales de los polinucleótidos tienen una longitud de 20-80 nucleótidos.
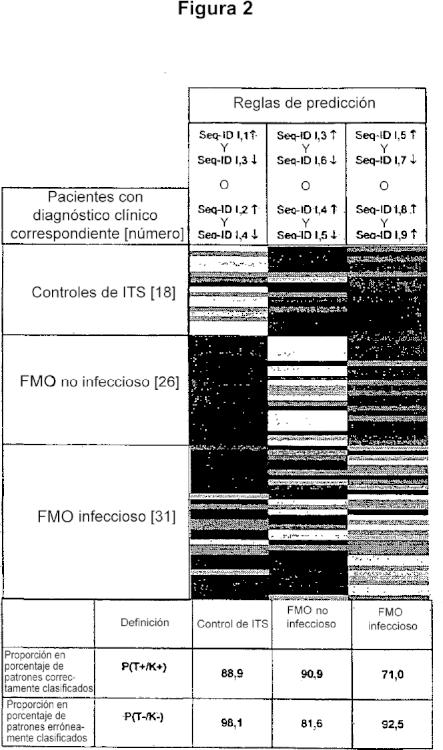
3. Uso según la reivindicación 1-2, caracterizado porque una expresión en exceso de SEQ ID I.1 y una expresión en defecto de SEQ ID I.3 o una expresión en exceso de SEQ ID I.2 y una expresión en defecto de SEQ ID I.4 indica la clasificación “ninguna infección y sin fallo multiorgánico”;
una expresión en exceso de SEQ ID I.3 y una expresión en defecto de SEQ ID I.6 o una expresión en exceso de SEQ ID.I,4 y una expresión en defecto de SEQ ID I.5 indica la clasificación “fallo multiorgánico no infeccioso”;
una expresión en exceso de SEQ ID I.5 y una expresión en defecto de SEQ ID I.7 o una expresión en exceso de SEQ ID
I.8 y una expresión en defecto de SEQ ID I.9 indica la clasificación “fallo multiorgánico infeccioso”.
4. Uso según la reivindicación 1-3, caracterizado porque las secuencias o las secuencias parciales de polinucleótidos se sustituyen al menos parcialmente por análogos sintéticos, aptámeros y/o ácidos nucleicos de péptidos.
5. Uso según la reivindicación 1-4 en una micromatriz.
6. Procedimiento para la clasificación de pacientes que están enfermos de un fallo multiorgánico infeccioso o no infeccioso que comprende las etapas:
aislar ARNm de una muestra de paciente;
marcar el ARNm con una unidad detectable;
poner en contacto el ARNm marcado con los marcadores de actividad génica según la reivindicación 1 de manera que los marcadores de actividad génica individuales también estén presentes separados entre sí después de la puesta en contacto;
lavar los marcadores de actividad génica hibridados;
estimular la unidad detectable de manera que ésta emita una señal;
leer las señales de hibridación para cada marcador de actividad génica individual y comparar con una muestra de referencia de un paciente sano,
indicando una expresión en exceso de SEQ ID I.1 y una expresión en defecto de SEQ ID I.3 o una expresión en exceso de SEQ ID I.2 y una expresión en defecto de SEQ ID I.4 la clasificación “ninguna infección y sin fallo multiorgánico”;
indicando una expresión en exceso de SEQ ID I.3 y una expresión en defecto de SEQ ID I.6 o una expresión en exceso de SEQ ID I.4 y una expresión en defecto de SEQ ID I.5 la clasificación “fallo orgánico no infeccioso”; y
indicando una expresión en exceso de SEQ ID I.5 y una expresión en defecto de SEQ ID I.7 o una expresión en exceso de SEQ ID I.8 y una expresión en defecto de SEQ ID I.9 la clasificación “fallo multiorgánico infeccioso”.
7. Procedimiento según la reivindicación 6, caracterizado porque la muestra de paciente comprende fluidos corporales, especialmente sangre, líquido cefalorraquídeo, orina, líquido ascítico, líquido seminal, saliva, líquido de punción, contenido celular o una mezcla de los mismos.
8. Procedimiento según la reivindicación 6 ó 7, en el que el procedimiento se realiza con una micromatriz.
9. Micromatriz para la clasificación de pacientes con fallo multiorgánico infeccioso o no infeccioso constituida por polinucleótidos con las secuencias SEQ ID I.1, SEQ ID I.2. SEQ ID I.3, SEQ ID I.4, SEQ ID I.5. SEQ ID I.6, SEQ ID I.7, SEQ ID I.8 y SEQ ID I.9 o secuencias parciales de los mismos con una longitud de 20 a 200 nucleótidos.
10. Dispositivo para la clasificación de pacientes con fallo multiorgánico infeccioso o no infeccioso que comprende;
un módulo para la preparación de muestras de la muestra de paciente obtenida in vitro, un módulo para la hibridación de la muestra de paciente con sondas de actividad génica que se derivan de los clasificadores de actividad génica constituido por clasificadores de actividad génica con las secuencias SEQ ID I.1, SEQ ID I.2, SEQ ID I.3, SEQ ID
I.4, SEQ ID I.5, SEQ ID I.6, SEQ ID I.7, SEQ ID I.8 y SEQ ID I.9 o secuencias parciales de las mismas con una longitud de 20 a 200 nucleótidos,
un módulo para la lectura de las señales de hibridación,
un módulo para el análisis de imágenes de las señales de hibridación leídas,
un módulo que hace posible la comparación automática con clasificadores de actividad génica guardados de pacientes sanos y
un módulo que hace posible la visualización de la comparación resultante.
Patentes similares o relacionadas:
MODULADORES DEL PESO CORPORAL, ÁCIDOS NUCLEICOS Y PROTEÍNAS CORRESPONDIENTES, Y USOS DIAGNÓSTICOS Y TERAPÉUTICOS DE LOS MISMOS, del 17 de Febrero de 2012, de THE ROCKEFELLER UNIVERSITY: LA PRESENTE INVENCION SE REFIERE GENERALMENTE AL CONTROL DEL PESO CORPORAL DE ANIMALES INCLUIDOS MAMIFEROS Y HUMANOS, Y EN CONCRETO A MATERIALES […]
POLIMORFISMOS DE VEGF Y TERAPIA ANTI-ANGIOGÉNESIS, del 17 de Enero de 2012, de GENENTECH, INC.: Método para predecir si un paciente se encuentra con un mayor riesgo de hipertensión asociada con el tratamiento con un antagonista de VEGF, que comprende cribar […]
MÉTODO DE DIAGNÓSTICO Y DE SEGUIMIENTO DE UNA VAGINOSIS BACTERIANA MEDIANTE CUANTIFICACIÓN MOLECULAR, del 28 de Diciembre de 2011, de UNIVERSITE DE LA MEDITERRANEE, AIX-MARSEILLE II: Método de diagnóstico y de seguimiento in vitro del estado de la flora bacteriana vaginal frente a la presencia de una vaginosis bacteriana […]
DETECCIÓN DE GÉRMENES ASOCIADOS A PERIODONTITIS, del 9 de Diciembre de 2011, de GREINER BIO-ONE GMBH: Procedimiento para la detección y/o para la determinación de bacterias asociadas a periodontitis de una muestra biológica, que comprende las etapas i) obtención […]
CONFORMACIÓN DE ADN (ESTRUCTURAS DE BUCLE) EN EXPRESIÓN GÉNICA NORMAL Y ANORMAL, del 22 de Noviembre de 2011, de ISIS INNOVATION LIMITED: Procedimiento de diagnóstico de un cancer por detección de expresión genica anormal en un individuo que comprende determinar en una muestra del individuo […]
USO DE POLIMORFISMOS GENÉTICOS QUE SE ASOCIAN CON LA EFICACIA DEL TRATAMIENTO DE UNA ENFERMEDAD INFLAMATORIA, del 4 de Noviembre de 2011, de NOVARTIS AG NOVARTIS PHARMA GMBH: Uso de pimecrolimus en la fabricación de un medicamento para el tratamiento de dermatitis atópica pediátrica en una población seleccionada de pacientes, en donde la población […]
MÉTODOS PARA EVALUAR ESTADOS PATOLÓGICOS USANDO ARN EXTRACELULAR, del 2 de Noviembre de 2011, de ONCOMEDX INC: Método para detectar, diagnosticar o monitorizar una lesión de un órgano en un ser humano, comprendiendo el método la etapa de detectar cualitativa o cuantitativamente […]
MÉTODOS DE TRATAMIENTO DE PSICOSIS Y ESQUIZOFRENIA BASADOS EN POLIMORFISMOS DEL GEN DEL CNTF, del 23 de Agosto de 2011, de NOVARTIS AG: Un método para determinar la capacidad de respuesta de un individuo con un trastorno psicótico al tratamiento con Iloperidona, que comprende; […]