PROCEDIMIENTO DE DEGRADACIÓN DE UNA PROTEÍNA DIFÍCILMENTE DEGRADABLE.
Un procedimiento ex vivo para digerir una proteína prión patógena,
que comprende la etapa de poner en contacto la proteína prión patógena con una enzima seleccionada entre el grupo constituido por - una enzima que comprende la secuencia de aminoácidos de la SEC ID Nº: 2; y - una enzima homóloga que muestra una actividad de digerir la proteína prión patógena, y que comprende una secuencia de aminoácidos que tiene un 95% o más de homología con la secuencia de aminoácidos de la SEC ID Nº: 2
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2003/013658.
Solicitante: MEIJI SEIKA KAISHA, LTD..
Nacionalidad solicitante: Japón.
Dirección: 4-16, KYOBASHI 2-CHOME, CHUO-KU TOKYO 104-8002 JAPON.
Inventor/es: MIWA,Takehiro, NISHIZAWA,Koji, HAYASHI,Yoshie, WATANABE,Manabu, MURAYAMA,Yuichi, YOSHIOKA,Miyako, MIURA,Katsuhiro.
Fecha de Publicación: .
Fecha Solicitud PCT: 24 de Octubre de 2003.
Clasificación Internacional de Patentes:
- A23B4/22 NECESIDADES CORRIENTES DE LA VIDA. › A23 ALIMENTOS O PRODUCTOS ALIMENTICIOS; SU TRATAMIENTO, NO CUBIERTO POR OTRAS CLASES. › A23B CONSERVACION, P.EJ. MEDIANTE ENLATADO, DE CARNE, PESCADO, HUEVOS, FRUTAS, VERDURAS, SEMILLAS COMESTIBLES; MADURACION QUIMICA DE FRUTAS Y VERDURAS; PRODUCTOS CONSERVADOS, MADURADOS O ENLATADOS. › A23B 4/00 Métodos generales de conservación para carne, embutidos, pescado o productos a base de pescado. › Microorganismos; Enzimas.
- C12N9/56 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › Bacillus subtilis o Bacillus licheniformis.
- C12P21/06 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
Clasificación PCT:
Clasificación antigua:
- C12N1/00 C12N […] › Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356310_T3.pdf

Fragmento de la descripción:
CAMPO TÉCNICO
La presente invención se refiere a un agente para digerir una proteína altamente resistente a desnaturalización y degradación (particularmente una proteína prión patógena) y un procedimiento para digerir la proteína.
ANTECEDENTES DE LA INVENCIÓN
Una proteína prión patógena en enfermedades tales como temblor en ovejas o ratones, enfermedad de Creutzfeldt-Jakob (CJD) en seres humanos, y encefalopatía bovina espongiforme (BSE; popularmente conocida como la enfermedad de las vacas locas) en ganado da lugar a síntomas nerviosos tal como distasia o disbasia. Hay que observar que el consumo humano de carne de vaca infectada con la proteína prión patógena puede provocar una variante de enfermedad de Creutzfeldt-Jakob (vCJD) por infección. En particular, la BSE es una enfermedad extremadamente grave a la luz de un suministro seguro de carne de vaca para el consumo humano.
Tales enfermedades se pueden desarrollar cuando la proteína prión patógena transferida en el cuerpo humano desde el exterior provoca un cambio conformacional de una proteína prión normal en general localizada en el cerebro [Nature, (Gran Bretaña), 1994, Vol. 370, p. 471 (referencia no patente 1)]. Para evitar el desarrollo de la enfermedad por una infección de la proteína prión patógena, es necesario digerir y destoxificar la proteína prión patógena como una causa de la misma hasta el grado que la enfermedad no se desarrolle.
Sin embargo, la proteína prión patógena se cree que es extremadamente estable cuando se somete a un tratamiento de esterilización usado comúnmente (tal como ebullición) y muestra o poca o ninguna pérdida de infectividad por el tratamiento de esterilización. Además, aunque el patógeno sea una proteína, no es difícil digerir el patógeno completamente con una proteasa de manera convencional. En estas circunstancias, se desean un procedimiento para digerir la proteína prión patógena de manera eficaz y un procedimiento para prevenir que las enfermedades se desarrollen por infección.
Como un procedimiento para digerir una proteína altamente resistente a la desnaturalización y degradación tal como una proteína prión patógena, por ejemplo, la Publicación de Patente No examinada Japonesa (Kokai) Nº 6 - 46871 (referencia de patente 1) describe un procedimiento para digerir proteínas que contienen queratina altamente resistentes a proteasas convencionales, usando queratinasa, una proteasa, derivada de Bacillus licheniformis PWD-1. La publicación describe que la queratinasa se usa en la digestión de las proteínas que contienen queratina (por ejemplo, pelo animal, pelo humano, o plumas), pero ni describe ni sugiere ningún efecto de la queratinasa sobre una proteína prión patógena.
A este respecto, se obtuvo un ADN que codifica la queratinasa derivada de Bacillus licheniformis PWD-1 [Publicación Internacional No examinada (Kohyo) Nº 10 - 500863 (referencia de patente 2)].
Además, la Patente de Estados Unidos Nº 6.613.505 (referencia de patente 3) describe que la queratinasa derivada de Bacillus licheniformis PWD-1 se usa en la digestión de una proteína prión patógena altamente resistente a desnaturalización y degradación. Sin embargo, para reducir o digerir la proteína prión patógena mediante el procedimiento descrito en la Patente de Estados Unidos Nº 6.613.505, dos etapas de tratamiento, esto es, un tratamiento por calor como un pretratamiento, y un tratamiento de enzima, son necesarios. En este procedimiento, es necesario un aparato para calendar si es necesario, y de este modo no es fácil llevar a cabo el procedimiento en instalaciones comunes sin tal aparato de calentamiento. Además, los procedimientos de dos etapas se complican.
Además, la Publicación Internacional Nº 02/053723 (referencia de patente 4) describe que una proteasa resistente al calor se usa en la digestión de una proteína prión patógena. Sin embargo, describe que cuando una proteína prión patógena se digirió por una proteasa derivada de Bacillus thermoproteolytics Rokko descrita en sus Ejemplos, la proteína prión patógena no se digirió suficientemente con la proteasa sola, pero no se digirió suficientemente con la proteasa en la presencia de dodecil sulfato sódico. Además, es necesaria una sal neutra para activar la proteasa. Además, la proteasa requiere un ion metálico, y de este modo cuando está presente un agente quelante en una reacción, la actividad disminuye notablemente.
(referencia de no patente 1) Nature, (Gran Bretaña), 1994, Vol. 370, p. 471 (referencia de patente 1) Publicación de Patente Japonesa no Examinada (Kokai) Nº 6-46871 (referencia de patente 2) Publicación Internacional No examinada (Kohyo) Nº 10500863 (referencia de patente 3) Patente de Estados Unidos Nº 6.613.505
(referencia de patente 4) Publicación Internacional Nº 02/053723
El documento W098/30682A1 describe una enzima que es adecuada para el cuidado de la piel y describe con subtilisina DY (SEC ID Nº: 3) una enzima que es idéntica a la enzima que se usa de acuerdo con esta solicitud. La subtilisina DY se especifica como una proteasa. El documento W002/083082A2 describe una queratinasa PWD-1 para digerir las proteínas de priones.
DESCRIPCIÓN DE LA INVENCIÓN
Un objetivo de la presente invención es proporcionar un procedimiento para destoxificar una proteína prión patógena, usando una enzima.
Los presentes inventores encontraron una enzima que muestran una actividad extremadamente alta de digerir una proteína fuertemente resistente a desnaturalización y degradación (particularmente una proteína prión patógena) derivada de un microorganismo que pertenece al género Bacillus, en comparación con las enzimas conocidas para digerir un proteína altamente resistente a desnaturalización y degradación.
La enzima que se puede usar en la presente invención mostró excelentes propiedades, como se muestra en los Ejemplos descritos más adelante, en comparación con las enzimas mencionadas anteriormente reseñadas previamente para usar en la digestión de una proteína prión patógena, por ejemplo, la enzima (queratinasa) preparada a partir de Bacillus licheniformis PWD-1 descrito en la Patente de Estados Unidos Nº 6.613.505, y la enzima preparada a partir de Bacillus thermoproteolyticus Rokko descrito en la Publicación Internacional Nº 02/053723.
Particularmente, se encontró que la enzima que se puede usar en la presente invención mostró una actividad extremadamente alta de digerir una proteína prión patógena en comparación con la enzima preparada a partir de Bacillus licheniformis PWD-1 (véanse los Ejemplos 7 y 8). Además, sorprendentemente se encontró que la proteína se digirió sin un tratamiento térmico descrito en la Patente de Estados Unidos Nº 6.613.505 (véanse los Ejemplos 7 y 8).
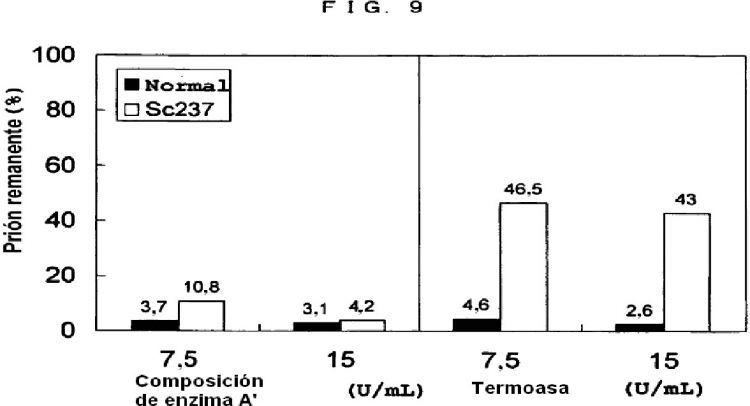
En comparación con la enzima preparada a partir de Bacillus thermoproteolyticus Rokko, se encontró que la enzima que se puede usar en la presente invención mostró una actividad extremadamente alta de digerir una proteína prión patógena (véanse los Ejemplos 9 to 11). Además, sorprendentemente se encontró que la proteína mostró una excelente actividad de digerir una proteína prión patógena independientemente de la presencia de dodecil sulfato sódico (véanse los Ejemplos 9 a 11).
La presente invención se refiere a un procedimiento ex vivo para digerir una proteína prión patógena, que comprende la etapa de poner en contacto la proteína prión patógena con una enzima seleccionada entre el grupo constituido por una enzima que comprende la secuencia de aminoácidos de la SEC ID Nº: 2; y una enzima homóloga que muestra una actividad de digerir la proteína prión patógena, y que comprende una secuencia de aminoácidos que tienen un 95% o más de homología con la secuencia de aminoácidos de la SEC ID Nº: 2.
Además, la invención se refiere al uso ex vivo de la enzima descrita anteriormente para digerir una proteína prión patógena.
Finalmente, la invención se refiere a un procedimiento ex vivo para destoxificar una proteína prión patógena, que comprende la etapa de poner en contacto una materia sujeto que se puede contaminar con una proteína prión patógena con la enzima descrita anteriormente
La enzima usada en la invención muestra una actividad de digerir una proteína altamente resistente a desnaturalización y degradación y tiene las siguientes propiedades: (a) actividad y especificidad de... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento ex vivo para digerir una proteína prión patógena, que comprende la etapa de poner en contacto la proteína prión patógena con una enzima seleccionada entre el grupo constituido por
5 - una enzima que comprende la secuencia de aminoácidos de la SEC ID Nº: 2; y
- una enzima homóloga que muestra una actividad de digerir la proteína prión patógena, y que comprende una secuencia de aminoácidos que tiene un 95% o más de homología con la secuencia de aminoácidos de la SEC ID Nº: 2.
2. Un uso ex vivo de la enzima descrita en la reivindicación 1 para digerir una proteína 10 prión patógena.
3. Un procedimiento ex vivo para destoxificar una proteína prión patógena, que comprende la etapa de poner en contacto una materia sujeto que puede estar contaminada con una proteína prión patógena con la enzima descrita en la reivindicación 1.
5. El procedimiento ex vivo de acuerdo con la reivindicación 4, en el que la etapa de poner en contacto se lleva a cabo sin precalentamiento de la materia sujeto a 90ºC o más. 15 4. El procedimiento ex vivo de acuerdo con la reivindicación 3, en el que la etapa de poner en contacto se lleva a cabo sin precalentamiento de la materia sujeto.
20 6. Un uso ex vivo de la enzima descrita en la reivindicación 1 para destoxificar una proteína prión patógena.
Patentes similares o relacionadas:
 Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
 Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Uso de tripeptidil peptidasas tolerantes a la prolina en composiciones de aditivo para piensos, del 26 de Febrero de 2020, de Dupont Nutrition Biosciences ApS: Un método para preparar una composición de aditivo para piensos que comprende: mezclar al menos una tripeptidil peptidasa tolerante a la prolina que tiene […]
Enzimas específicas de sitio y métodos de uso, del 19 de Febrero de 2020, de Poseida Therapeutics, Inc: Un polipéptido que comprende al menos una secuencia de aminoácidos que tiene la secuencia de LSTEQVVAIASX1X2GGKQALEAVKAQLLVLRAAPYE (SEQ ID NO: 1), en donde […]
Composiciones para unir módulos de dedos de cinc, del 15 de Enero de 2020, de Sangamo Therapeutics, Inc: Una proteína de dedos de cinc de múltiples dedos que se une específicamente a un sitio diana, comprendiendo la proteína de dedos de cinc de […]
Concentrado de proteínas de granos que contienen almidón: composición, método de fabricación y usos del mismo, del 1 de Enero de 2020, de THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF AGRICULTURE: Un proceso para producir un concentrado de proteinas a partir de un grano o semilla oleaginosa que contiene almidon, el proceso comprende: (i) moler el […]
 Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
 Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]
Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]