PROCEDIMIENTO DE PREPARACIÓN DE SOLIFENACINA.
Procedimiento de preparación de carboxilato de (1S)-(3R)-1-azabiciclo[2.
2.2]oct-3-il 3,4-dihidro-1-fenil- 2(1H)-isoquinolina (solifenacina) o sus sales farmacéuticamente aceptables con elevada pureza óptica, caracterizado porque la base de solifenacina en bruto se convierte a tartrato ácido, que a continuación se convierte opcionalmente a otra sal farmacéuticamente aceptable o la base de solifenacina.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CZ2007/000119.
Solicitante: ZENTIVA, K.S.
Nacionalidad solicitante: República Checa.
Dirección: U KABELOVNY 130 DOLNI MECHOLUPY 102 37 PRAHA 10 REPUBLICA CHECA.
Inventor/es: JIRMAN,Josef , JUNEK,Richard.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D453/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › Compuestos heterocíclicos que contienen sistemas cíclicos de quinuclidina o isoquinuclidina, p. ej. alcaloides de quinina.
PDF original: ES-2375668_T3.pdf
Fragmento de la descripción:
Procedimiento de preparación de solifenacina.
SECTOR TÉCNICO
La presente invención se refiere a un nuevo procedimiento de preparación de carboxilato de (1S) - (3R) -1azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina (solifenacina) de fórmula III, que se utiliza para el tratamiento sintomático de la incontinencia urgente y/o aumento de la frecuencia de orinar y la urgencia de orinar en pacientes con vejiga hiperactiva.
ANTECEDENTES DE LA INVENCIÓN
La literatura de patentes originales (EP 0 801 067, WO 9620194) describe varios procedimientos de preparación de solifenacina.
El primer procedimiento consiste en la reacción de carboxilato de (1S) -etil 1-fenil-1, 2, 3, 4-tetrahidro-2-isoquinolina de fórmula II con 3- (R) -quinuclidol de fórmula I en una suspensión de tolueno y en presencia de hidruro de sodio. La mezcla reaccionante se lleva hasta reflujo con destilación simultánea del etanol que se forma, que se obtiene en forma de una mezcla azeotrópica con tolueno.
Otro procedimiento de preparación que se describe en la patente es la reacción de cloruro de 1-fenil-1, 2, 3, 4tetrahidro-2-isoquinolina carbonilo de fórmula IV con 3-quinuclidol de fórmula V en dimetilformamida, que produce carboxilato de 1-azabiciclo [2.2.2.]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina de fórmula VI.
En el documento EP 0 801 067 ó WO 9620194 se publica otra versión, en la que se hace reaccionar carbonato de 3 (R) -quinuclidilo alquilo con 1-fenil-1, 2, 3, 4-tetrahidro-2-isoquinolina para obtener solifenacina. La solifenacina en bruto obtenida mediante la utilización de uno de los procedimientos de preparación mencionados anteriormente se purifica posteriormente en forma de hidrocloruro u oxalato y durante su purificación por cristalización a partir de los materiales iniciales que no reaccionan aparecen productos secundarios. Sin embargo, el efecto de purificación de la transformación a estas sales es pequeño. Para alcanzar una pureza adecuada para la preparación del producto final, succinato de solifenacina, que se utiliza para la preparación de medicamentos, la cristalización de HCl u oxalato debe repetirse varias veces, lo que naturalmente reduce el rendimiento. El documento EP 1 714 965 da a conocer un procedimiento para reducir las impurezas de solifenacina mediante la preparación de la sal succinato. El documento JP 52 108992 utiliza ácido tartárico en la purificación de cefalexina.
DESCRIPCIÓN DE LA INVENCIÓN
La presente invención da a conocer un nuevo procedimiento de preparación de carboxilato de (1S) - (3R) -1azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina (solifenacina) ópticamente puro o sus sales 50 farmacéuticamente aceptables, que consiste en la preparación de tartrato ácido de solifenacina en forma cristalina. La presente invención se basa en el efecto excepcionalmente bueno de purificación de la transformación de la base en bruto al tartrato ácido mediante la acción de ácido L-tartárico y posterior aislamiento del tartrato ácido de solifenacina cristalino. El procedimiento de la presente invención puede ser utilizado para la purificación de solifenacina preparada mediante cualquier procedimiento de preparación conocido, en particular para la solifenacina 55 preparada mediante la reacción de carboxilato de (1S) -alquil 1-fenil-1, 2, 3, 4-tetrahidro-2-isoquinolina con s 3- (R) quinuclidol con catálisis de una base no nucleofílica. El tartrato ácido de solifenacina no se ha preparado ni caracterizado hasta ahora. El tartrato ácido de solifenacina cristalino es una sal estable que se puede transformar en otra sal de solifenacina farmacéuticamente aceptable, por ejemplo, succinato, o se puede utilizar directamente en la preparación de un medicamento. Esta sal se ha caracterizado mediante rayos X, DSC y procedimientos de espectroscopía IR, y CP-MAS 13C-RMN. El procedimiento de la presente invención puede realizarse, por ejemplo, de la siguiente manera: Una mezcla de reacción con solifenacina en bruto, preparada mediante cualquier procedimiento conocido (véase más arriba) se enfría después de lograr la conversión y se añade agua a la mezcla. Después de la separación de la fase orgánica, la capa acuosa se lava con otra porción del disolvente orgánico. Los extractos orgánicos combinados se lavan con agua, solución salina y por último con agua otra vez. Posteriormente, la capa orgánica se evapora hasta sequedad. Después de esta purificación, aún permanecen en la mezcla de reacción algunas impurezas, tales como carboxilato de (1R) - (3R) -1-azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina, carboxilato de (1S) - (3S) -1-azabiciclo [2.2.2] oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina y 1 (S) -fenil-1, 2, 3, 4-tetrahidroisoquinolina.
Como la purificación de solifenacina mediante su cristalización en forma de la sal de hidrocloruro u oxalato ha mostrado baja eficiencia, se realizó un esfuerzo para encontrar una manera más adecuada de purificación de la solifenacina en bruto. Lo que demostró ser más adecuado fue convertir la base de solifenacina a succinato mediante la acción de ácido succínico. Sin embargo, el mayor efecto de limpieza, por mucho, se logró con la conversión de la base de solifenacina en bruto a sal cristalina de tartrato ácido mediante la acción del ácido L-tartárico. La forma cristalina del tartrato ácido de carboxilato de (1S) - (3R) -1-azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H)
isoquinolina se ha caracterizado mediante el procedimiento del patrón de difracción de rayos X (señales en 3, 9, 11, 6, 12, 1, 13, 9, 17, 8, 19, 5 y 24, 5 ± 0, 2 grados 28) y por procedimientos de espectroscopía IR y CP-MAS 13C-RMN y DSC (1 pico a 200, 0 º C) (figuras 1 a 4) .
El procedimiento que ha demostrado representar la forma más eficiente de preparación de solifenacina es el procedimiento que comprende: la preparación de base de solifenacina mediante reacción de carboxilato de (1S) alquil 1-fenil-1, 2, 3, 4-tetrahidro-2-isoquinolina con 3- (R) -quinuclidol catalizada por una base no nucleofílica (Esquema 1) , además del aislamiento de la base en bruto y la posterior purificación final, que consiste en la transformación de la base de solifenacina a tartrato ácido mediante la acción del ácido L-tartárico en el medio de un disolvente polar o mezcla de disolventes polares y el aislamiento del tartrato ácido de solifenacina cristalino. La sal pura de tartrato ácido de solifenacina preparada de esta manera se puede transformar en succinato de solifenacina utilizado comúnmente de forma farmacéutica, o utilizado directamente para la preparación de un medicamento.
Una base no nucleofílica es una base que tiene considerablemente reducida la capacidad de sustitución nucleofílica. Generalmente este es el caso de alcoholatos o aminas con impedimento estérico, además de compuestos de litio o del grupo de sustancias llamadas fosfacenos, en particular, por ejemplo, tert-butóxido de potasio, tert-butóxido de sodio, tert-butil-litio, LDA, K-HMDS, DBU, DBN, 2, 6-di-terc-butil-4-metilpiridina, base P1-t-Bu, BEMP, BTPP y base P2-t-Bu mientras que son especialmente adecuados terc-butóxido de potasio y terc-amilato de sodio o potasio. Del grupo de disolventes polares para la preparación y aislamiento del tartrato ácido es más adecuado utilizar alcoholes C1-C4, sus mezclas y posiblemente sus combinaciones con agua.
45 El tartrato de solifenacina se puede preparar de forma alternativa de manera que se añade ácido L-tartárico directamente a la fase orgánica con la base de solifenacina en bruto, es decir, sin aislamiento previo de la base, por ejemplo, de manera que se añade un equivalente de la solución saturada de ácido L-tartárico en un alcohol a la solución de la base en bruto en un disolvente no polar. El tartrato ácido de solifenacina es precipitado, succionado y 50 posteriormente se cristaliza de una manera habitual.
BREVE DESCRIPCIÓN DE LAS FIGURAS
La figura 1 representa un patrón de difracción XRPD de tartrato ácido de carboxilato de (1S) - (3R) -1azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina.
La figura 2 representa un espectro IR de tartrato ácido de carboxilato de (1S) - (3R) -1-azabiciclo[2.2.2]oct-3-il 3, 4dihidro-1-fenil-2 (1H) -isoquinolina.
La figura 3 representa un espectro CP-MAS 13C-RMN de tartrato ácido de carboxilato de (1S) - (3R) -1azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil-2 (1H) -isoquinolina.
La figura 4 representa una curva de DSC de tartrato ácido... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento de preparación de carboxilato de (1S) - (3R) -1-azabiciclo[2.2.2]oct-3-il 3, 4-dihidro-1-fenil2 (1H) -isoquinolina (solifenacina) o sus sales farmacéuticamente aceptables con elevada pureza óptica, caracterizado porque la base de solifenacina en bruto se convierte a tartrato ácido, que a continuación se convierte opcionalmente a otra sal farmacéuticamente aceptable o la base de solifenacina.
2. Procedimiento, según la reivindicación 1, caracterizado porque la base de solifenacina se convierte en tartrato ácido mediante la acción de ácido L-tartárico y posteriormente se aísla el tartrato ácido de solifenacina cristalino.
3. Procedimiento, según la reivindicación 2, caracterizado porque el tartrato ácido de solifenacina es recristalizado adicionalmente a partir de un disolvente polar o una mezcla de disolventes polares, preferentemente del grupo de alcoholes C1-C4 o sus combinaciones con agua.
4. Procedimiento, según las reivindicaciones 2 y 3, caracterizado porque la base de solifenacina en bruto se prepara mediante la reacción de carboxilato de (1S) -alquil 1-fenil-1, 2, 3, 4-tetrahidro-2-isoquinolina, en la que alquil se refiere a un alquilo primario C1-C4, con 3- (R) -quinuclidol en el medio de una base no nucleofílica.
5. Procedimiento, según la reivindicación 4, caracterizado porque se utiliza una base no nucleofílica del grupo de los alcoholatos o aminas con impedimento estérico, o compuestos de litio, o fosfacenos.
6. Procedimiento, según la reivindicación 5, caracterizado porque se utiliza terc-butanolate de potasio, sodio
o litio.
7. Procedimiento, según la reivindicación 5, caracterizado porque se utiliza terc-amilato de potasio o sodio.
8. Sal cristalina de tartrato ácido de solifenacina.
9. Sal cristalina, según la reivindicación 8, caracterizada porque el espectro de rayos X registra señales típicas en: 3, 9, 11, 6, 12, 1, 13, 9, 17, 8, 19, 5 y 24, 5 ± 0, 2 grados 28º
10. Sal cristalina, según la reivindicación 8, caracterizada porque el DSC registra una endoterma con el pico a 200, 0º C a la velocidad de calentamiento de 10º C/min.
11. Sal cristalina, según la reivindicación 8, caracterizada por las señales a 11, 2, 19, 6, 24, 7, 27, 1, 38, 1, 45, 8, 47, 4, 52, 9, 56, 4, 70, 1, 73, 7, 75, 3, 125, 7, 127, 9, 128, 8, 133, 7, 137, 2, 145, 2, 154, 6, 177, 0 ppm en el espectro CP/ 13C RMN MAS.
Patentes similares o relacionadas:
Compuestos de amida de quinuclidina sustituida geminal como agonistas de receptores alfa-7 nicotínicos de acetilcolina, del 2 de Octubre de 2019, de Axovant Sciences GmbH: Un compuesto de amida de quinuclidina sustituida geminal representado por la fórmula (I): **(Ver fórmula)** en donde el resto C(R1)(R2) forma un carbociclo (de […]
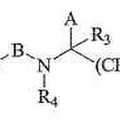 Agentes antibacterianos, del 13 de Junio de 2012, de NOVARTIS VACCINES AND DIAGNOSTICS, INC.: Un compuesto que tiene la fórmula II: **Fórmula**
o un estereoisómero, sal farmacéuticamente aceptable, o éster del mismo, en la queD-G-Y, tomadas conjuntamente, están seleccionados […]
Agentes antibacterianos, del 13 de Junio de 2012, de NOVARTIS VACCINES AND DIAGNOSTICS, INC.: Un compuesto que tiene la fórmula II: **Fórmula**
o un estereoisómero, sal farmacéuticamente aceptable, o éster del mismo, en la queD-G-Y, tomadas conjuntamente, están seleccionados […]
PROCEDIMIENTO PARA LA PRODUCCION DE AGENTES NEURORRECEPETORES MARCADOS CON YODO RADIOACTIO., del 1 de Junio de 2005, de MAP MEDICAL TECHNOLOGIES OY: La presente invención se refiere a un procedimiento para producir agentes neuroreceptores radioiodados con rendimientos mejorados. En el citado […]
COMPUESTOS HETEROCICLICOS., del 16 de Febrero de 2003, de ELI LILLY AND COMPANY: LA PRESENTE INVENCION PROPORCIONA COMPUESTOS HETEROCICLICOS QUE SON UTILES PARA LA MODULACION DE UN RECEPTOR MUSCARINICO.
DERIVADOS DE QUINUCLIDINA., del 16 de Febrero de 1995, de PFIZER INC.: LOS DERIVADOS DE LA QUINUCLIDINA CON LAS FORMULAS (I), (II) O (III) Y SUS SALES FARMACEUTICAMENTE ACEPTABLES, EN DONDE M, P, Z, Y, R1, R2 Y R3 SON LO DEFINIDO […]
NUEVOS DERIVADOS PEPTIDICOS, PROCEDIMIENTO PARA SU OBTENCION Y LAS COMPOSICIONES FARMACEUTICAS QUE LOS CONTIENEN., del 16 de Diciembre de 1994, de ADIR ET COMPAGNIE: LA INVENCION SE REFIERE A DERIVADOS DE FORMULA GENERAL (I), EN LA QUE A REPRESENTA CON LOS ATOMOS DE CARBONO Y DE NITROGENO CON LOS QUE ESTA UNIDO UN GRUPO CICLOAMIDICO; B REPRESENTA […]
DERIVADOS DE AZABICICLOOCTAN-3-ONA Y SU USO, del 3 de Enero de 2011, de APREA AB: Un compuesto seleccionado de **Fórmula** acetato de [2-(metoximetil)-3-oxo-1-azabiciclo[2.2.2]oct-2-il]metilo; **Fórmula** ciclopentanocarboxilato […]
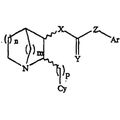 3-SUSTITUIDOS-2(ARILALQUIL)-1-AZABICICLOALCANOS Y METODOS DE USO DE LOS MISMOS, del 16 de Junio de 2008, de TARGACEPT, INC.: Un compuesto que tiene una estructura de las fórmulas: (Ver fórmula) en donde: m y n por separado son 1 ó 2, p es 1, 2, 3 ó 4, X es oxígeno o NR'', Y es oxígeno […]
3-SUSTITUIDOS-2(ARILALQUIL)-1-AZABICICLOALCANOS Y METODOS DE USO DE LOS MISMOS, del 16 de Junio de 2008, de TARGACEPT, INC.: Un compuesto que tiene una estructura de las fórmulas: (Ver fórmula) en donde: m y n por separado son 1 ó 2, p es 1, 2, 3 ó 4, X es oxígeno o NR'', Y es oxígeno […]