Polipéptidos que tienen actividad de alfa-glucosidasa y polinucleótidos que los codifican.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10157000.
Solicitante: NOVOZYMES, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1445 DREW AVENUE DAVIS, CA 95616 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HARRIS, PAUL, BLINKOVSKY,ALEXANDER, OTANI,SUZANNE, GE,HAIYAN, YAVER,DEBBIE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N1/20 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › Bacterias; Sus medios de cultivo.
- C12N15/00 C12N […] › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N9/30 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › de origen fúngico.
- C12P21/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
PDF original: ES-2545612_T3.pdf
Fragmento de la descripción:
Polipéptidos que tienen actividad de alfa-glucosidasa y polinucleótidos que los codifican.
Antecedentes de la invención 5
Campo de la invención
La presente invención se refiere a polipéptidos aislados que tienen actividad de alfa-glucosidasa y polinucleótidos aislados que codifican los polipéptidos. La invención también se refiere a constructos de ácidos nucleicos, vectores y 10 células huésped que comprenden los polinucleótidos así como métodos para producir y utilizar los polipéptidos.
Descripción de la técnica relacionada
Diferentes enzimas están implicadas en la degradación de almidón. 15
Las enzimas incluyen alfa-amilasa, beta-amilasa, amiloglucosidasa, pululanasa, isoamilasa, alfa-glucosidasa y ciclodextrina glucosiltransferasa.
Las alfa-glucosidasas (EC 3.2.1.20) hidrolizan residuos terminales no reductores alfa-1, 4-enlazados de glucosa en varios sustratos, liberando glucosa. Degradan rápidamente los disacáridos y oligosacáridos mientras que, de hacerlo, 20 atacan lentamente a los polisacáridos. La maltosa, los derivados de maltosa, sacarosa, aril-alfa-glucósidos y alquil-alfa-glucósidos pueden hacer de sustratos.
La purificación y propiedades de una alfa-glucosidasa de Aspergillus fumigatus ha sido descrita por Rudick y Elbein, 1974, Archives of Biochemistr y and Biophysics 161: 281-290. 25
Se ha informado de que otros hongos filamentosos producen alfa-glucosidasas, tales como Aspergillus flavus (Olutiola, 1981, Mycologia 73: 1130) , Aspergillus nidulans (Kato et al., 2002, Appl. Environ. Microbiol. 68: 1250-1256) , Aspergillus niger (Rudick et al., 1979, Archives of Biochemistr y and Biophysics 193: 509) , Aspergillus or y zae (Leibowitz and Mechlinski, 1926, Hoppe- Seyler's Zeitschrift fur Physiologische Chemie 154: 64) , Mucor javanicus (Yamasaki et al., 30 1978, Berichte des Ohara Instituts para Landwirtschaftliche Biologie 17: 123) , Mucor racemosus (Yamasaki et al., 1977, Agricultural and Biological Chemistr y 41: 1553) , Mucor rouxii (Flores-Carreon and Ruiz- Herrera, 1972, Biochemica et Biophyisica Acta 258: 496) , Penicillium pupurogenum (Yamasaki et al., 1976, Agricultural and Biological Chemistr y 40: 669) y Penicillium oxalicum (Yamasaki et al., 1977, Agricultural and Biological Chemistr y 41: 1451) .
Las alfa-glucosidasas se pueden usar en combinación con otras enzimas que degradan el almidón, por ejemplo, alfa-amilasa, para conseguir la hidrólisis completa del almidón en aplicaciones industriales donde es deseable la conversión en azúcares fermentables. En consecuencia, hay una necesidad en la técnica de alfa-glucosidasas alternativas con propiedades mejoradas tales como pH óptimo, temperatura óptima y termoestabilidad.
Es un objetivo de la presente invención el proporcionar polipéptidos que tienen actividad de alfa-glucosidasa y polinucleótidos que codifican los polipéptidos.
Resumen de la invención 45
La presente invención se refiere a un polipéptido aislado que tiene actividad de alfa-glucosidasa, donde el polipéptido tiene una secuencia de aminoácidos que tiene al menos un 90% de identidad con los aminoácidos 20 a 988 de la SEC ID nº 6.
La presente invención también se refiere a polinucleótidos aislados que comprenden una secuencia de 50 nucleótidos que codifica el polipéptido de la invención.
La presente invención también se refiere a constructos de ácidos nucleicos, vectores de expresión recombinantes y células huésped recombinantes que comprenden los polinucleótidos.
La presente invención también se refiere a métodos para producir polipéptidos de la invención que tienen actividad de alfa-glucosidasa que comprenden (a) cultivar una célula huésped recombinante que comprende un constructo de ácidos nucleicos que comprende un polinucleótido que codifica el polipéptido bajo condiciones propicias para la producción del polipéptido; y (b) recuperar del polipéptido.
Breve descripción de las figuras 60
La Figura 1 muestra la secuencia de ADN genómico y la secuencia de aminoácidos deducida de una alfa-glucosidasa de Aspergillus fumigatus (Agl1) (SEC ID nº 1 y 2, respectivamente) . 65
La Figura 2 muestra la secuencia de ADN genómico y la secuencia de aminoácidos deducida de una alfa-glucosidasa de Aspergillus fumigatus (Agl2) (SEC ID nº 3 y 4, respectivamente) .
La Figura 3 muestra la secuencia de ADN genómico y la secuencia de aminoácidos deducida de una alfa-glucosidasa de Aspergillus fumigatus (Agl3) (SEC ID nº 5 y 6, respectivamente) .
La Figura 4 muestra un mapa de restricción de pAILo1.
La Figura 5 muestra un mapa de restricción de pBM121b. 5
La Figura 6 muestra un mapa de restricción de pBM120a.
La Figura 7 muestra un mapa de restricción de pSMO216.
La Figura 8 muestra un mapa de restricción de pHyGe011.
La Figura 9 muestra un mapa de restricción de pJSF9b.
La Figura 10 muestra la dependencia del pH que tiene la actividad de la alfa-glucosidasa de Aspergillus fumigatus Agl1 10 purificada en tampón acetato 50 mM/tampón fosfato 50 mM a 37°C.
La Figura 11 muestra la termoestabilidad de la alfa-glucosidasa de Aspergillus fumigatus Agl1 purificada tras la incubación en acetato sódico pH 5, 0 y 0, 05 M durante 5 minutos a diferentes temperaturas.
La Figura 12 muestra la dependencia de la temperatura que tiene la actividad de la alfa-glucosidasa de Aspergillus fumigatus Agl1 purificada en acetato sódico pH 5, 0 y 50 mM. 15
La Figura 13 muestra la dependencia del pH que tiene la actividad de la alfa-glucosidasa de Aspergillus fumigatus Agl3 purificada en tampón acetato 50 mM/tampón fosfato 50 mM a 37°C.
La Figura 14 muestra la termoestabilidad de la alfa-glucosidasa de Aspergillus fumigatus Agl3 purificada tras la incubación en acetato sódico pH 5, 0 y 50 mM durante 5 minutos a diferentes temperaturas.
La Figura 15 muestra la dependencia de la temperatura que tiene la actividad de la alfa-glucosidasa de Aspergillus 20 fumigatus Agl3 purificada en acetato sódico pH 5, 0 y 50 mM.
Definiciones
Actividad de alfa-glucosidasa: el término "actividad de alfa-glucosidasa" se define en este documento como una 25 actividad de alfa-D-glucósido glucohidrolasa (E.C. 3.2.1.20) que cataliza la exohidrólisis de los residuos terminales no reductores 1, 4-enlazados de alfa-D-glucosa con la liberación de alfa-D-glucosa.
Los sustratos naturales de la actividad enzimática incluyen, por ejemplo, maltosa, maltotriosa, maltotetraosa, maltopentaosa, almidón (soluble) , amilosa, amilopectina, isomaltosa, kojibiosa, sacarosa, nigerosa, turanosa, melicitosa y glucógeno. Para los fines de la presente invención, la actividad de alfa-glucosidasa se determina con maltosa como 30 sustrato en tampón de acetato sódico 0, 1 M y pH 4, 3 a 25°C. Una unidad de actividad de alfa-glucosidasa se define como 1, 0 µmol de glucosa producida por minuto a 25°C y pH 4, 3 de maltosa como sustrato en tampón de acetato sódico.
Los polipéptidos de la presente invención tienen al menos un 20%, preferiblemente al menos un 40%, más 35 preferiblemente al menos un 50%, más preferiblemente al menos un 60%, más preferiblemente al menos un 70%, más preferiblemente al menos un 80%, incluso más preferiblemente al menos un 90%, de la forma más preferible al menos un 95% e incluso de forma más preferible al menos un 100% de la actividad de alfa-glucosidasa del polipéptido que consiste en la secuencia de aminoácidos mostrada como los aminoácidos 15 a 881 de la SEC ID nº 2, los aminoácidos 30 a 967 de la SEC ID nº 4 o los aminoácidos 20 a 988 de la SEC ID nº 6. 40
Polipéptido aislado: el término "polipéptido aislado" tal y como se usa en este documento se refiere a un polipéptido que es al menos un 20% puro, preferiblemente al menos un 40% puro, más preferiblemente al menos un 60%, puro incluso más preferiblemente al menos un 80% puro, de la forma más preferible al menos un 90% puro e incluso de forma más preferible al menos un 95% puro, tal y como se determina mediante SDS-PAGE. 45
Polipéptido sustancialmente puro: el término "polipéptido sustancialmente puro" denota en este documento un preparado de polipéptidos que contiene como mucho un 10%, preferiblemente como mucho un 8%, más preferiblemente como mucho un 6%, más preferiblemente como mucho un 5%, más preferiblemente como mucho un 4%, más preferiblemente como mucho un 3%, incluso más preferiblemente como mucho un 2%, de la forma más preferible como 50 mucho un 1% e incluso de forma más preferible como mucho un 0, 5% en peso de otro material polipeptídico con el cual está asociado originalmente o por recombinación.... [Seguir leyendo]
Reivindicaciones:
1. Polipéptido aislado que tiene actividad de alfa-glucosidasa, donde el polipéptido tiene una secuencia de aminoácidos que tiene al menos un 90% de identidad con los aminoácidos 20 a 988 de la SEC ID nº 6. 5
2. Polipéptido según la reivindicación 1, con una secuencia de aminoácidos que tiene al menos un 95%, al menos un 97% de identidad con los aminoácidos 20 a 988 de la SEC ID nº 6.
3. Polipéptido según cualquiera de las reivindicaciones 1-2, que comprende la secuencia de aminoácidos de la SEC ID 10 nº 6.
4. Polipéptido según cualquiera de las reivindicaciones 1-3, que consiste en la SEC ID nº 6; o fragmentos de la misma que tienen actividad de alfa-glucosidasa.
5. Polipéptido según las reivindicaciones 1-4, que consiste en la SEC ID nº 6.
6. Polipéptido según cualquiera de las reivindicaciones 1-5, que consiste en los aminoácidos 20 a 988 de la SEC ID nº 6.
7. Polipéptido según la reivindicación 1, que es codificado por el polinucleótido contenido en plásmido pJSF9b que está contenido en E. coli NRRL B-30856.
8. Polinucleótido aislado que comprende una secuencia de nucleótidos que codifica el polipéptido según cualquiera de las reivindicaciones 1-7. 25
9. Constructo de ácidos nucleicos que comprende el polinucleótido según la reivindicación 8 operativamente enlazado a una o varias secuencias de control que dirigen la producción del polipéptido en un huésped de expresión.
10. Vector de expresión recombinante que comprende el constructo de ácidos nucleicos según la reivindicación 9. 30
11. Célula huésped recombinante que comprende el constructo de ácidos nucleicos según la reivindicación 9.
12. Método para producir el polipéptido según cualquiera de las reivindicaciones 1-7 que comprende (a) cultivar una célula, que en su forma tipo salvaje es capaz de producir el polipéptido, bajo condiciones propicias para la producción 35 del polipéptido; y (b) recuperar el polipéptido.
13. Método para producir el polipéptido según cualquiera de las reivindicaciones 1-7 que comprende (a) cultivar una célula huésped que comprende un constructo de ácidos nucleicos que comprende una secuencia de nucleótidos que codifica el polipéptido bajo condiciones propicias para la producción del polipéptido; y (b) recuperar el polipéptido. 40
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
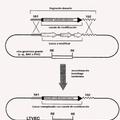 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]