COMPUESTOS PARA SER USADOS EN EL TRATAMIENTO DE ENFERMEDADES BASADAS EN LA EXPRESIÓN DE TRANSCRITOS TÓXICOS CON REPETICIONES CUG O CCUG.
Compuestos para ser usados en el tratamiento de enfermedades basadas en la expresión de transcritos tóxicos con repeticiones CUG o CCUG.
La presente invención hace referencia a moléculas peptídicas, concretamente hexapéptidos, para la prevención y/o tratamiento de enfermedades cuya etiología se basa en la presencia de transcritos tóxicos que comprenden repeticiones CUG o CCUG, preferentemente: DM1, DM2 y SCA8.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201030462.
Solicitante: UNIVERSITAT DE VALENCIA.
Nacionalidad solicitante: España.
Inventor/es: PEREZ PAYA, ENRIQUE, PEREZ ALONSO,MANUEL, ARTERO ALLEPUZ,RUBEN DARIO, GARCÍA LÓPEZ,AMPARO, ORZAEZ CALATAYUD,MARIA DEL MAR, LLAMUSI TROISI,MARIA BEATRIZ.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/08 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 5 a 11 aminoácidos.
- A61P21/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema muscular o neuromuscular.
- A61P25/14 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › para el tratamiento de movimientos anormales, p.ej. corea, disquinesia.
- C07K7/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 5 a 11 aminoácidos.
PDF original: ES-2365967_A1.pdf
Fragmento de la descripción:
Compuestos para ser usados en el tratamiento de enfermedades basadas en la expresión de transcritos tóxicos con repeticiones CUG o CCUG.
Campo de la invención
La presente invención hace referencia a compuestos que comprenden hexapéptidos, para ser usados en la prevención y/o tratamiento de enfermedades cuya etiología se basa en la expresión de transcritos tóxicos que comprenden repeticiones CUG o CCUG como, por ejemplo, Distrofia Miotónica tipo 1 (DM1), Distrofia Miotónica tipo 2 (DM2) y Ataxia Espinocerebelar de tipo 8 (SCA8).
Por lo tanto la presente invención puede ser englobada en el campo de la medicina en general y más específicamente en el campo relacionado con la prevención y/o tratamiento de enfermedades genéticas de carácter hereditario.
Estado de la técnica
La DM1 o enfermedad de Steinert (DM1, OMIM #160900) es el tipo de distrofia muscular más frecuente en la población adulta con una prevalencia mundial de aproximadamente 1 paciente cada 8000 personas, siendo clasificada como enfermedad rara. Es una enfermedad neuromuscular, con síntomas definitorios que afectan principalmente al músculo, tales como miotonía y debilidad muscular, aunque es característicamente multisistémica viéndose afectados entre otros órganos y sistemas el sistema cardiaco (arritmias cardiacas), el ocular (cataratas), el endocrino (hiperinsulinemia) y el sistema reproductor (hipogonadismo).
A nivel genético la DM1 presenta un patrón de herencia autosómico dominante, penetrancia alta y expresividad variable. El origen de la enfermedad está en una mutación dinámica en la región 3' no traducida (3'UTR) del gen proteína quinasa de la distrofia miotónica (DMPK, Entrez #1760), localizada en la región cromosómica 19q13.2-q13.3. Dicha mutación consiste en una expansión anormal de repeticiones del trinucleótido CTG en el exón 15 de dicho gen DMPK, que en la población sana aparece en número variable de entre 5-35 copias, mientras que en los pacientes se encuentra en número mayor de 50. El número de tripletes CTG correlaciona con la gravedad de los síntomas y edad a la que éstos aparecen. Así, para los casos en los que el número de repeticiones oscila entre 50 y unos pocos cientos se habla de DM1 de inicio adulto, donde las primeras manifestaciones clínicas suelen aparecer en la segunda década de vida. Para los casos en los que el número de repeticiones es mayor, alcanzando incluso los miles de copias, la patología se manifiesta ya desde el nacimiento en forma de DM congénita (DMC o enfermedad de Thomsen), siendo ésta la variante más grave de la enfermedad, con síntomas como retraso mental, trastornos respiratorios y problemas en la diferenciación muscular, entre otros.
En los últimos años, se han propuesto una serie de hipótesis en relación a mecanismos moleculares relacionados con la patogénesis de la DM1, siendo uno de los más consensuados la ganancia de función tóxica del ARN. Según este mecanismo los ARNs portadores de expansiones CUG forman horquillas que resultan tóxicas para las células que las expresan provocando, entre otras alteraciones moleculares, cambios en el splicing alternativo de transcritos definidos, por secuestro de factores reguladores del mismo. Un apoyo decisivo para esta hipótesis proviene del trabajo de Mankodi et al. (2000) en ratones transgénicos. Dichos ratones expresan aproximadamente 250 repeticiones del trinucleótido CUG en un ARNm heterólogo desarrollando miotonía y defectos musculares típicos de la DM1, demostrando que las expansiones CUG ejercen un efecto tóxico por sí mismas independientemente del contexto en el que estén (Mankodi et al., 2000). Posteriormente, otros modelos generados en Drosophila confirmaron la toxicidad de las repeticiones CUG independientemente de DMPK (García-López et al., 2008).
Desde el descubrimiento de que ARNs con expansiones CUG pueden resultar tóxicos para las células, toda una serie de evidencias científicas apoyan que estas expansiones, o expansiones parecidas, en otros ARNs, pueden originar patologías genéticas hereditarias semejantes a la DM1. Por ejemplo, en la DM2, las expansiones del tetranucleótido CCUG en el primer intrón de los ARNs transcritos del gen ZNF9 (proteína de dedos de zinc 9, Entrez #7555) desencadenan una patología muy semejante a la DM1 (OMIM #602668). De hecho en el estado de la técnica es conocida la existencia de genes relacionados con la función nerviosa que presentan niveles alterados tanto en pacientes de DM1 como de DM2, lo cual apoya la idea de un mecanismo de patogénesis común a ambas enfermedades.
Por su parte, la ataxia espinocerebelar tipo 8 (SCA8, OMIM #603680) es una enfermedad neurodegenerativa causada por la expansión de tripletes CTG en un transcrito no codificante del gen SCA8. Se ha visto que la transcripción bidireccional de este gen conduce tanto a la expresión de ARNs con expansiones CUG (no traducidos), que desencadenan alteraciones moleculares relacionadas con las descritas para la DM1, como a transcritos con expansiones CAG que se traducen en proteínas con poliglutaminas.
En el núcleo, los ARNs portadores de expansiones CUG se pliegan formando una estructura en horquilla capaz de unir y secuestrar factores de unión al ARN, formando grandes inclusiones ribonucleoproteicas. Hasta la fecha, se ha descrito que las repeticiones CUG interfieren con la actividad de un número creciente de proteínas nucleares, las cuales incluyen factores de transcripción y factores de splicing alternativo. Entre éstos últimos se encuentran las ribonucleoproteínas heterogéneas nucleares hnRNP F y hnRNP H, así como las proteínas de la familia MBNL1-3 (Muscleblind-like proteins). Debido a este secuestro, los pacientes presentan alteraciones en el procesado alternativo de centenares de transcritos específicos, lo que llevó a acuñar el término de espliceopatía, para la cual la DM es el primer ejemplo descrito. También se ha propuesto que la actividad de distintos microARNs podría verse alterada.
El secuestro de proteínas nucleares impide a las mismas realizar sus funciones normales en la célula. Se han aislado y caracterizado varias proteínas capaces de unirse a horquillas CUG de doble cadena tanto in vitro como in vivo. Entre ellas destacan factores de transcripción como la proteína de especificidad 1 (Sp1), el receptor gamma del ácido retinoico (RARγ) o los miembros de la familia de transductores de señal y activadores de la transcripción STAT1 y STAT3. Algunos de estos factores pueden llegar a sufrir un secuestro de hasta el 90% en células DM1 en cultivo, lo cual les impide activar la transcripción de sus genes diana, disminuyendo así su expresión.
Otros factores de transcripción alterados en la DM1 son NKX2-5 y MyoD. Estas proteínas están relacionadas con el desarrollo y conducción cardíaca, y con la diferenciación de mioblastos, respectivamente. Los niveles de NKX2-5 están aumentados en los pacientes, mientras que MyoD está reducida. El motivo por el cual los niveles de estos factores de transcripción están desregulados, así como su relación con la formación de horquillas CUG, se desconoce.
Hasta la fecha varios trabajos han demostrado que las repeticiones CUG afectan a la expresión de un gran número de genes. Utilizando microarrays de ratón, se han detectado al menos 175 transcritos musculares alterados por la expresión de transcritos CUG expandidos. Además, al menos 128 transcritos están también desregulados en ratones knockout de MBNL1, sugiriendo que el secuestro y subsiguiente pérdida de función de MBNL1 juega un papel crucial en la enfermedad.
Los ratones knockout de MBNL1 presentan cataratas del tipo iridiscente, sufren miotonía y defectos histológicos a nivel muscular. Los ratones knockout de MBNL2 también desarrollan miotonía (por un procesado incorrecto de los transcritos Clcn-1) y otras alteraciones musculares típicas de la DM1. Además, la sobreexpresión de MBNL1 en ratones modelo que expresan 250 repeticiones CTG revierte los defectos en el procesado de al menos 4 transcritos (Serca1, Clcn1, Tnnt3 y ZASP), así como la miotonía. En Drosophila, los embriones mutantes mbl presentan desorganización de las bandas Z de los sarcómeros, hipercontracción del abdomen y alteraciones en el procesado alternativo de transcritos como ZASP, troponina T (tnT) y la α-actinina. Del mismo modo, la sobreexpresión de MBNL1 en moscas modelo que expresan 480 repeticiones CTG suprime fenotipos provocados por las repeticiones. Todos estos resultados supusieron un importante... [Seguir leyendo]
Reivindicaciones:
1. Compuesto que comprende un hexapéptido de Fórmula I, sales, derivados, o estereoisómeros farmacéuticamente aceptables del mismo:
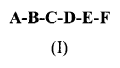
donde:
A puede ser cualquiera de los aminoácidos c ó p,
B puede ser cualquiera de los aminoácidos p ó q,
C es el aminoácido y,
D puede ser cualquiera de los aminoácidos a ó t,
E puede ser cualquiera de los aminoácidos q ó w, y
F es el aminoácido e.
2. Compuesto, según la reivindicación 1, seleccionado del grupo: SEQ ID NO: 1 a SEQ ID NO: 19.
3. Compuesto, según la reivindicaciones 1 ó 2, que consiste en un hexapéptido de secuencia SEQ ID NO: 10.
4. Compuesto, según las reivindicaciones 1 a 3, caracterizado porque los aminoácidos que forman parte de la Fórmula I son L-aminoácidos, D-aminoácidos o mezclas de los mismos.
5. Compuesto, según cualquiera de las reivindicaciones anteriores, que comprende un hexapéptido de Fórmula I en configuración directa o retroinversa.
6. Uso de un compuesto según cualquiera de las reivindicaciones anteriores para preparar un medicamento.
7. Uso de al menos un compuesto de las reivindicaciones 1 a 5, según la reivindicación 6, para la elaboración de una composición farmacéutica destinada a la prevención y/o tratamiento de enfermedades cuya etiología se basa en la presencia de transcritos tóxicos que comprenden repeticiones CUG o CCUG, comprendidas en el grupo: DM1, DM2 y SCA8.
8. Composición farmacéutica que comprende al menos un compuesto de las reivindicaciones 1 a 5.
Patentes similares o relacionadas:
Péptido basado en colágeno tipo II alfa-1 útil para el tratamiento de una enfermedad de la superficie ocular, del 15 de Julio de 2020, de EYEBIO KOREA: Un péptido que consiste en una secuencia de aminoácidos representada por SEQ ID NO: 1.
Péptido que tiene actividad antiinflamatoria, y uso del mismo, del 8 de Julio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en una secuencia de aminoácidos de SEQ ID NO: 1, SEQ ID NO: 2 o SEQ ID NO: 3.
Péptido que tiene actividades antiinflamatoria, osteogénica y promotora del crecimiento del cabello, y uso del mismo, del 24 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que tiene actividad antiinflamatoria, que consiste en la secuencia de aminoácidos SEQ ID NO: 2.
Nueva inmunoterapia contra diversos tumores como el cáncer gastrointestinal y gástrico, del 24 de Junio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido seleccionado del grupo siguiente: a) péptido consistente en la secuencia conforme a la SEQ ID N.º 86, b) el péptido conforme a a), en la […]
Anticuerpos monoclonales humanizados y quiméricos para CD99, del 17 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un anticuerpo monoclonal humanizado aislado que se une específicamente a CD99 humano, y comprende: (a) una cadena ligera que comprende la secuencia de aminoácidos expuesta […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.
Péptido que tiene actividades antiinflamatoria, osteogénica y de fomento del crecimiento del pelo, y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Péptido que tiene actividad antiinflamatoria, que consiste en secuencias de aminoácidos de SEQ ID NO: 3.
Inmunoterapia WT1 para enfermedad angiogénica intraocular, del 17 de Junio de 2020, de INTERNATIONAL INSTITUTE OF CANCER IMMUNOLOGY, INC.: Una composición farmacéutica que comprende un péptido WT1 o péptido WT1 variante para su uso en el tratamiento y/o prevención de una enfermedad […]