COMPUESTOS DE GLP-1 ACILADOS.
Análogo de GLP-1 teniendo al menos un residuo de aminoácido no proteogénico en las posiciones 7 y/o 8 en relación a la secuencia GLP-1 (7-37),
la cual se acila con una fracción B-U' al residuo de lisina en la posición 26, donde (i) B-U' comprende al menos dos grupos acídicos, uno de los cuales está unido terminalmente; (ii) U' se selecciona a partir de y dondem es 0, 1, 2, 3, 4, 5, ó 6, n es 1, 2, ó 3, s es 0, 1, 2, ó 3, t es 0, 1, 2, 3, ó 4, p es 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17,18, 19, 20, 21, 22, ó 23; y (iii) B es un grupo acídico seleccionado a partir de donde l es 12, 13, 14, 15, 16, 17, 18, 19, ó 20
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/060855.
Solicitante: NOVO NORDISK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: CORPORATE PATENTS NOVO ALLE P.O. BOX 3000 DK-2880 BAGSVAERD DINAMARCA.
Inventor/es: LAU, JESPER, MADSEN, KJELD, HANSEN,THOMAS,KRUSE, STEPHENSEN,HENRIK, BLOCH,PAW, ZARAGOZA DORWALD,FLORENCIO.
Fecha de Publicación: .
Fecha Solicitud PCT: 20 de Marzo de 2006.
Fecha Concesión Europea: 4 de Agosto de 2010.
Clasificación Internacional de Patentes:
- C07K14/605 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Glucagones.
Clasificación PCT:
- A61K38/26 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Glucagón.
- A61K47/48
- C07K14/605 C07K 14/00 […] › Glucagones.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
Compuestos de GLP-1 acilados.
Campo de la invención
Esta invención se refiere al campo de péptidos terapéuticos, es decir a nuevos compuestos de GLP-1 extendidos.
Antecedentes de la invención
Se ha usado una variedad de enfoques diferentes para modificar la estructura del péptido 1 tipo glucagón (GLP-1) para proporcionar una mayor duración de acción in vivo.
WO 96/29342 expone derivados de hormonas peptídicas donde la hormona peptídica progenitora se ha modificado introduciendo un sustituyente lipofílico en el residuo de aminoácido C-terminal o en el residuo de aminoácido N-terminal.
WO 98/08871 expone derivados de GLP-1 donde al menos un residuo de aminoácido del péptido progenitor tiene un sustituyente lipofílico ligado.
WO 99/43708 expone derivados de GLP-1 (7-35) y GLP-1 (7-36) los cuales tienen un sustituyente lipofílico fijado al residuo de aminoácido C-terminal.
WO 00/34331 expone análogos de GLP-1 acilados.
WO 00/69911 expone péptidos insulinotrópicos activados para inyectarse en pacientes donde estos supuestamente deben reaccionar con componentes de la sangre para formar conjugados y así supuestamente proporcionando una mayor duración de acción in vivo.
WO 02/46227 expone análogos de GLP-1 y de exendin-4 fusionados a albúmina de suero humana para extender la vida media in vivo.
Muchos pacientes de diabetes particularmente en el segmento de la diabetes de tipo 2 están sujetos a la denominada "Belonefobia", es decir un miedo sustancial de pincharse ellos mismos. En el segmento de la diabetes de tipo 2 la mayoría de pacientes se tratan con agentes hipoglucémicos orales, y debido a que los compuestos de GLP-1 se prevee que sean el primer producto inyectable a administrar a estos pacientes, el miedo a las inyecciones pueden llegar a ser un obstáculo serio para el uso difundido de los compuestos de GLP-1 los cuales son muy prometedores a nivel clínico. Por tanto, hay una necesidad de desarrollar nuevos compuestos de GLP-1 que se puedan administrar menos de una vez al día, por ejemplo una vez cada segundo o tercer día preferiblemente una vez a la semana, reteniéndose a la vez un perfil clínico aceptable.
Resumen de la invención
La invención proporciona un análogo de GLP-1 teniendo una modificación de al menos un residuo de aminoácido no proteogénico en las posiciones 7 y/o 8 en relación a la secuencia de GLP-1 (7-37) (SEC ID Nº 1), el cual está acilado con una fracción B-U' tal y como se define abajo para el residuo de lisina en la posición 26, y donde dicha fracción comprende al menos dos grupos acídicos, donde un grupo acídico está unido terminalmente.
La presente invención también proporciona composiciones farmacéuticas comprendiendo un compuesto según la presente invención y un excipiente farmacéuticamente aceptable, y el uso de compuestos según la presente invención para preparar medicamentos para tratar la enfermedad.
La invención proporciona un método para aumentar el tiempo de acción en un paciente de un análogo de GLP-1 en más de aproximadamente 40 horas, caracterizado por modificar al menos uno de los residuos de aminoácido en las posiciones 7 y 8 de un péptido de GLP-1 (7-37) o un análogo del mismo, y acilar dicho análogo de GLP-1 con una fracción B-U' como se describe abajo en el residuo de lisina en la posición 26 de dicho análogo de GLP-1.
La fracción B-U' comprende al menos dos grupos acídicos, uno de los cuales está unido terminalmente; U' está seleccionado de

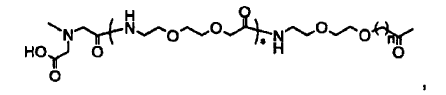

donde m es 0, 1, 2, 3, 4, 5, ó 6: n es 1, 2, ó 3; s es 0, 1, 2, ó 3; t es 0, 1, 2, 3, ó 4; p es 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17,18, 19, 20, 21, 22, ó 23; y B es un grupo acídico seleccionado de
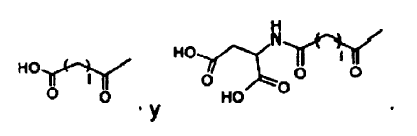
donde l es 12, 13, 14, 15, 16, 17, 18, 19, ó 20.
Descripción de la invención
En la presente especificación, los siguientes términos tienen el significado indicado:
El término "polipéptido" y "péptido" como se utiliza en este caso significa un compuesto compuesto por al menos cinco constituyente aminoácidos conectados por enlaces peptídicos. Los aminoácidos constituyentes pueden ser del grupo de los aminoácidos codificados por el código genético y estos pueden ser aminoácidos naturales los cuales no están no codificados por el código genético, al igual que aminoácidos sintéticos. Los aminoácidos naturales que no están codificados por el código genético son por ejemplo, γ-carboxiglutamato, ornitina, fosfoserina, D-alanina y D-glutamina. Los aminoácidos sintéticos comprenden aminoácidos fabricados por síntesis química, es decir D-isómeros de los aminoácidos codificados por el código genético tal como D-alanina y D-leucina, Aib (ácido α-aminoisobutírico), Abu (ácido α-aminobutirico), Tle (terc-butilglicina), β-alanina, ácido benzoico de 3-aminometilo, ácido antranílico.
Los 22 aminoácidos proteogénicos son: Alanina, Arginina, Asparagina, Ácido aspártico, Cisteína, Cistina, glutamina, Ácido glutámico, Glicina, Histidina, Hidroxiprolina, Isoleucina, Leucina, Lisina, Metionina, Fenilalanina, Prolina, Serina, Treonina, Triptófano, Tirosina, Valina.
Así un aminoácido no proteogénico es una fracción la cual se puede incorporar en un péptido a través de enlaces peptídicos pero no es un aminoácido proteogénico. Ejemplos son γ-carboxiglutamato, ornitina, fosfoserina, D-aminoácidos tales como D-alanina y D-glutamina, los aminoácidos sintéticos no proteogénicos comprenden aminoácidos fabricados por síntesis química, es decir D-isómeros de los aminoácidos codificados por el código genético tal como D-alanina y D-leucina, Aib (ácido α-aminoisobutírico), Abu (ácido α-aminobutírico), Tle (terc-butilglicina), ácido benzoico de 3-aminometilo, ácido antranílico, desamino-Histidina, los análogos beta de aminoácidos tales como β-alanina, etc. D-histidina, desamino-histidina, 2-amino-histidina, β-hidroxi-histidina, homohistidina, Nα-acetilo-histidina, α-fluorometil-histidina, α-metilo-histidina, 3-piridilalanina, 2-piridilalanina o 4-piridilalanina, (1-aminociclopropilo) ácido carboxílico, (1-aminociclobutilo) ácido carboxílico, (1-aminociclopentilo) ácido carboxílico, (1-aminociclohexilo) ácido carboxílico, (1-aminocicloheptilo) ácido carboxílico, o (1-aminociclooctilo) ácido carboxílico.
El término "análogo" como se usa aquí en referencia a un polipéptido significa un péptido modificado donde uno o más residuos de aminoácido del péptido se han sustituido por otros residuos de aminoácido y/o donde uno o más residuos de aminoácido se han delecionados del péptido y/o donde uno o más residuos de aminoácido se han delecionado del péptido y o donde uno o más residuos de aminoácido se han añadido al péptido. Tal adición o deleción de residuos de aminoácido puede tener lugar en el N-terminal del péptido y/o en el C-terminal del péptido. Un sistema simple se usa frecuentemente para describir análogos: por ejemplo [Arg34]GLP-1 (7-37)Lys designa un análogo de GLP-1 (7-37) donde la lisina producida naturalmente en posición 34 se ha sustituido por arginina y donde se ha añadido una lisina al residuo de aminoácido terminal, es decir a Gly37.Todos los aminoácidos para los cuales el isómero óptico no está indicado se deben entender por significar el L-isómero. En formas de realización de la invención se han modificado un máximo de 17 aminoácidos. En las formas de realización de la invención se han modificado un máximo de 15 aminoácidos. En formas de realización de la invención se han modificado un máximo de 10 aminoácidos. En formas de realización de la invención se han modificado un máximo de 8 aminoácidos. En formas de realización de la invención se han modificado un máximo de 7 aminoácidos. En formas de realización de la invención se han modificado un máximo de 6 aminoácidos. En formas de realización de la invención se han modificado un máximo...
Reivindicaciones:
1. Análogo de GLP-1 teniendo al menos un residuo de aminoácido no proteogénico en las posiciones 7 y/o 8 en relación a la secuencia GLP-1 (7-37), la cual se acila con una fracción B-U' al residuo de lisina en la posición 26, donde
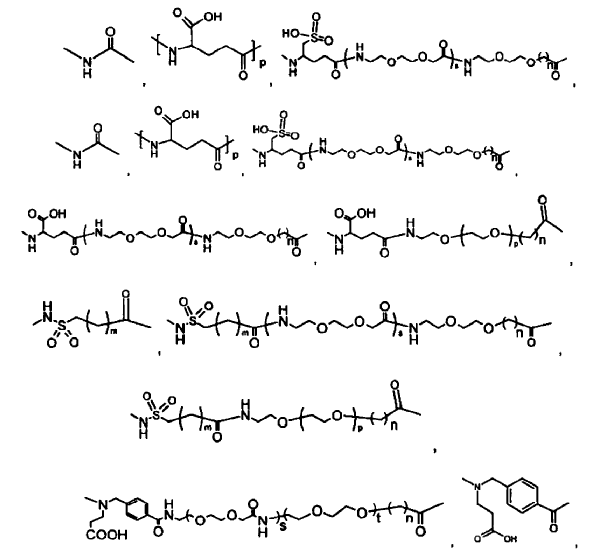
y

donde
m es 0, 1, 2, 3, 4, 5, ó 6,
n es 1, 2, ó 3,
s es 0, 1, 2, ó 3,
t es 0, 1, 2, 3, ó 4,
p es 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17,18, 19, 20, 21, 22, ó 23; y (iii) B es un grupo acídico seleccionado a partir de
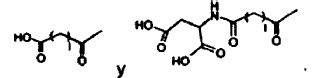
donde l es 12, 13, 14, 15, 16, 17, 18, 19, ó 20.
2. Análogo de GLP-1 según la reivindicación 1, el cual es un compuesto de la Fórmula I (SEC ID nº. 2):

donde
Xaa7 es L-histidina, imidazopropionil, α-hidroxi-histidina, D-histidina, desamino-histidina, 2-amino-histidina, β-hidroxi-histidina, homohistidina, Nα-acetilo-histidina, Nα-formil-histidina, α-fluorometil-histidina, α-metil-histidina, 3-piridilalanina, 2-piridilalanina o 4-piridilalanina;
Xaa8 es Ala, Gly, Val, Leu, Ile, Thr, Ser, Lys, Aib, ácido carboxílico (1-aminociclopropil), ácido carboxílico (1-aminociclobutil), ácido carboxílico (1-aminociclopentil), ácido carboxílico (1-aminociclohexil), ácido carboxílico (1-aminocicloheptil), o ácido carboxílico (1-aminociclooctil); Xaa16 es Val o Leu;
Xaa18 es Ser, Lys, o Arg;
Xaa19 es Tyr o Gln;
Xaa20 es Leu o Met;
Xaa22 es Gly, Glu, o Aib;
Xaa23 es Gln, Glu, Lys, o Arg;
Xaa25 es Ala o Val;
Xaa27 es Glu o Leu;
Xaa30 es Ala, Glu, o Arg;
Xaa33 es Val o Lys;
Xaa34 es Lys, Glu, Asn, o Arg;
Xaa35 es Gly o Aib;
Xaa36 es Arg, Gly, o Lys, o está ausente;
Xaa37 es Gly, Ala, Glu, Pro, Lys, o está ausente.
3. Análogo de GLP-1 según las reivindicaciones 1-2, donde m es 2, 3, 4, ó 5; n es 1 ó 2; s es 0, 1, ó 2; t es 0, 1, 2, ó 3; p es 1, 2, 3, 4, 7, 11, ó 23.
4. Análogo de GLP-1 según las reivindicaciones 1-3 donde B-U'- es


donde l es 14, 15, 16, 17, 18, 19, ó 20,
p es 1, 2, 3, 4, 7, 8, 9, 10, 11, ó 12,
s es 0, 1, ó 2,
t es 0 ó 1,
m es 2, 3, ó 4.
5. Análogo de GLP-1 según la reivindicación 4, donde l es 14, 15, 16, 17, ó 18; p es 1, 2, 3, 4, ó 11; s es 0, 1, ó 2; t es 0 ó 1.
6. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-5, donde s es 1.
7. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-5, donde l es 16.
8. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-5, donde p es 3 ó 4.
9. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-5, donde n es 1.
10. Análogo de GLP-1 según cualquiera de las reivindicaciones 2-9, donde Xaa7 es His o desamino-histidina; Xaa8 es Ala, Gly, Val, Leu, Ile, Lys, o Aib; Xaa16 es Val; Xaa18 es Ser; Xaa19 es Tyr; Xaa20 es Leu; Xaa22 es Gly, Glu, o Aib; Xaa23 es Gln o Glu; Xaa25 es Ala; Xaa27 es Glu; Xaa30 es Ala o Glu; Xaa33 es Val; Xaa34 es Lys o Arg; Xaa35 es Gly o Aib; Xaa36 es Arg o Lys; Xaa37 es Gly, amida, o está ausente.
11. Análogo de GLP-1 según la reivindicación 10, donde Xaa7 es His; Xaa8 es Gly o Aib; Xaa16 es Val; Xaa18 es Ser; Xaa19 es Tyr; Xaa20 es Leu; Xaa22 es Glu o Aib; Xaa23 es Gln; Xaa25 es Ala; Xaa27 es Glu; Xaa30 es Ala; Xaa33 es Val; Xaa34 es Lys o Arg; Xaa35 es Gly o Aib; Xaa36 es Arg; Xaa37 es Gly.
12. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-11, donde dicho análogo de GLP-1 comprende una modificación de la L-histidina N-terminal en la posición 7 de la secuencia de GLP-1 (7-37).
13. Análogo GLP-1 según la reivindicación 12, donde dicho análogo de GLP-1 comprende imidazopropionil7, α-hidroxi-histidina7 o N-metil-histidina7, D-histidina7, desamino-histidina7, 2-amino-histidina7, β-hidroxi-histidina7, homohistidina7, Nα-acetil-histidina7, α-fluorometil-histidina7, α-metil-histidina7, 3-piridilalanina, 2-piridilalanina7, o 4-piridilalanina7.
14. Análogo de GLP-1 según cualquiera de las reivindicaciones 1-13, donde dicho análogo de GLP-1 comprende una sustitución de L-alanina en la posición 8 de la secuencia de GLP-1 (7-37) por otro residuo de aminoácido.
15. Análogo de GLP-1 según la reivindicación 14, donde dicho análogo de GLP-1 comprende Aib8, Gli8, Val8, Ile8, Leu8, Ser8, Tr8, (1-aminociclopropil) ácido carboxílico, (1-aminociclobutil) ácido carboxílico, (1-aminociclopentil) ácido carboxílico, (1-aminociclohexil) ácido carboxílico, (1-aminocicloheptil) ácido carboxílico, o (1-aminociclooctil) ácido carboxílico.
16. Análogo de GLP-1 según la reivindicación 15, donde dicho análogo de GLP-1 comprende Aib8.
17. Análogo de GLP-1 según cualquiera de las reivindicaciones precedentes, donde dicho análogo de GLP-1 comprende no más de quince residuos de aminoácidos que han sido cambiados, añadidos o delecionados en comparación con GLP-1 (7-37) (SEC ID Nº. 1).
18. Análogo de GLP-1 según la reivindicación 17, donde no más de diez residuos de aminoácidos han sido cambiados, añadidos o delecionados en comparación con GLP-1 (7-37) (SEC ID nº. 1).
19. Análogo de GLP-1 según la reivindicación 18, donde no más de seis residuos de aminoácidos han sido cambiados, añadidos o delecionados en comparación con GLP-1 (7-37) (SEC ID nº. 1).
20. Análogo de GLP-1 según cualquiera de las reivindicaciones anteriores, donde dicho análogo de GLP-1 comprende no más de 3 residuos de aminoácidos los cuales no están codificados por el código genético.
21. Análogo de GLP-1 según cualquiera de las reivindicaciones precedentes, donde dicho análogo de GLP-1 comprende sólo un residuo de lisina.
22. Análogo de GLP-1 según cualquiera de las reivindicaciones anteriores, el cual es Aib8,Arg34-GLP-1(7-37), Aib8,22,Arg34-GLP-1(7-37), [3-(4-Imidazolil)Propionil7,Arg34]GLP-1-(7-37)péptido, Aib8,Arg34,Pro37-GLP-1(7-37), o Aib8,22,27,30,35,Arg34,Pro37-GLP-1(7-37)amida; todos los cuales son sustituidos por B-U' en la posición 26.
23. Compuesto según cualquiera de las reivindicaciones precedentes, el cual está seleccionado de entre
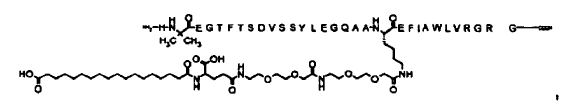
N-
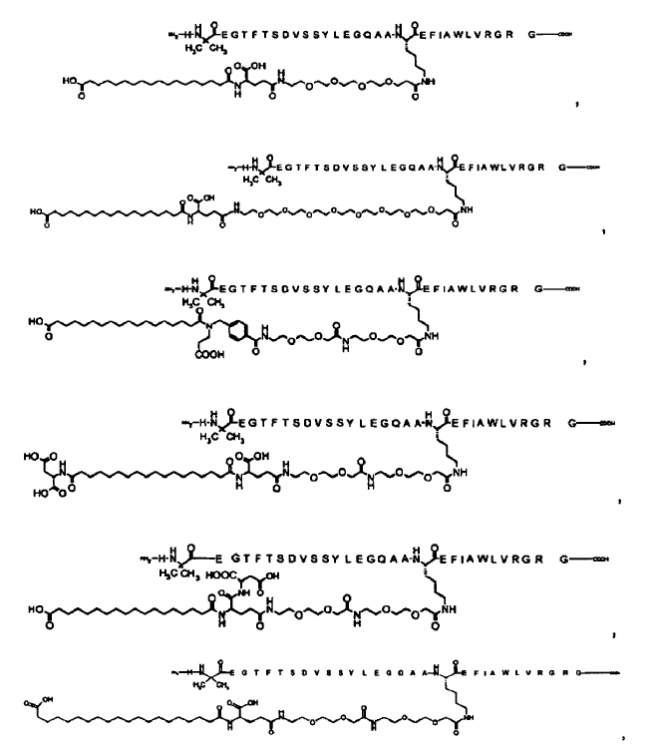
N-
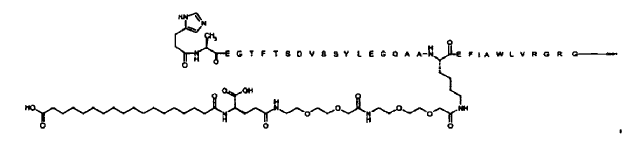
N-

N-
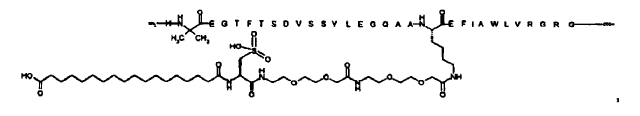
N-
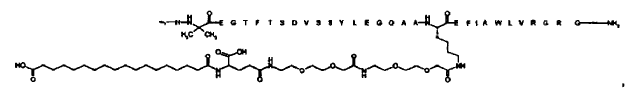
N-
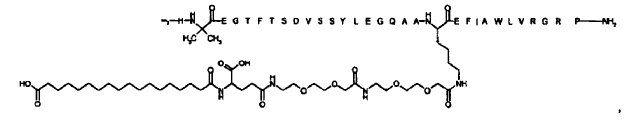
N-
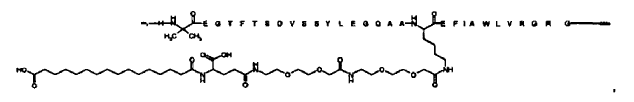
Aib8,Lys26(N-
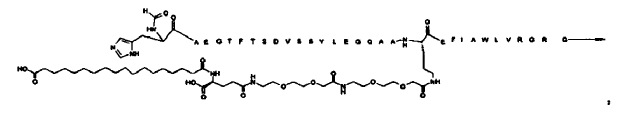
N-α7-formil, N-
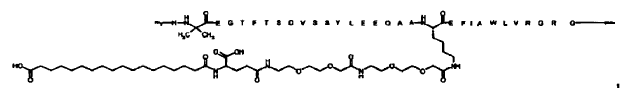
N-
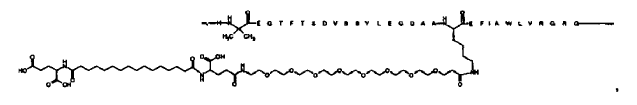
N-
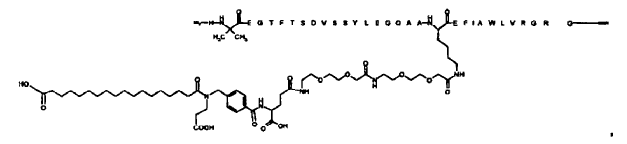
N-

N-
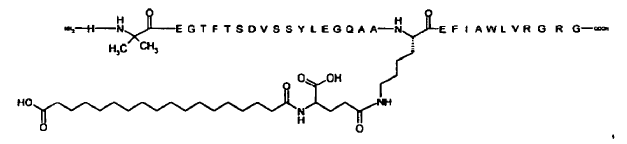
N-
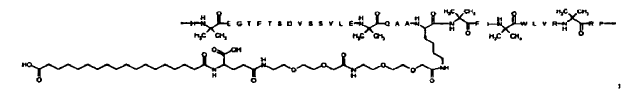
N-
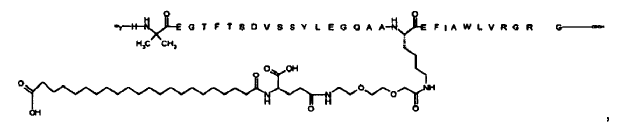
N-
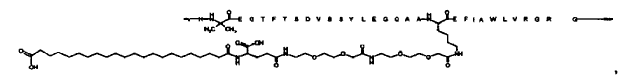
N-
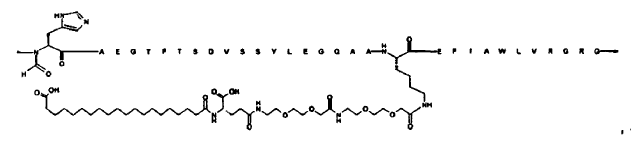
y
N-α1-formil-N-
24. Método para aumentar el tiempo de acción en un paciente de un análogo de GLP-1 a más de aproximadamente 40 horas, caracterizado por el hecho de modificar al menos uno de los residuos de aminoácido en las posiciones 7 y 8 de un péptido GLP-1 (7-37) o un análogo del mismo, y acilar dicho análogo de GLP-1 con una fracción B-U'- como se describe en cualquiera de las reivindicaciones precedentes en el residuo de lisina en la posición 26 de dicho análogo de GLP-1.
25. Composición farmacéutica comprendiendo un compuesto según cualquiera de las reivindicaciones 1-23, y un excipiente farmacéuticamente aceptable.
26. Composición farmacéutica según la reivindicación 25, la cual es adecuada para su administración parenteral.
27. Uso de un compuesto según cualquiera de las reivindicaciones 1-23 para la preparación de un medicamento.
28. Uso de un compuesto según cualquiera de las reivindicaciones 1-23 para la preparación de un medicamento para el tratamiento o prevención de hiperglicemia, diabetes de tipo 2, tolerancia a la glucosa alterada, diabetes de tipo 1, obesidad, hipertensión, síndrome X, dislipidemia, trastornos cognitivos, aterosclerosis, infarto miocardial, cardiopatía coronaria y otros trastornos cardiovasculares, derrame cerebral, síndrome de intestino inflamatorio, dispepsia, y úlceras gástricas.
29. Uso de un compuesto según cualquiera de las reivindicaciones 1-23 para la preparación de un medicamento para retardar o impedir la progresión de la enfermedad en la diabetes de tipo 2.
30. Uso de un compuesto según cualquiera de las reivindicaciones 1-23 para la preparación de un medicamento para reducir la ingesta de alimentos, reducir la apoptosis β-celular, aumentar la función β-celular y la masa β-celular, y/o restaurar la sensibilidad a la glucosa de las β-células.
31. Compuesto según cualquiera de las reivindicaciones 1-23 para su uso como un medicamento.
32. Compuesto según cualquiera de las reivindicaciones 1-23 para su uso en el tratamiento o la prevención de hiperglicemia, diabetes de tipo 2, tolerancia a la glucosa alterada, diabetes de tipo 1, obesidad, hipertensión, síndrome X, dislipidemia, trastornos cognitivos, aterosclerosis, infarto miocardial, cardiopatía coronaria y otros trastornos cardiovasculares, derrame cerebral, síndrome de intestino inflamatorio, dispepsia, y úlceras gástricas.
33. Compuesto según cualquiera de las reivindicaciones 1-23 para su uso para retardar o impedir la progresión de la enfermedad en la diabetes de tipo 2.
34. Compuesto según cualquiera de las reivindicaciones 1-23 para reducir la ingesta de alimentos, reducir la apoptosis β-celular, aumentar la función β-celular y la masa β-celular, y/o para restaurar la sensibilidad a la glucosa de las β-células.
Patentes similares o relacionadas:
Agonistas del receptor de glucagón, del 24 de Junio de 2020, de ELI LILLY AND COMPANY: Un compuesto agonista del receptor de glucagón que comprende la fórmula: YX1QGTFX2SDYSKYLDX3KKAX4EFVX5WLLEX6X7 en la que X1 es Aib; X2 es T o L; X3 es Aib; […]
Profármacos de GLP-1, del 17 de Junio de 2020, de NOVO NORDISK A/S: Un compuesto de GLP-1 de la fórmula general I: R1 -(NHXaa1)-Xaa2-(OHis)-(péptido GLP-1) (Fórmula I) en donde el péptido GLP-1 es […]
Método para preparar semaglutida, del 13 de Mayo de 2020, de Hybio Pharmaceutical Co., Ltd: Método de preparación de semaglutida, que comprende las etapas de: etapa 1: acoplar Gly a una resina mediante síntesis en fase sólida para obtener Gly-resina; y […]
Coagonistas estables del receptor de GLP-1/glucagón basados en GLP-1, del 6 de Mayo de 2020, de NOVO NORDISK A/S: Un derivado de GLP-1 caracterizado por tener la fórmula: amida de Nε34-[2-[2-[2-[[2-[2-[2-[[(4S)-4-carboxi-4- [[(4S)-4-carboxi-4-(17- carboxiheptadecanoilamino)butanoil]amino]butanoil]amino]etoxi]etoxi]acetil]amino]etoxi]etoxi]acetil]- […]
Una composición para el tratamiento de la diabetes que comprende un análogo de oxintomodulina, del 11 de Marzo de 2020, de HANMI PHARM. CO., LTD.: Una composición para su uso en la prevención o el tratamiento de la diabetes, la composición comprende un conjugado de análogo de oxintomodulina como un ingrediente […]
Modificador de exenatida y uso del mismo, del 12 de Febrero de 2020, de BrightGene Bio-Medical Technology Co., Ltd: Un modificador de exenatida o sales farmacéuticamente aceptables del mismo que tienen actividad del agonista del receptor de GLP-1, como se muestra en la fórmula (I): (Ex-4)-L-Y […]
Derivados de GLP-1 doble-acilados, del 4 de Diciembre de 2019, de NOVO NORDISK A/S: Un derivado de un análogo de GLP-1, cuyo análogo comprende un primer residuo de K en una posición correspondiente a la posición 26 de GLP-1 […]
Análogos de glucagón, del 13 de Noviembre de 2019, de ZEALAND PHARMA A/S: Un compuesto que tiene la fórmula: R1-X-Z-R2 en donde R1 es H (es decir, hidrógeno), alquilo C1-4, acetilo, formilo, benzoílo o trifluoroacetilo; […]